名校
解题方法
1 . 钴广泛应用于机械制造、电子电器、航空航天、电池制造等行业,是国家重要的战略资源。用含钴废料(主要成分为 ,含少量
,含少量 、
、 、CaO、MgO、
、CaO、MgO、 等)制备草酸钴晶体(
等)制备草酸钴晶体( )的工艺流程如图所示,试回答下列问题:
)的工艺流程如图所示,试回答下列问题:
① 具有强氧化性。
具有强氧化性。
② ,
, 。
。
(1)为提高含钴废料的浸出效率,可采取的措施是___________ (任写一条)。
(2) 在水溶液中的电离方程式为
在水溶液中的电离方程式为___________ ;浸出渣的主要成分为___________ (填化学式)。
(3)向“浸出液”中加入适量的 时,
时, 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(4)①“除钙镁”后,滤液中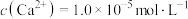 时,
时,
___________  。
。
②若“调pH”时溶液的pH偏低,将会导致 、
、 沉淀不完全,其原因是
沉淀不完全,其原因是___________ 。
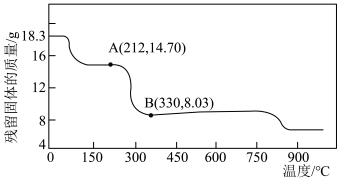
(5)将 在空气中加热最终可得到钴的氧化物。分解时测得残留固体的质量随温度变化的曲线如图所示。[已知:
在空气中加热最终可得到钴的氧化物。分解时测得残留固体的质量随温度变化的曲线如图所示。[已知: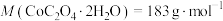 ]
] ,此过程中发生反应的化学方程式为
,此过程中发生反应的化学方程式为___________ 。
 ,含少量
,含少量 、
、 、CaO、MgO、
、CaO、MgO、 等)制备草酸钴晶体(
等)制备草酸钴晶体( )的工艺流程如图所示,试回答下列问题:
)的工艺流程如图所示,试回答下列问题: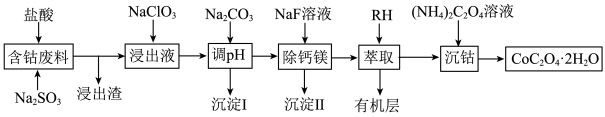
①
 具有强氧化性。
具有强氧化性。②
 ,
, 。
。(1)为提高含钴废料的浸出效率,可采取的措施是
(2)
 在水溶液中的电离方程式为
在水溶液中的电离方程式为(3)向“浸出液”中加入适量的
 时,
时, 发生反应的离子方程式为
发生反应的离子方程式为(4)①“除钙镁”后,滤液中
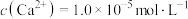 时,
时,
 。
。②若“调pH”时溶液的pH偏低,将会导致
 、
、 沉淀不完全,其原因是
沉淀不完全,其原因是(5)将
 在空气中加热最终可得到钴的氧化物。分解时测得残留固体的质量随温度变化的曲线如图所示。[已知:
在空气中加热最终可得到钴的氧化物。分解时测得残留固体的质量随温度变化的曲线如图所示。[已知: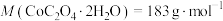 ]
]
 ,此过程中发生反应的化学方程式为
,此过程中发生反应的化学方程式为
您最近一年使用:0次
7日内更新
|
135次组卷
|
5卷引用:2024届内蒙古自治区名校联盟高三下学期联合质量检测(三模)理科综合试题-高中化学
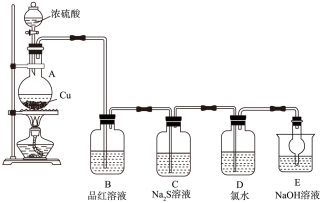
2 . 实验室里研究不同价态硫元素之间的转化。__________ 。
(2)B中的现象是__________ 。
(3)C中的现象是__________ , 在反应中做
在反应中做__________ 剂。
(4)D中氯水褪色,此反应中硫元素的化合价由__________ 转化为__________ ;甲认为可以补充一个实验进一步证明硫元素的价态转化,实验方案和现象为:取D中褪色后的溶液于试管中__________ 。
(5)E的作用是__________ ,离子方程式为__________ 。
(2)B中的现象是
(3)C中的现象是
 在反应中做
在反应中做(4)D中氯水褪色,此反应中硫元素的化合价由
(5)E的作用是
您最近一年使用:0次
解题方法
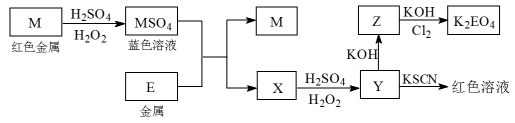
3 . 随着电子工业的发展,电子垃圾的数量逐渐增多,对环境构成了极大的污染。某化学兴趣探究小组将一批废弃的线路板简单处理后,得到红色金属M和金属E并进行如下框图所示转化,获得高效净水剂K2EO4.(答题时,化学式及化学方程式中的M、E均用所对应的元素符号表示):_______ 。
(2)检验X中阳离子的方法和现象是_______ 。
(3)如果各步转化无损失,M转化为MSO4消耗的H2O2与X转化为Y消耗的H2O2的用量之比为:_______ 。
(4)由MSO4的蓝色溶液经一系列操作可以获得蓝色晶体,这些操作中用到的实验仪器除了酒精灯、蒸发皿、铁架台外,还需要用到的玻璃仪器有_____ 、______ 、______ (填写仪器名称)。
(5)某同学利用H2还原MO来测定M的相对原子质量,下图是测定装置示意图,A中试剂是盐酸。_______ (填写偏高、偏低、正常),装置D的作用_______ ;
②连接好装置并检验装置的气密性,检验气密性的方法是:________ 。然后应首先“加热反应管E”还是“从A瓶中逐滴加入液体”?_______ 在这两步之间还应进行的操作是_______ 。
(2)检验X中阳离子的方法和现象是
(3)如果各步转化无损失,M转化为MSO4消耗的H2O2与X转化为Y消耗的H2O2的用量之比为:
(4)由MSO4的蓝色溶液经一系列操作可以获得蓝色晶体,这些操作中用到的实验仪器除了酒精灯、蒸发皿、铁架台外,还需要用到的玻璃仪器有
(5)某同学利用H2还原MO来测定M的相对原子质量,下图是测定装置示意图,A中试剂是盐酸。
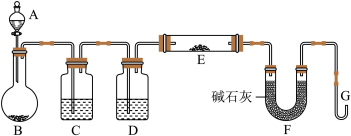
②连接好装置并检验装置的气密性,检验气密性的方法是:
您最近一年使用:0次
解题方法
4 . 硫酸四氨合铜晶体( )常用作杀虫剂、媒染剂。已知:常温下
)常用作杀虫剂、媒染剂。已知:常温下 受热易分解,在空气中会水解生成铜的碱式盐;在溶液中存在以下电离过程:
受热易分解,在空气中会水解生成铜的碱式盐;在溶液中存在以下电离过程: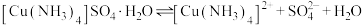 。现以废铜屑(表面沾有油污)为原料制备
。现以废铜屑(表面沾有油污)为原料制备 的实验步骤如下:
的实验步骤如下: 的制备
的制备
(1)步骤①中采取“碱煮水洗”,“碱”是指一种钠盐,其化学式是_____ 。
(2)步骤②在常温下进行,需要加入的试剂有稀 和另一种液态试剂,发生的化学反应方程式为
和另一种液态试剂,发生的化学反应方程式为_____ 。
Ⅱ.晶体的制备
将上述制备的 溶液加入装置A中,滴加
溶液加入装置A中,滴加 氨水时,有浅蓝色沉淀
氨水时,有浅蓝色沉淀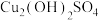 生成;继续滴加氨水,沉淀消失,得到深蓝色
生成;继续滴加氨水,沉淀消失,得到深蓝色 溶液。将A中溶液转移至B中,析出
溶液。将A中溶液转移至B中,析出 晶体;将B中混合物转移至装置C中抽滤(减压过滤),用乙醇洗涤晶体2~3次;取出晶体,冷风吹干。
晶体;将B中混合物转移至装置C中抽滤(减压过滤),用乙醇洗涤晶体2~3次;取出晶体,冷风吹干。_____ 。
(4)抽滤时,抽气泵处于工作状态,活塞需_____ (填“打开”或“关闭”),作用是_____ 。
(5)使用下列试剂可代替乙醇来促进 晶体析出的有
晶体析出的有_____ 。(填标号)
a.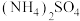 b.稀氨水 c.
b.稀氨水 c. d.
d. 溶液
溶液
(6)晶体采用冷风吹干而不用加热烘干的原因是_____ 。
Ⅲ.废液回收
减压过滤后的废液中含有 、乙醇和氨水,向废液中加入硫酸,回收乙醇并获得
、乙醇和氨水,向废液中加入硫酸,回收乙醇并获得 和的混合溶液。
和的混合溶液。
(7) 溶液受热易分解,则回收乙醇的实验方法为
溶液受热易分解,则回收乙醇的实验方法为_____ 。
 )常用作杀虫剂、媒染剂。已知:常温下
)常用作杀虫剂、媒染剂。已知:常温下 受热易分解,在空气中会水解生成铜的碱式盐;在溶液中存在以下电离过程:
受热易分解,在空气中会水解生成铜的碱式盐;在溶液中存在以下电离过程: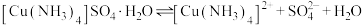 。现以废铜屑(表面沾有油污)为原料制备
。现以废铜屑(表面沾有油污)为原料制备 的实验步骤如下:
的实验步骤如下: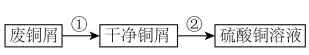
 的制备
的制备(1)步骤①中采取“碱煮水洗”,“碱”是指一种钠盐,其化学式是
(2)步骤②在常温下进行,需要加入的试剂有稀
 和另一种液态试剂,发生的化学反应方程式为
和另一种液态试剂,发生的化学反应方程式为Ⅱ.晶体的制备
将上述制备的
 溶液加入装置A中,滴加
溶液加入装置A中,滴加 氨水时,有浅蓝色沉淀
氨水时,有浅蓝色沉淀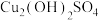 生成;继续滴加氨水,沉淀消失,得到深蓝色
生成;继续滴加氨水,沉淀消失,得到深蓝色 溶液。将A中溶液转移至B中,析出
溶液。将A中溶液转移至B中,析出 晶体;将B中混合物转移至装置C中抽滤(减压过滤),用乙醇洗涤晶体2~3次;取出晶体,冷风吹干。
晶体;将B中混合物转移至装置C中抽滤(减压过滤),用乙醇洗涤晶体2~3次;取出晶体,冷风吹干。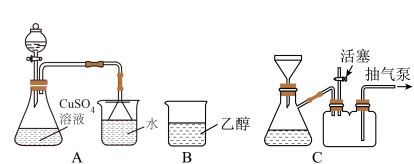
(4)抽滤时,抽气泵处于工作状态,活塞需
(5)使用下列试剂可代替乙醇来促进
 晶体析出的有
晶体析出的有a.
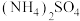 b.稀氨水 c.
b.稀氨水 c. d.
d. 溶液
溶液(6)晶体采用冷风吹干而不用加热烘干的原因是
Ⅲ.废液回收
减压过滤后的废液中含有
 、乙醇和氨水,向废液中加入硫酸,回收乙醇并获得
、乙醇和氨水,向废液中加入硫酸,回收乙醇并获得 和的混合溶液。
和的混合溶液。(7)
 溶液受热易分解,则回收乙醇的实验方法为
溶液受热易分解,则回收乙醇的实验方法为
您最近一年使用:0次
解题方法
5 . 科学家最近首次发现像大脑一样学习的材料—— 。某小组以接触法制硫酸的废催化剂(主要成分是
。某小组以接触法制硫酸的废催化剂(主要成分是 ,含少量
,含少量 等杂质)为原料制备
等杂质)为原料制备 的流程如下:
的流程如下: 难溶于水,
难溶于水, 易溶于水;
易溶于水;
②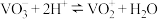
③几种金属离子氢氧化物沉淀的 。
。
请回答下列问题:
(1)“碱浸”中提高反应速率的可行措施有___________ (答出两条)。
(2)有人建议:在“酸浸”和“调 ”之间加入适量双氧水,理由是
”之间加入适量双氧水,理由是___________ 。
(3)理论上,为实现 完全沉淀,应调节
完全沉淀,应调节 ,在工业生产中,常调节
,在工业生产中,常调节 ,其目的是
,其目的是___________ (用化学用语和必要的文字说明)。
(4)“高温还原”中试剂X可能是 ,如果制备等量的
,如果制备等量的 (氧化产物都是
(氧化产物都是 ),则还原剂
),则还原剂 的物质的量之比为
的物质的量之比为___________ 。
(5)“煅烧2”需要在流动空气中煅烧的目的是___________ 。
(6)将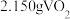 产品溶于强碱溶液,加热煮沸,淍节
产品溶于强碱溶液,加热煮沸,淍节 为8.5,把溶液稀释成
为8.5,把溶液稀释成 溶液,取
溶液,取 稀释后的溶液于锥形瓶中,加入酼酸酸化的KI溶液(过量),溶液中的还原产物为V3+,滴加指示剂,用0.10mol∙L−1Na2S2O3溶液滴定,重复三次,溶液中测得数据如下表所示:
稀释后的溶液于锥形瓶中,加入酼酸酸化的KI溶液(过量),溶液中的还原产物为V3+,滴加指示剂,用0.10mol∙L−1Na2S2O3溶液滴定,重复三次,溶液中测得数据如下表所示:
该产品的纯度为___________ %(保留3位有效数字)。如果加入稀酼酸过多,会使测定结果偏高,其原因是___________ (用离子方程式表示)。
 。某小组以接触法制硫酸的废催化剂(主要成分是
。某小组以接触法制硫酸的废催化剂(主要成分是 ,含少量
,含少量 等杂质)为原料制备
等杂质)为原料制备 的流程如下:
的流程如下:
 难溶于水,
难溶于水, 易溶于水;
易溶于水;②
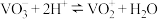
③几种金属离子氢氧化物沉淀的
 。
。| 金属氢氧化物 |  |  |  |
开始沉淀的 | 2.7 | 4.0 | 4.6 |
完全沉淀的 | 3.7 | 5.2 | 6.0 |
(1)“碱浸”中提高反应速率的可行措施有
(2)有人建议:在“酸浸”和“调
 ”之间加入适量双氧水,理由是
”之间加入适量双氧水,理由是(3)理论上,为实现
 完全沉淀,应调节
完全沉淀,应调节 ,在工业生产中,常调节
,在工业生产中,常调节 ,其目的是
,其目的是(4)“高温还原”中试剂X可能是
 ,如果制备等量的
,如果制备等量的 (氧化产物都是
(氧化产物都是 ),则还原剂
),则还原剂 的物质的量之比为
的物质的量之比为(5)“煅烧2”需要在流动空气中煅烧的目的是
(6)将
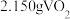 产品溶于强碱溶液,加热煮沸,淍节
产品溶于强碱溶液,加热煮沸,淍节 为8.5,把溶液稀释成
为8.5,把溶液稀释成 溶液,取
溶液,取 稀释后的溶液于锥形瓶中,加入酼酸酸化的KI溶液(过量),溶液中的还原产物为V3+,滴加指示剂,用0.10mol∙L−1Na2S2O3溶液滴定,重复三次,溶液中测得数据如下表所示:
稀释后的溶液于锥形瓶中,加入酼酸酸化的KI溶液(过量),溶液中的还原产物为V3+,滴加指示剂,用0.10mol∙L−1Na2S2O3溶液滴定,重复三次,溶液中测得数据如下表所示:| 序号 | 起始读数 | 终点读数 |
| ① | 0.20 | 21.55 |
| ② | 0.02 | 20.12 |
| ③ | 0.03 | 19.93 |
您最近一年使用:0次
名校
6 . 钪是一种稀土金属元素,在国防、航天、核能等领域具有重要应用。氯化钪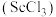 是制备钪的重要原料。工业上利用固体废料“赤泥”(含
是制备钪的重要原料。工业上利用固体废料“赤泥”(含 、
、 、
、 、
、 、
、 等)制取
等)制取 的流程如图。
的流程如图。 难溶于盐酸;②草酸可与多种金属离子形成可溶性络合物。
难溶于盐酸;②草酸可与多种金属离子形成可溶性络合物。
回答下列问题:
(1)酸浸中,滤渣的主要成分是_______ (填化学式), 溶解的离子反应方程式为
溶解的离子反应方程式为_______ 。
(2)“步骤Ⅰ”中加入 后选择合适试剂调pH,再将溶液加热煮沸一段时间,加热煮沸的目的是
后选择合适试剂调pH,再将溶液加热煮沸一段时间,加热煮沸的目的是_______ 。
(3)草酸用量过多时,钪的沉淀率反而下降,原因是_______ 。
(4)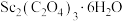 在空气中加热分解时,
在空气中加热分解时, %随温度变化如图所示。
%随温度变化如图所示。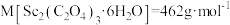 。
。
250℃时固体的主要成分是:_______ (填化学式)。
(5)传统制备 的方法是先得到
的方法是先得到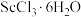 沉淀,再高温脱水得
沉淀,再高温脱水得 ,但通常含有
,但通常含有 杂质,原因是
杂质,原因是_______ 。
(6)“加热氯化”过程主要发生反应的化学方程式为:_______ 。
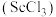 是制备钪的重要原料。工业上利用固体废料“赤泥”(含
是制备钪的重要原料。工业上利用固体废料“赤泥”(含 、
、 、
、 、
、 、
、 等)制取
等)制取 的流程如图。
的流程如图。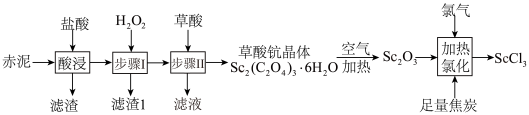
 难溶于盐酸;②草酸可与多种金属离子形成可溶性络合物。
难溶于盐酸;②草酸可与多种金属离子形成可溶性络合物。回答下列问题:
(1)酸浸中,滤渣的主要成分是
 溶解的离子反应方程式为
溶解的离子反应方程式为(2)“步骤Ⅰ”中加入
 后选择合适试剂调pH,再将溶液加热煮沸一段时间,加热煮沸的目的是
后选择合适试剂调pH,再将溶液加热煮沸一段时间,加热煮沸的目的是(3)草酸用量过多时,钪的沉淀率反而下降,原因是
(4)
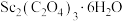 在空气中加热分解时,
在空气中加热分解时, %随温度变化如图所示。
%随温度变化如图所示。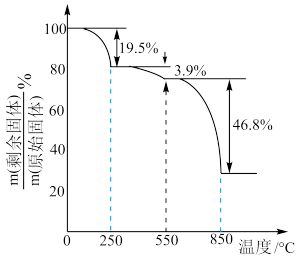
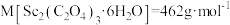 。
。250℃时固体的主要成分是:
(5)传统制备
 的方法是先得到
的方法是先得到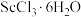 沉淀,再高温脱水得
沉淀,再高温脱水得 ,但通常含有
,但通常含有 杂质,原因是
杂质,原因是(6)“加热氯化”过程主要发生反应的化学方程式为:
您最近一年使用:0次
解题方法
7 . 现有8种元素的性质、数据如下表所列,它们属于第二或第三周期。
回答下列问题:
(1)③的元素符号是_____ ,④的元素名称是_____ 。①在元素周期表中的位置是(周期、族)_____ 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是_____ ;名称是_____ ;碱性最强的化合物的电子式是:_____ ,其含有的化学键的名称为_____ 。
(3)比较④和⑦的氢化物的稳定性(用化学式表示)_____ 。
(4)写出⑦的最高价氧化物对应水化物跟它的氢化物反应的化学方程式:_____ 。
(5)写出②最高价氧化物对应水化物跟⑤的氢化物水溶液反应的离子方程式:_____ 。
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | |
| -2 | -3 | -1 | -3 |
(1)③的元素符号是
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是
(3)比较④和⑦的氢化物的稳定性(用化学式表示)
(4)写出⑦的最高价氧化物对应水化物跟它的氢化物反应的化学方程式:
(5)写出②最高价氧化物对应水化物跟⑤的氢化物水溶液反应的离子方程式:
您最近一年使用:0次
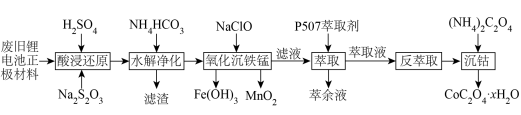
8 . 近年来,废旧锂离子电池的回收成为目前新能源产业重要的发展方向。某锂离子二次电池的正极材料主要为LiCoO2,还含有少量Al、Fe、Mn、Ni的化合物。通过如图所示的流程利用废旧锂离子电池制备草酸钴晶体(CoC2O4·xH2O),回答下列问题:
(1)LiCoO2中Co的化合价为___________ ,“酸浸还原”中LiCoO2转化为(Co2+,氧化产物是SO2,该反应中氧化剂与还原剂的物质的量之比为___________ 。
(2)“水解净化”的滤渣主要成分为___________ (填化学式)。
(3)“氧化沉铁锰”的操作为控制体系的pH在4~5,加入NaClO溶液。其中Mn2+转化为MnO2的离子方程式为___________ ;实际生产中,随着反应时间的延长,锰和铁的沉淀率逐渐增大,但钴的损失量也随之增大,可能的原因是___________ 。
(4)利用“P507萃取剂”从“滤液”中分离Co2+萃取时,Co、Ni的萃取率和Co/Ni分离因素与水相pH的关系如图所示。
(5)“沉钴”时反应的化学方程式为___________ 。
| 离子 | Co2+ | Fe3+ | Fe2+ | Al3+ | Mn2+ | Ni2+ |
| pH | 9.3 | 3.2 | 9.0 | 4.7 | 10.1 | 8.9 |
(1)LiCoO2中Co的化合价为
(2)“水解净化”的滤渣主要成分为
(3)“氧化沉铁锰”的操作为控制体系的pH在4~5,加入NaClO溶液。其中Mn2+转化为MnO2的离子方程式为
(4)利用“P507萃取剂”从“滤液”中分离Co2+萃取时,Co、Ni的萃取率和Co/Ni分离因素与水相pH的关系如图所示。
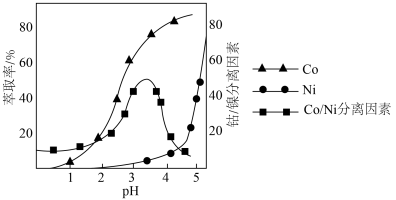
| A.2.5 | B.3.0 | C.3.5 | D.4.0 |
(5)“沉钴”时反应的化学方程式为
您最近一年使用:0次
2024-05-08更新
|
165次组卷
|
3卷引用:2024届内蒙古自治区赤峰市高三下学期三模理科综合试题-高中化学
9 . 实验室需要0.1 mol⋅L NaOH溶液450 mL和0.5 mol⋅L
NaOH溶液450 mL和0.5 mol⋅L 硫酸溶液450 mL。根据这两种溶液的配制情况回答下列问题:
硫酸溶液450 mL。根据这两种溶液的配制情况回答下列问题:
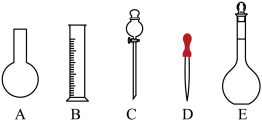
(1)如图所示的仪器中配制溶液肯定不需要的是___________ (填字母)。仪器C的名称是___________ ,本实验所需玻璃仪器E的规格和名称是___________ 。___________ (填“大于”“等于”或“小于”,下同)0.1 mol⋅L 。若NaOH溶液未冷却即转移至容量瓶定容,则所配制溶液浓度
。若NaOH溶液未冷却即转移至容量瓶定容,则所配制溶液浓度___________ 0.1 mol⋅L 。
。
(3)根据计算得知,所需质量分数为98%、密度为1.84 g⋅cm 的浓硫酸的体积为
的浓硫酸的体积为___________ mL(计算结果保留一位小数)。如果实验室有10 mL、25 mL、50 mL量筒,应选用___________ mL规格的量筒最好。
(4)如果定容时不小心超过刻度线,应如何操作:___________ 。
 NaOH溶液450 mL和0.5 mol⋅L
NaOH溶液450 mL和0.5 mol⋅L 硫酸溶液450 mL。根据这两种溶液的配制情况回答下列问题:
硫酸溶液450 mL。根据这两种溶液的配制情况回答下列问题:(1)如图所示的仪器中配制溶液肯定不需要的是
 。若NaOH溶液未冷却即转移至容量瓶定容,则所配制溶液浓度
。若NaOH溶液未冷却即转移至容量瓶定容,则所配制溶液浓度 。
。(3)根据计算得知,所需质量分数为98%、密度为1.84 g⋅cm
 的浓硫酸的体积为
的浓硫酸的体积为(4)如果定容时不小心超过刻度线,应如何操作:
您最近一年使用:0次
10 . 肼是一种火箭燃料。某小组在实验室用NaClO溶液和NH3反应制备肼(N2H4),并进行相关性质探究实验。相关物质的性质如下:
I.实验室制备N2H4_____________ 。
(2)仪器a的作用是____________ 。
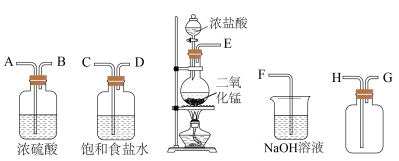
(3)实验室用下列装置制备并收集干净的Cl2,装置的连接顺序是E→__________ →F(用字母表示)。___________ 。
Ⅱ.测定产品中水合腓(N2H4·H2O)的含量
(5)称取产品6.0g,加入通量NaHCO3固体(调节溶液的pH在6.5左右),加水配成250mL溶液,移取25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用0.3000mol/L的碘标准溶液滴定(已知: )。
)。
①滴定到达终点的现象是___________ 。
②重复上述滴定实验2~3次,测得消耗碘标准溶液体积的平均值为20.00mL,产品中水合肼的质量分数为__________ 。
Ⅲ.探究肼的化学性质
(6)取三颈烧瓶中溶液,加入适量稀硫酸,振荡,置于冰水浴中冷却,容器底部有无色晶体析出。过滤后用__________ 洗涤,检验洗涤是否完成的操作为____________ 。
物质 | 性状 | 熔点/℃ | 沸点/℃ | 性质 |
N2H4 | 无色液体 | 1.4 | 113 | 与水混溶,有强还原性 |
N2H6SO4 | 无色晶体 | 254 | - | 不溶于75%的乙醇溶液 |
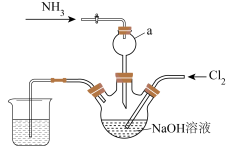
(2)仪器a的作用是
(3)实验室用下列装置制备并收集干净的Cl2,装置的连接顺序是E→
Ⅱ.测定产品中水合腓(N2H4·H2O)的含量
(5)称取产品6.0g,加入通量NaHCO3固体(调节溶液的pH在6.5左右),加水配成250mL溶液,移取25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用0.3000mol/L的碘标准溶液滴定(已知:
 )。
)。①滴定到达终点的现象是
②重复上述滴定实验2~3次,测得消耗碘标准溶液体积的平均值为20.00mL,产品中水合肼的质量分数为
Ⅲ.探究肼的化学性质
(6)取三颈烧瓶中溶液,加入适量稀硫酸,振荡,置于冰水浴中冷却,容器底部有无色晶体析出。过滤后用
您最近一年使用:0次
2024-04-29更新
|
150次组卷
|
2卷引用:2024届内蒙古锡林郭勒盟高三第三次模拟考试理综试卷-高中化学



