名校
1 . 常温下,二甲基亚砜( )为无色无臭且能与水混溶的透明液体,熔点为18.4℃,沸点为189℃。实验室模拟“
)为无色无臭且能与水混溶的透明液体,熔点为18.4℃,沸点为189℃。实验室模拟“ 氧化法”制备二甲基亚砜的装置如图所示(加热装置及夹持装置已省略)。
氧化法”制备二甲基亚砜的装置如图所示(加热装置及夹持装置已省略)。

①制备二甲基亚砜的反应原理为
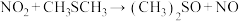 。
。②二甲基硫醚和二甲基亚砜的密度分别为
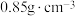 和
和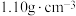 。
。③
 微热易分解为NO、
微热易分解为NO、 和
和 。
。实验过程:将仪器A中制得的气体通入15.00mL二甲基硫醚中,控制温度为60∼80℃,反应一段时间得到二甲基亚砜粗品,粗品经减压蒸馏后共收集到11.10mL二甲基亚砜纯品。回答下列问题:
(1)通入
 的目的是
的目的是a.碱石灰 b.
 c.硅胶
c.硅胶(2)冷凝管进出水的方向
(3)二甲基亚砜能与水混溶的原因可能为
(4)NaOH溶液吸收尾气中NO和
 生成亚硝酸盐的化学方程式为
生成亚硝酸盐的化学方程式为(5)本实验的产率是
您最近一年使用:0次
7日内更新
|
194次组卷
|
6卷引用:2024届浙江省舟山中学高三下学期模拟预测化学试题
解题方法
2 . 钛酸钡( )具有高介电常数和低介电损耗,是压电陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。一种超细微
)具有高介电常数和低介电损耗,是压电陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。一种超细微 粉末的制备方法如下。
粉末的制备方法如下。 的电离方程式为
的电离方程式为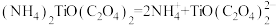 请回答:
请回答:
(1)下列说法正确的是___________。
(2)用溶液2提取的一种副产物可作肥料,该物质是___________ (写电子式);得到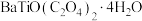 沉淀后需要洗涤,请写出实验操作以检验洗涤是否完全
沉淀后需要洗涤,请写出实验操作以检验洗涤是否完全___________ 。
(3)请写出煅烧过程发生反应的化学方程式___________ 。
(4)如何设计实验方案检验气体A经干燥处理后的剩余气体成分________ 。
 )具有高介电常数和低介电损耗,是压电陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。一种超细微
)具有高介电常数和低介电损耗,是压电陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。一种超细微 粉末的制备方法如下。
粉末的制备方法如下。
 的电离方程式为
的电离方程式为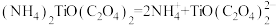 请回答:
请回答:(1)下列说法正确的是___________。
| A.压电陶瓷属于新型无机非金属材料,能实现机械能与电能的相互转化 |
B.溶液1中加入 溶液的离子方程式为 溶液的离子方程式为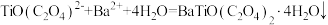 |
| C.实验室中煅烧用到的主要仪器有酒精喷灯、三脚架、泥三角和蒸发皿 |
| D.流程中的三步反应均为非氧化还原反应 |
(2)用溶液2提取的一种副产物可作肥料,该物质是
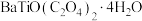 沉淀后需要洗涤,请写出实验操作以检验洗涤是否完全
沉淀后需要洗涤,请写出实验操作以检验洗涤是否完全(3)请写出煅烧过程发生反应的化学方程式
(4)如何设计实验方案检验气体A经干燥处理后的剩余气体成分
您最近一年使用:0次
3 . 铵明矾晶体的化学式为 ,以铵明矾为原料可实现如图转化。
,以铵明矾为原料可实现如图转化。 与题中阳离子不形成配合物,固体A为纯净物。
与题中阳离子不形成配合物,固体A为纯净物。
(1)铵明矾晶体“隔绝空气加热”分解产物中含硫化合物有___________ 。
(2)步骤III中生成白色沉淀C反应的化学方程式为___________ 。
(3)合成铵明矾过程中常使用过量的硫酸铵,一个作用是抑制硫酸铝水解,另一个重要作用是___________ 。
(4)设计实验验证固体A含有的金属元素:___________ 。
(5)步骤I中,铵明矾晶体在各温度段内受热“失重计算值”如表所示。(失重计算值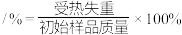 )
)
通过上述数据可判断,在温度区间___________ ℃,铵明矾基本上失去了结晶水。
 ,以铵明矾为原料可实现如图转化。
,以铵明矾为原料可实现如图转化。
 与题中阳离子不形成配合物,固体A为纯净物。
与题中阳离子不形成配合物,固体A为纯净物。(1)铵明矾晶体“隔绝空气加热”分解产物中含硫化合物有
(2)步骤III中生成白色沉淀C反应的化学方程式为
(3)合成铵明矾过程中常使用过量的硫酸铵,一个作用是抑制硫酸铝水解,另一个重要作用是
(4)设计实验验证固体A含有的金属元素:
(5)步骤I中,铵明矾晶体在各温度段内受热“失重计算值”如表所示。(失重计算值
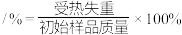 )
)| 温度区间/℃ | 18→190 | 190→430 | 430→505 | 505→900 |
| 失重计算值/% | 39.20 | 7.80 | 13.00 | 26.00 |
您最近一年使用:0次
名校
4 . 锶( )与钙同主族,某固态化合物Y的组成为
)与钙同主族,某固态化合物Y的组成为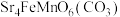 ,以Y为原料可实现如下转化:
,以Y为原料可实现如下转化: 均不能形成配合物。请回答:
均不能形成配合物。请回答:
(1)写出溶液C中的所有阳离子___________ 。
(2)步骤Ⅴ中的反应为 ,说明
,说明 能够较完全转化为
能够较完全转化为 ,的两个原因分别是:①生成
,的两个原因分别是:①生成 降低了体系的能量,促使反应正向进行②
降低了体系的能量,促使反应正向进行②___________ 。
(3)下列说法不正确 的是___________。
(4)固体Y可与 溶液反应,写出该反应的离子方程式
溶液反应,写出该反应的离子方程式___________ 。
(5)设计实验方案检验气体中除 以外的两种主要成分
以外的两种主要成分___________ 。
 )与钙同主族,某固态化合物Y的组成为
)与钙同主族,某固态化合物Y的组成为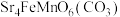 ,以Y为原料可实现如下转化:
,以Y为原料可实现如下转化:
 均不能形成配合物。请回答:
均不能形成配合物。请回答:(1)写出溶液C中的所有阳离子
(2)步骤Ⅴ中的反应为
 ,说明
,说明 能够较完全转化为
能够较完全转化为 ,的两个原因分别是:①生成
,的两个原因分别是:①生成 降低了体系的能量,促使反应正向进行②
降低了体系的能量,促使反应正向进行②(3)下列说法
A.固体B中含有 | B.步骤Ⅱ反应促进了 的水解 的水解 |
C.步骤Ⅲ可推断碱性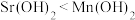 | D.直接加热 无法获得 无法获得 |
(4)固体Y可与
 溶液反应,写出该反应的离子方程式
溶液反应,写出该反应的离子方程式(5)设计实验方案检验气体中除
 以外的两种主要成分
以外的两种主要成分
您最近一年使用:0次
名校
解题方法
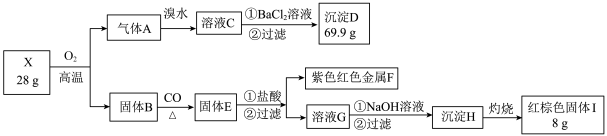
5 . 为探究某矿物X(含三种常见元素)的组成和性质,某兴趣小组设计了如下实验:已知实验中所用试剂均足量,固体B是一种单质和化合物的混合物,请回答如下问题:______ 。
(2)气体A与溴水反应的离子方程式:______ 。
(3)X在高温下与氧气充分反应的化学方程式:______ 。
(4)红棕色固体Ⅰ溶于HI溶液的离子方程式______ 。
(5)检验溶液G中的金属阳离子的实验方案:______ 。
(2)气体A与溴水反应的离子方程式:
(3)X在高温下与氧气充分反应的化学方程式:
(4)红棕色固体Ⅰ溶于HI溶液的离子方程式
(5)检验溶液G中的金属阳离子的实验方案:
您最近一年使用:0次
6 . 硫酸盐(含 )气溶胶是雾霾的主要成分,主要通过
)气溶胶是雾霾的主要成分,主要通过 转化产生。不同
转化产生。不同 条件下
条件下 在水溶液中的主要存在形态及其对应的物质的量分数如图所示:
在水溶液中的主要存在形态及其对应的物质的量分数如图所示: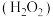 是大气中重要的氧化剂,其有多种途径将
是大气中重要的氧化剂,其有多种途径将 氧化成硫酸盐。
氧化成硫酸盐。
① 可在催化剂
可在催化剂 或
或 的作用下产生
的作用下产生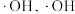 能将
能将 氧化。
氧化。 产生的机理如下:
产生的机理如下:
反应Ⅰ: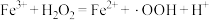 (慢反应);
(慢反应);
反应Ⅱ: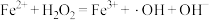 (快反应).
(快反应).
下列说法正确的是________ (填选项字母)。
A.反应涉及非极性键的断裂与形成
B.反应Ⅰ的活化能大于反应Ⅱ
C.向固定容积的反应体系中充入氦气, 氧化
氧化 的反应速率加快
的反应速率加快
D.与 作催化剂相比,相同条件下
作催化剂相比,相同条件下 作催化剂时
作催化剂时 氧化效率可能更高
氧化效率可能更高
②研究表明 与
与 水溶液的反应机理如下:
水溶液的反应机理如下:
Ⅰ.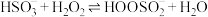 ;
;
Ⅱ.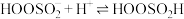 ;
;
Ⅲ.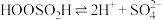 。
。
由此可判断,该条件下的 值为
值为__________ (填“ ”“
”“ ”或“
”或“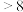 ”);请写出该过程中
”);请写出该过程中 与
与 总反应的离子方程式:
总反应的离子方程式:____________ 。
(2) 与
与 水溶液的反应是硫酸盐产生的另一个重要途径.主要反应如下:
水溶液的反应是硫酸盐产生的另一个重要途径.主要反应如下:
Ⅰ.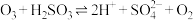 ;
;
Ⅱ. ;
;
Ⅲ.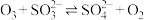 。
。
在含硫微粒总的物质的量为 的
的 水溶液中加入适量
水溶液中加入适量 固体,再通入
固体,再通入 ,反应一段时间后,测得
,反应一段时间后,测得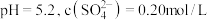 ,则
,则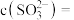
____________ (保留两位有效数字,请写出计算过程)。
(3)科学家最近发现了一种利用水催化促进硫酸盐形成的化学新机制,如图所示: 或
或 可以将电子快速转移到周围的气相
可以将电子快速转移到周围的气相 分子。观察图示可知“水分子桥”主要靠
分子。观察图示可知“水分子桥”主要靠________________ 形成;写出 与
与 间发生的总反应的离子方程式:
间发生的总反应的离子方程式:____________________ 。
②事实上,上述机理只能解释酸雨等现象的形成,却不能解释雾霾中固体硫酸盐小颗粒的存在。进一步研究发现,氨气在雾霾的形成过程中也起到了重要作用,其作用可能是________________ 。
 )气溶胶是雾霾的主要成分,主要通过
)气溶胶是雾霾的主要成分,主要通过 转化产生。不同
转化产生。不同 条件下
条件下 在水溶液中的主要存在形态及其对应的物质的量分数如图所示:
在水溶液中的主要存在形态及其对应的物质的量分数如图所示: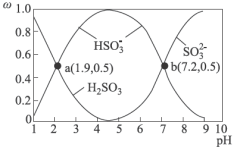
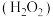 是大气中重要的氧化剂,其有多种途径将
是大气中重要的氧化剂,其有多种途径将 氧化成硫酸盐。
氧化成硫酸盐。①
 可在催化剂
可在催化剂 或
或 的作用下产生
的作用下产生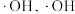 能将
能将 氧化。
氧化。 产生的机理如下:
产生的机理如下:反应Ⅰ:
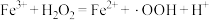 (慢反应);
(慢反应);反应Ⅱ:
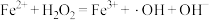 (快反应).
(快反应).下列说法正确的是
A.反应涉及非极性键的断裂与形成
B.反应Ⅰ的活化能大于反应Ⅱ
C.向固定容积的反应体系中充入氦气,
 氧化
氧化 的反应速率加快
的反应速率加快D.与
 作催化剂相比,相同条件下
作催化剂相比,相同条件下 作催化剂时
作催化剂时 氧化效率可能更高
氧化效率可能更高②研究表明
 与
与 水溶液的反应机理如下:
水溶液的反应机理如下:Ⅰ.
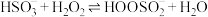 ;
;Ⅱ.
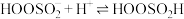 ;
;Ⅲ.
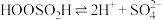 。
。由此可判断,该条件下的
 值为
值为 ”“
”“ ”或“
”或“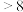 ”);请写出该过程中
”);请写出该过程中 与
与 总反应的离子方程式:
总反应的离子方程式:(2)
 与
与 水溶液的反应是硫酸盐产生的另一个重要途径.主要反应如下:
水溶液的反应是硫酸盐产生的另一个重要途径.主要反应如下:Ⅰ.
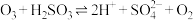 ;
;Ⅱ.
 ;
;Ⅲ.
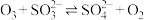 。
。在含硫微粒总的物质的量为
 的
的 水溶液中加入适量
水溶液中加入适量 固体,再通入
固体,再通入 ,反应一段时间后,测得
,反应一段时间后,测得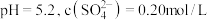 ,则
,则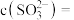
(3)科学家最近发现了一种利用水催化促进硫酸盐形成的化学新机制,如图所示:
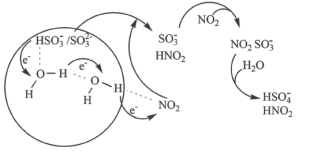
 或
或 可以将电子快速转移到周围的气相
可以将电子快速转移到周围的气相 分子。观察图示可知“水分子桥”主要靠
分子。观察图示可知“水分子桥”主要靠 与
与 间发生的总反应的离子方程式:
间发生的总反应的离子方程式:②事实上,上述机理只能解释酸雨等现象的形成,却不能解释雾霾中固体硫酸盐小颗粒的存在。进一步研究发现,氨气在雾霾的形成过程中也起到了重要作用,其作用可能是
您最近一年使用:0次
2024-05-24更新
|
107次组卷
|
2卷引用:2024届浙江省高三下学期5月份大联考化学试题
解题方法
7 . 以方铅矿(主要含PbS、FeS)和废铅膏(主要含PbO2、PbO)为原料实现如下转化。 的形式浸出。
的形式浸出。
②

请回答:
(1)浸出过程中,发生了多个反应。请写出PbO2、PbS在盐酸和MgCl2溶液的作用下转化为 的离子方程式
的离子方程式___________ ;在浸出时,MgCl2的作用为___________ 。
(2)H2S气体主要是由___________ (填化学式)反应产生的,___________ (填“可以”、“不可以”)用CuSO4溶液吸收。
(3)下列说法正确的是___________。
(4)设计实验,验证结晶后过滤得到的滤液中含有Fe元素___________ 。
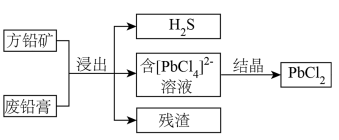
 的形式浸出。
的形式浸出。②

请回答:
(1)浸出过程中,发生了多个反应。请写出PbO2、PbS在盐酸和MgCl2溶液的作用下转化为
 的离子方程式
的离子方程式(2)H2S气体主要是由
(3)下列说法正确的是___________。
A.浸出产生的 最终氧化为 最终氧化为 存在于溶液中 存在于溶液中 |
B. 的空间构型是正四面体 的空间构型是正四面体 |
C.可以向含 的溶液中加入适量的冷水结晶获得PbCl2 的溶液中加入适量的冷水结晶获得PbCl2 |
| D.工业上主要通过电解熔融PbCl2制金属Pb |
(4)设计实验,验证结晶后过滤得到的滤液中含有Fe元素
您最近一年使用:0次
解题方法
8 . 黄铜矿的主要成份是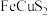 ,以
,以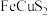 为原料实现如下转化:
为原料实现如下转化:
(1)写出溶液A中的所有阳离子___________ , 的作用
的作用___________ 。
(2)下列说法正确的是___________。
(3) 等锰(Ⅱ)的化合物可制备
等锰(Ⅱ)的化合物可制备 。
。 隔绝空气受热分解生成
隔绝空气受热分解生成 ,产物中无单质,写出该反应的化学方程式
,产物中无单质,写出该反应的化学方程式___________ 。请设计实验方案验证气体产物___________ 。
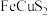 ,以
,以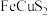 为原料实现如下转化:
为原料实现如下转化: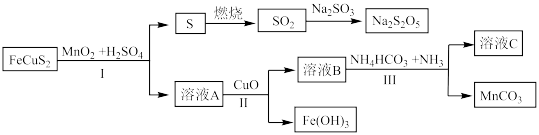
(1)写出溶液A中的所有阳离子
 的作用
的作用(2)下列说法正确的是___________。
| A.S单质存在于火山口或地壳的岩层中 |
B.溶液C含有 |
C. 的水溶液显碱性 的水溶液显碱性 |
D.依据转化关系可知: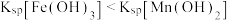 |
(3)
 等锰(Ⅱ)的化合物可制备
等锰(Ⅱ)的化合物可制备 。
。 隔绝空气受热分解生成
隔绝空气受热分解生成 ,产物中无单质,写出该反应的化学方程式
,产物中无单质,写出该反应的化学方程式
您最近一年使用:0次
解题方法
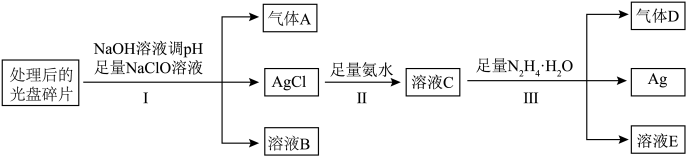
9 . 光盘金属层含有Ag(其它金属微量忽略不计),可以进行资源回收利用,下图为从光盘中提取Ag的工业流程:
②配离子的形成是分步进行的: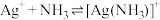
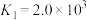 。
。
③AgCl的 ,
,
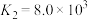 。
。
请回答:
(1)已知Ag位于周期表的第五周期IB族,Ag的原子序数为___________ ;气体A的化学式为___________ ,写出溶液C中所有的阳离子___________ 。
(2)反应Ⅲ的离子方程式为___________ 。
(3)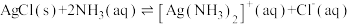 是一个可逆反应。
是一个可逆反应。
①结合相关数据说明上述反应是可逆反应___________ ;
②设计实验验证上述反应是可逆反应___________ 。
②配离子的形成是分步进行的:
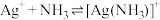
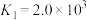 。
。③AgCl的
 ,
,
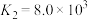 。
。请回答:
(1)已知Ag位于周期表的第五周期IB族,Ag的原子序数为
(2)反应Ⅲ的离子方程式为
(3)
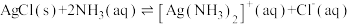 是一个可逆反应。
是一个可逆反应。①结合相关数据说明上述反应是可逆反应
②设计实验验证上述反应是可逆反应
您最近一年使用:0次
解题方法
10 .  固体发生如下转化。
固体发生如下转化。
(1) 固体中所含的化学键为
固体中所含的化学键为_______ ,写出加“过量氯水”后的溶液中的所有阴离子_______ 。
(2)下列说法不正确的是_______。
(3)请依据非氧化还原反应,设计实验验证“固体混合物”中含硫元素的微粒__________ 。
(4)写出 与足量炭黑反应的化学方程式
与足量炭黑反应的化学方程式_______ 。
 固体发生如下转化。
固体发生如下转化。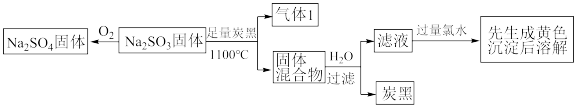
(1)
 固体中所含的化学键为
固体中所含的化学键为(2)下列说法不正确的是_______。
A. 的键角比 的键角比 的键角大 的键角大 |
B.只用稀硝酸不能验证 是否全部氧化为 是否全部氧化为 |
| C.气体1可用作高温炼铁的原料气 |
| D.过滤时,滤纸要对折两次后打开成圆锥形,放入漏斗且紧贴内壁 |
(3)请依据非氧化还原反应,设计实验验证“固体混合物”中含硫元素的微粒
(4)写出
 与足量炭黑反应的化学方程式
与足量炭黑反应的化学方程式
您最近一年使用:0次



