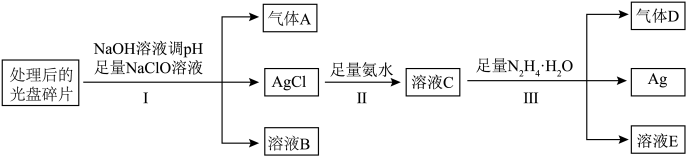
光盘金属层含有Ag(其它金属微量忽略不计),可以进行资源回收利用,下图为从光盘中提取Ag的工业流程:
②配离子的形成是分步进行的: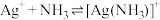
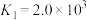 。
。
③AgCl的 ,
,
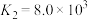 。
。
请回答:
(1)已知Ag位于周期表的第五周期IB族,Ag的原子序数为___________ ;气体A的化学式为___________ ,写出溶液C中所有的阳离子___________ 。
(2)反应Ⅲ的离子方程式为___________ 。
(3)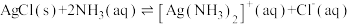 是一个可逆反应。
是一个可逆反应。
①结合相关数据说明上述反应是可逆反应___________ ;
②设计实验验证上述反应是可逆反应___________ 。
②配离子的形成是分步进行的:
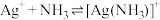
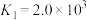 。
。③AgCl的
 ,
,
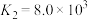 。
。请回答:
(1)已知Ag位于周期表的第五周期IB族,Ag的原子序数为
(2)反应Ⅲ的离子方程式为
(3)
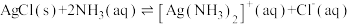 是一个可逆反应。
是一个可逆反应。①结合相关数据说明上述反应是可逆反应
②设计实验验证上述反应是可逆反应
更新时间:2024-05-20 16:24:30
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
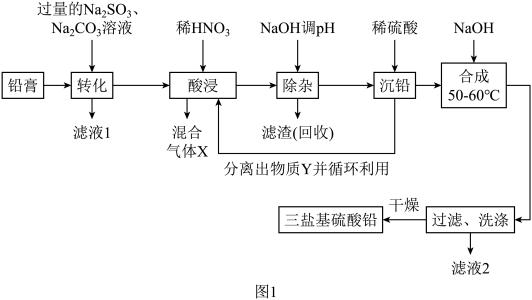
【推荐1】现以铅蓄电池的填充物铅膏(主要含PbSO4、PbO2、PbO和少量FeO)为原料,可生产三盐基硫酸铅(PbSO4·3PbO·H2O)和副产品Fe2O3·xH2O,其工艺流程如下: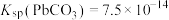 ,
,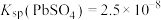 ,
,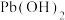 具有两性,PbO2有强氧化性。
具有两性,PbO2有强氧化性。
(1)铅和碳同主族,与Cs同周期,则铅的外围电子轨道表示式为__________ 。
(2)“转化”后的难溶物质为PbCO3和少量PbSO4,则PbO2转化为PbCO3的离子方程式为__________ ,滤液1中 和
和 的浓度之比为
的浓度之比为__________ 。
(3)在50~60℃“合成”三盐基硫酸铅的化学方程式为__________ 。“合成”需控制溶液的pH不能大于10的原因为__________ 。
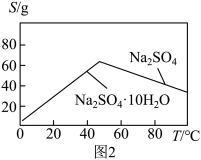
(4)根据图2所示的溶解度随温度的变化曲线,由“滤液1”和“滤液2”获得Na2SO4晶体的操作为将“滤液”调节pH为7,然后蒸发浓缩、__________ ,洗涤后干燥 作抗震添加剂,但皮肤长期接触对身体有害。
作抗震添加剂,但皮肤长期接触对身体有害。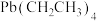 是一种难电离且易溶于有机溶剂的配合物,其晶体类型属于
是一种难电离且易溶于有机溶剂的配合物,其晶体类型属于__________ 晶体。已知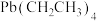 晶体的堆积方式如图3,则其在xy平面上的二维堆积中的配位数是
晶体的堆积方式如图3,则其在xy平面上的二维堆积中的配位数是__________ 。
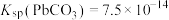 ,
,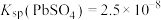 ,
,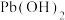 具有两性,PbO2有强氧化性。
具有两性,PbO2有强氧化性。(1)铅和碳同主族,与Cs同周期,则铅的外围电子轨道表示式为
(2)“转化”后的难溶物质为PbCO3和少量PbSO4,则PbO2转化为PbCO3的离子方程式为
 和
和 的浓度之比为
的浓度之比为(3)在50~60℃“合成”三盐基硫酸铅的化学方程式为
(4)根据图2所示的溶解度随温度的变化曲线,由“滤液1”和“滤液2”获得Na2SO4晶体的操作为将“滤液”调节pH为7,然后蒸发浓缩、
 作抗震添加剂,但皮肤长期接触对身体有害。
作抗震添加剂,但皮肤长期接触对身体有害。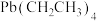 是一种难电离且易溶于有机溶剂的配合物,其晶体类型属于
是一种难电离且易溶于有机溶剂的配合物,其晶体类型属于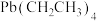 晶体的堆积方式如图3,则其在xy平面上的二维堆积中的配位数是
晶体的堆积方式如图3,则其在xy平面上的二维堆积中的配位数是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】 是一种黑色固体,难溶于水、稀硫酸,可用于锰盐的制备,也用作氧化剂、催化剂等。某学习小组设计实验将粗
是一种黑色固体,难溶于水、稀硫酸,可用于锰盐的制备,也用作氧化剂、催化剂等。某学习小组设计实验将粗 样品(含有较多的
样品(含有较多的 和
和 )转化为纯
)转化为纯 ,其流程如图所示:
,其流程如图所示:
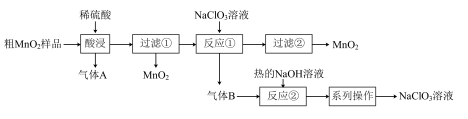
回答下列问题:
(1)“酸浸”中生成气体A的离子方程式为___________ 。
(2)反应①的离子方程式为___________ 。
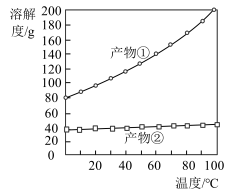
(3)若要得到较浓的 溶液,根据反应②产物的溶解度曲线(如图所示),产物②为
溶液,根据反应②产物的溶解度曲线(如图所示),产物②为___________ (写化学式),“系列操作”为先___________ ,后___________ 。
(4)若粗 样品的质量为
样品的质量为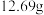 ,经“过滤①”得到
,经“过滤①”得到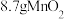 ,并收集到
,并收集到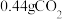 ,则在“反应①”中至少需要
,则在“反应①”中至少需要 的物质的量为
的物质的量为___________  。
。
(5)该流程中可循环利用的物质有___________ 。
 是一种黑色固体,难溶于水、稀硫酸,可用于锰盐的制备,也用作氧化剂、催化剂等。某学习小组设计实验将粗
是一种黑色固体,难溶于水、稀硫酸,可用于锰盐的制备,也用作氧化剂、催化剂等。某学习小组设计实验将粗 样品(含有较多的
样品(含有较多的 和
和 )转化为纯
)转化为纯 ,其流程如图所示:
,其流程如图所示:
回答下列问题:
(1)“酸浸”中生成气体A的离子方程式为
(2)反应①的离子方程式为
(3)若要得到较浓的
 溶液,根据反应②产物的溶解度曲线(如图所示),产物②为
溶液,根据反应②产物的溶解度曲线(如图所示),产物②为
(4)若粗
 样品的质量为
样品的质量为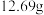 ,经“过滤①”得到
,经“过滤①”得到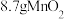 ,并收集到
,并收集到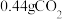 ,则在“反应①”中至少需要
,则在“反应①”中至少需要 的物质的量为
的物质的量为 。
。(5)该流程中可循环利用的物质有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】已知固体A受热易分解,实验流程和结果如下:
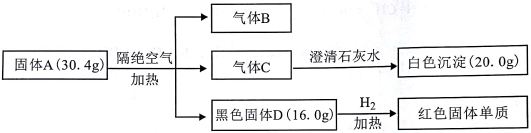
B和C为常见气体且所含元素相同。气体C在标准状况下密度为1.96g·L-1。请回答:
(1)白色沉淀的化学式____________ 。
(2)写出A受热分解的化学方程式___________________________ 。
(3)取少量固体D溶于稀硫酸,加入适量的KI溶液,反应后溶液显棕黄色,同时产生一种白色的碘化物沉淀。写出产生该现象的离子方程式________________________________ 。

B和C为常见气体且所含元素相同。气体C在标准状况下密度为1.96g·L-1。请回答:
(1)白色沉淀的化学式
(2)写出A受热分解的化学方程式
(3)取少量固体D溶于稀硫酸,加入适量的KI溶液,反应后溶液显棕黄色,同时产生一种白色的碘化物沉淀。写出产生该现象的离子方程式
您最近一年使用:0次
【推荐1】二氧化碳捕集与封存是应对气候变化问题的解决方案之一、回答下列问题:
(1)我国科研团队利用低温等离子体协同催化技术,在常温常压下实现了将CO2和CH4一步转化为化工产品。已知甲烷和乙酸的燃烧热分别为-890.31kJ/mol、-876.72kJ/mol。试写出CO2与CH4合成乙酸的热化学方程式:______
(2)在某一总压强为35kPa的刚性密闭容器中CH4、CO2的分压分别为p(CH4)=15kPa、p(CO2)=20kPa,加入Ni/α-Al2O3催化剂并加热至1123K使其发生反应:CH4(g)+CO2(g) 2CO(g)+2H2(g)。
2CO(g)+2H2(g)。
①研究表明CO的生成速率v(CO)=1.28×10-2·p(CH4)·p(CO2)(kPa·s-1)某时刻测得p(H2)=10kPa,则p(CH4)=______ kPa,v(CO)=______ kPa·s-1
②达到平衡后测得体系压强是起始时的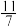 ,则该反应的平衡常数数值Kp=
,则该反应的平衡常数数值Kp=______ (Kp为分压代替浓度表示的平衡常数)
(3)氮化镓(GaN)与Cu可组成如图所示的人工光合系统,该装置能以CO2和H2O为原料合成CH4。
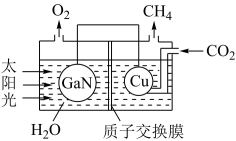
①装置工作时H+移向______ (填“GaN”或“Cu”)电极,该电极上的电极反应式为______
②本实验条件下,若CO2转化为烃(如甲烷、乙烯等)的转化率为10%,生成CH4的选择性为12%,现收集到12molCH4,则通入的CO2为______ mol。(已知:选择性=生成目标产物消耗的原料量/原料总的转化量)
(1)我国科研团队利用低温等离子体协同催化技术,在常温常压下实现了将CO2和CH4一步转化为化工产品。已知甲烷和乙酸的燃烧热分别为-890.31kJ/mol、-876.72kJ/mol。试写出CO2与CH4合成乙酸的热化学方程式:
(2)在某一总压强为35kPa的刚性密闭容器中CH4、CO2的分压分别为p(CH4)=15kPa、p(CO2)=20kPa,加入Ni/α-Al2O3催化剂并加热至1123K使其发生反应:CH4(g)+CO2(g)
 2CO(g)+2H2(g)。
2CO(g)+2H2(g)。①研究表明CO的生成速率v(CO)=1.28×10-2·p(CH4)·p(CO2)(kPa·s-1)某时刻测得p(H2)=10kPa,则p(CH4)=
②达到平衡后测得体系压强是起始时的
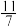 ,则该反应的平衡常数数值Kp=
,则该反应的平衡常数数值Kp=(3)氮化镓(GaN)与Cu可组成如图所示的人工光合系统,该装置能以CO2和H2O为原料合成CH4。

①装置工作时H+移向
②本实验条件下,若CO2转化为烃(如甲烷、乙烯等)的转化率为10%,生成CH4的选择性为12%,现收集到12molCH4,则通入的CO2为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】化学反应速率和限度与生产、生活密切相关。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
①由上表数据可知,反应速率最大的时间段为___________ min(填“0~1”、“1~2”、“2~3”、“3~4”或“4~5”),此段速率快的原因是___________ .
②4~5min时间段以盐酸的浓度变化来表示的该反应速率为___________ (设溶液体积不变)。
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中加入等体积的下列溶液以减慢反应速率,你认为可行的是___________ (填字母)。
A. NaCl溶液 B. KNO3溶液C. CH3COONa溶液 D.CuSO4溶液
(3)在4L的密闭容器中有3种气体进行反应,X、Y、Z的物质的量随时间变化的曲线如图所示,反应在t1min时达到化学平衡状态。
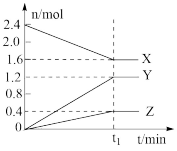
①该反应的化学方程式是___________ 。
②0~t1min内,X的转化率为___________ 。
③该反应达到平衡状态的标志是___________ (填字母)。
A.Y的体积分数在混合气体中保持不变
B.X、Y的反应速率比为2∶3
C.容器内气体压强保持不变
D.容器内气体的总质量保持不变
E.生成3molY的同时消耗2molX
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 氢气体积/mL(标准状况) | 60 | 200 | 424 | 536 | 592 |
②4~5min时间段以盐酸的浓度变化来表示的该反应速率为
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中加入等体积的下列溶液以减慢反应速率,你认为可行的是
A. NaCl溶液 B. KNO3溶液C. CH3COONa溶液 D.CuSO4溶液
(3)在4L的密闭容器中有3种气体进行反应,X、Y、Z的物质的量随时间变化的曲线如图所示,反应在t1min时达到化学平衡状态。

①该反应的化学方程式是
②0~t1min内,X的转化率为
③该反应达到平衡状态的标志是
A.Y的体积分数在混合气体中保持不变
B.X、Y的反应速率比为2∶3
C.容器内气体压强保持不变
D.容器内气体的总质量保持不变
E.生成3molY的同时消耗2molX
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】甲醇是一种重要的化工原料,具有开发和应用的广阔前景。工业上使用水煤气(CO与H2的混合气体)转化成甲醇,反应为 。往一容积为2L的密闭容器内,充入0.3molCO与0.4molH2发生反应。CO的平衡转化率与温度、压强的关系如图所示。
。往一容积为2L的密闭容器内,充入0.3molCO与0.4molH2发生反应。CO的平衡转化率与温度、压强的关系如图所示。

(1)p1、p2的大小关系是p1___________ p2(填“>”“<”或“=”)
(2) A、B、C三点的平衡常数KA、KB、KC由大到小关系是________ 。
(3)列叙述能说明上述反应能达到化学平衡状态的是___________(填字母)。
(4)上述投料在T2℃、p2压强下,平衡时H2的体积分数是___________ ;平衡后再加入1.0molCO后重新到达平衡,则CO的转化率___________ (填“增大”“不变”或“减小”)
(5)在T2℃、p2压强时,若p 2压强恒定为p,则平衡常数Kp=___________ (Kp用气体平衡分压代替气体平衡浓度,分压=总压×气体的物质的量分数,整理出含p的最简表达式)。
 。往一容积为2L的密闭容器内,充入0.3molCO与0.4molH2发生反应。CO的平衡转化率与温度、压强的关系如图所示。
。往一容积为2L的密闭容器内,充入0.3molCO与0.4molH2发生反应。CO的平衡转化率与温度、压强的关系如图所示。
(1)p1、p2的大小关系是p1
(2) A、B、C三点的平衡常数KA、KB、KC由大到小关系是
(3)列叙述能说明上述反应能达到化学平衡状态的是___________(填字母)。
| A.v正(H2)=v逆(CH3OH) |
| B.CH3OH的体积分数不再改变 |
| C.混合气体的平均摩尔质量不再改变 |
| D.同一时间内,消耗0.04molH2,生成0.02molCO |
(4)上述投料在T2℃、p2压强下,平衡时H2的体积分数是
(5)在T2℃、p2压强时,若p 2压强恒定为p,则平衡常数Kp=
您最近一年使用:0次
【推荐1】配位化合物广泛应用于日常生活、工业生产及科研中。例如Ni2+与丁二酮肟生成鲜红色的丁二酮肟镍沉淀,该反应可用于检验Ni2+。
(1)丁二酮肟镍是否属于螯合物___________ (填“是”或“否”),其配位数为___________ ,含有化学键的类型有___________ 。
a.氢键 b.配位键 c.极性键 d.非极性键
(2)绝大部分过渡金属都能与CO分子形成稳定的羰基配合物,金属羰基配合物中每个CO提供一对电子与金属原子形成配位键,且配位键的形成可使金属价层电子满足18电子规律,即中心原子的价电子数+配体提供的总电子数=18,则Fe(CO)x中Fe的配位数x的数值为___________ 。
(3)Cr3+配位能力很强,极易形成配位数为6的八面体结构,例如CrCl3∙6H2O就有3种水合异构体,其中一种结构取1mol与足量的AgNO3溶液反应,生成2mol白色沉淀,则该配合物的化学式为___________ 。
(4)[Ni(NH3)4]2+具有对称的空间构型,[Ni(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,中心离子Ni2+的杂化方式可能为___________ 。
a.sp3 b.dsp2 c.sp2 d.sp
(5)物质在外磁场的作用下会发生磁化现象,在磁场中物质的磁性可分为顺磁性、反磁性和铁磁性,中心离子或原子上含有未成对电子的物质具有顺磁性,下列配离子中具有顺磁性的是___________。
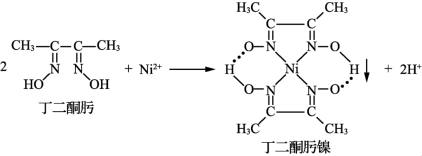
(1)丁二酮肟镍是否属于螯合物
a.氢键 b.配位键 c.极性键 d.非极性键
(2)绝大部分过渡金属都能与CO分子形成稳定的羰基配合物,金属羰基配合物中每个CO提供一对电子与金属原子形成配位键,且配位键的形成可使金属价层电子满足18电子规律,即中心原子的价电子数+配体提供的总电子数=18,则Fe(CO)x中Fe的配位数x的数值为
(3)Cr3+配位能力很强,极易形成配位数为6的八面体结构,例如CrCl3∙6H2O就有3种水合异构体,其中一种结构取1mol与足量的AgNO3溶液反应,生成2mol白色沉淀,则该配合物的化学式为
(4)[Ni(NH3)4]2+具有对称的空间构型,[Ni(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,中心离子Ni2+的杂化方式可能为
a.sp3 b.dsp2 c.sp2 d.sp
(5)物质在外磁场的作用下会发生磁化现象,在磁场中物质的磁性可分为顺磁性、反磁性和铁磁性,中心离子或原子上含有未成对电子的物质具有顺磁性,下列配离子中具有顺磁性的是___________。
| A.[Cr(OH)4]- | B.[Cu(CN)4]3− | C.[ZnCl4]2− | D.[Fe(CN)6]4− |
您最近一年使用:0次
【推荐2】铬是人体必需的微量元素,其在肌体的糖代谢和脂代谢中发挥着特殊作用,铬缺乏会造成葡萄糖耐量受损,可能伴随高血糖、尿糖等。而在工业中铬及其化合物在无机合成和有机合成中均有着重要作用。
Ⅰ.工业上以铬铁矿 为原料生产铬酸钠
为原料生产铬酸钠 ,实际操作是将铬铁矿和纯碱置于坩埚中,在空气中加热,得到
,实际操作是将铬铁矿和纯碱置于坩埚中,在空气中加热,得到 。
。
Ⅱ.市售的 为深绿色晶体,实验室中可用甲醇在酸性条件下还原
为深绿色晶体,实验室中可用甲醇在酸性条件下还原 制备
制备 (装置如图A所示):
(装置如图A所示):
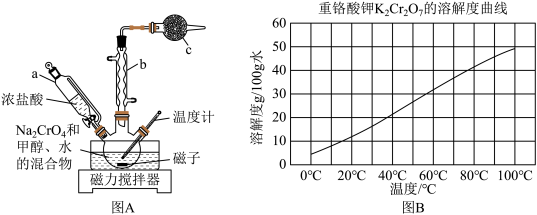
①将一定量铬酸钠、甲醇与水的混合物加入三颈烧瓶中;②升温至120℃时,缓慢滴加足量浓盐酸,保持100℃反应3h;③冷却,用NaOH溶液调节pH为6.5~7.5,得到 沉淀;④洗净
沉淀;④洗净 沉淀后,加入过量盐酸溶解,通过结晶法得到
沉淀后,加入过量盐酸溶解,通过结晶法得到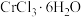 晶体。
晶体。
已知: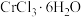 易溶于水、乙醇,易水解。
易溶于水、乙醇,易水解。
Ⅲ.重铬酸钾 俗称红矾,是一种重要的化工产品,可向
俗称红矾,是一种重要的化工产品,可向 溶液中加酸,使
溶液中加酸,使 转化为
转化为 ,再向
,再向 溶液中加入KCl,升高温度,经过一系列操作后可获得
溶液中加入KCl,升高温度,经过一系列操作后可获得 晶体。已知
晶体。已知 的溶解度随温度变化的曲线如图B所示。
的溶解度随温度变化的曲线如图B所示。
回答下列问题:
(1)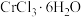 是配位化合物,由于内界配体不同而有不同的颜色,呈深绿色的晶体为
是配位化合物,由于内界配体不同而有不同的颜色,呈深绿色的晶体为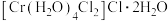 ,该配合物的配体为
,该配合物的配体为___________ 、___________ (填化学式)。
(2)在Ⅱ中制备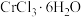 晶体时,步骤④中“加入过量盐酸”的目的是
晶体时,步骤④中“加入过量盐酸”的目的是___________ 。
(3)装置图A中,仪器c的名称为___________ ,仪器b的作用是___________ 。
(4)已知步骤Ⅱ中有 产生,则三颈烧瓶中甲醇还原铬酸钠的离子方程式为
产生,则三颈烧瓶中甲醇还原铬酸钠的离子方程式为___________ 。
(5)往 溶液中加入KCl,升高温度能获得
溶液中加入KCl,升高温度能获得 。获得晶体的一系列操作包括:趁热过滤、
。获得晶体的一系列操作包括:趁热过滤、___________ 、过滤、洗涤、干燥。其中“洗涤”步骤选用的洗涤剂为丙酮,其原因是___________ 。
Ⅰ.工业上以铬铁矿
 为原料生产铬酸钠
为原料生产铬酸钠 ,实际操作是将铬铁矿和纯碱置于坩埚中,在空气中加热,得到
,实际操作是将铬铁矿和纯碱置于坩埚中,在空气中加热,得到 。
。Ⅱ.市售的
 为深绿色晶体,实验室中可用甲醇在酸性条件下还原
为深绿色晶体,实验室中可用甲醇在酸性条件下还原 制备
制备 (装置如图A所示):
(装置如图A所示):
①将一定量铬酸钠、甲醇与水的混合物加入三颈烧瓶中;②升温至120℃时,缓慢滴加足量浓盐酸,保持100℃反应3h;③冷却,用NaOH溶液调节pH为6.5~7.5,得到
 沉淀;④洗净
沉淀;④洗净 沉淀后,加入过量盐酸溶解,通过结晶法得到
沉淀后,加入过量盐酸溶解,通过结晶法得到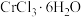 晶体。
晶体。已知:
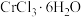 易溶于水、乙醇,易水解。
易溶于水、乙醇,易水解。Ⅲ.重铬酸钾
 俗称红矾,是一种重要的化工产品,可向
俗称红矾,是一种重要的化工产品,可向 溶液中加酸,使
溶液中加酸,使 转化为
转化为 ,再向
,再向 溶液中加入KCl,升高温度,经过一系列操作后可获得
溶液中加入KCl,升高温度,经过一系列操作后可获得 晶体。已知
晶体。已知 的溶解度随温度变化的曲线如图B所示。
的溶解度随温度变化的曲线如图B所示。回答下列问题:
(1)
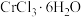 是配位化合物,由于内界配体不同而有不同的颜色,呈深绿色的晶体为
是配位化合物,由于内界配体不同而有不同的颜色,呈深绿色的晶体为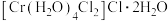 ,该配合物的配体为
,该配合物的配体为(2)在Ⅱ中制备
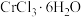 晶体时,步骤④中“加入过量盐酸”的目的是
晶体时,步骤④中“加入过量盐酸”的目的是(3)装置图A中,仪器c的名称为
(4)已知步骤Ⅱ中有
 产生,则三颈烧瓶中甲醇还原铬酸钠的离子方程式为
产生,则三颈烧瓶中甲醇还原铬酸钠的离子方程式为(5)往
 溶液中加入KCl,升高温度能获得
溶液中加入KCl,升高温度能获得 。获得晶体的一系列操作包括:趁热过滤、
。获得晶体的一系列操作包括:趁热过滤、
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】铁、铜的单质及它们的化合物与我们的生产、生活紧密相关。
(1)Cu 处于周期表中______ 区,其最高能层的符号为______ ,基态铜原子的价电子排布式为________ 。
(2)向硫酸铜溶液中逐滴滴加氨水,首先形成蓝色沉淀,继续滴加氨水。沉淀溶解,得到深蓝色透明溶液,向深蓝色溶液中加入乙醇,析出深蓝色晶体。
①写出沉淀溶解,得到深蓝色透明溶液的离子方程式:________ 。
②为什么加入乙醇,能够析出深蓝色晶体?________________
③为什么NH3 常在配合物中作配体,而NH4+却不能作配体?_______ 。
(3)Fe3+可以与SCN-、CN-、H2NCONH2(尿素)等多种配体形成很多的配合物。
①请写出一种与SCN-互为等电子体的分子:________ 。
②CN-的电子式为________ 。
③H2NCONH2(尿素)中N、C 原子的杂化方式分别为_______ 、_______ ,组成尿素的4种元素的第一电离能由大到小的顺序为__________ 。
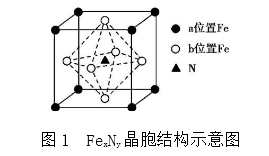
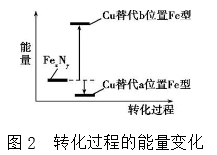
(4)某FeN,的晶胞如图1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x-n)CunNy。FexNy 转化为两种Cu替代型产物的能量变化如图2所示,其中更稳定的Cu替代型产物的化学式为________ 。
(1)Cu 处于周期表中
(2)向硫酸铜溶液中逐滴滴加氨水,首先形成蓝色沉淀,继续滴加氨水。沉淀溶解,得到深蓝色透明溶液,向深蓝色溶液中加入乙醇,析出深蓝色晶体。
①写出沉淀溶解,得到深蓝色透明溶液的离子方程式:
②为什么加入乙醇,能够析出深蓝色晶体?
③为什么NH3 常在配合物中作配体,而NH4+却不能作配体?
(3)Fe3+可以与SCN-、CN-、H2NCONH2(尿素)等多种配体形成很多的配合物。
①请写出一种与SCN-互为等电子体的分子:
②CN-的电子式为
③H2NCONH2(尿素)中N、C 原子的杂化方式分别为
(4)某FeN,的晶胞如图1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x-n)CunNy。FexNy 转化为两种Cu替代型产物的能量变化如图2所示,其中更稳定的Cu替代型产物的化学式为


您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】亚硝酸钠(NaNO2)易溶于水,微溶于乙醇,可作为肉类食品的护色剂,并可以防止肉毒杆菌在肉类食品中生长,保持肉制品的结构和营养价值;但是过量摄入会导致中毒。某化学兴趣小组对亚硝酸钠进行多角度探究:
I.亚硝酸钠的制备

(1)实验中用恒压滴液漏斗,相比普通分液漏斗,其显著优点是________ 。
(2)D中澄清石灰水变浑浊,则C中制备NaNO2的离子方程式为_______ 。
II.探究亚硝酸钠与硫酸反应生成的气体产物
已知:①NO+NO2+2OH-=2NO +H2O ②气体液化的温度:NO2:21℃,NO:-152℃
+H2O ②气体液化的温度:NO2:21℃,NO:-152℃
(3)反应前应打开弹簧夹,先通入一段时间氮气,其目的是______ 。
(4)为了检验装置A中生成的气体产物,装置的连接顺序(从左→右连接):A、C、______ 、_______ 、______ 。
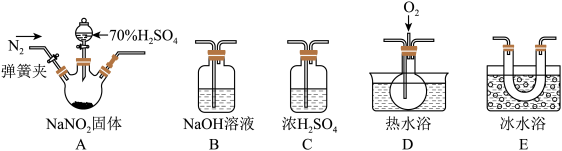
(5)关闭弹簧夹,打开分液漏斗活塞,滴入70%硫酸后,A中产生红棕色气体。
①确认A中产生的气体含有NO,依据的现象是_______ 。
②装置E的作用是________ 。
③通过上述实验探究过程,可得出装置A中反应的化学方程式为_______ 。
III.设计实验证明酸性条件下NaNO2具有氧化性
(6)供选用的试剂:NaNO2溶液、KMnO4溶液、FeSO4溶液、KI溶液、稀硫酸、淀粉溶液、KSCN溶液。根据提供的试剂,设计酸性条件下NaNO2具有氧化性的实验方案:_____ 。
I.亚硝酸钠的制备

(1)实验中用恒压滴液漏斗,相比普通分液漏斗,其显著优点是
(2)D中澄清石灰水变浑浊,则C中制备NaNO2的离子方程式为
II.探究亚硝酸钠与硫酸反应生成的气体产物
已知:①NO+NO2+2OH-=2NO
 +H2O ②气体液化的温度:NO2:21℃,NO:-152℃
+H2O ②气体液化的温度:NO2:21℃,NO:-152℃(3)反应前应打开弹簧夹,先通入一段时间氮气,其目的是
(4)为了检验装置A中生成的气体产物,装置的连接顺序(从左→右连接):A、C、

(5)关闭弹簧夹,打开分液漏斗活塞,滴入70%硫酸后,A中产生红棕色气体。
①确认A中产生的气体含有NO,依据的现象是
②装置E的作用是
③通过上述实验探究过程,可得出装置A中反应的化学方程式为
III.设计实验证明酸性条件下NaNO2具有氧化性
(6)供选用的试剂:NaNO2溶液、KMnO4溶液、FeSO4溶液、KI溶液、稀硫酸、淀粉溶液、KSCN溶液。根据提供的试剂,设计酸性条件下NaNO2具有氧化性的实验方案:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】制备纯净的液态无水四氯化锡的反应为Sn+2Cl2 SnCl4, Sn也可以与HCl反应生成SnCl2(SnCl4易挥发形成气体,极易发生水解,水解生成SnO2·xH20)。已知:
SnCl4, Sn也可以与HCl反应生成SnCl2(SnCl4易挥发形成气体,极易发生水解,水解生成SnO2·xH20)。已知:
制备装置如图所示:

回答下列问题:
(1)Sn在元素周期表中的位置为____________________________ 。
(2)Ⅱ、Ⅲ中的试剂分别为_______ 、__________ ;Ⅶ的作用是____________________ 、_____________ 。
(3)实验所得SnCl4因溶解了Cl2而略显黄色,提纯SnCl4的方法是____________ (填序号)。
a.用NaOH溶液洗涤再蒸馏 b.升华 c.重结晶 d.蒸馏 e.过滤
(4)写出I中反应的化学方程式:_____________________________________ 。
(5)加热Sn粒之前要先让氯气充满整套装置,其目的是_________________ 。
(6)写出SnCl4水解的化学方程式:________________________________________ 。
 SnCl4, Sn也可以与HCl反应生成SnCl2(SnCl4易挥发形成气体,极易发生水解,水解生成SnO2·xH20)。已知:
SnCl4, Sn也可以与HCl反应生成SnCl2(SnCl4易挥发形成气体,极易发生水解,水解生成SnO2·xH20)。已知:| 物质 | 摩尔质量(g/mol) | 熔点(℃) | 沸点(℃) |
| Sn | 119 | 231 | 2260 |
| SnCl2 | 190 | 246 | 623 |
| SnCl4 | 261 | -30 | 114 |

回答下列问题:
(1)Sn在元素周期表中的位置为
(2)Ⅱ、Ⅲ中的试剂分别为
(3)实验所得SnCl4因溶解了Cl2而略显黄色,提纯SnCl4的方法是
a.用NaOH溶液洗涤再蒸馏 b.升华 c.重结晶 d.蒸馏 e.过滤
(4)写出I中反应的化学方程式:
(5)加热Sn粒之前要先让氯气充满整套装置,其目的是
(6)写出SnCl4水解的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】硫酸铵一种优良的氮肥,适用于各种土壤和作物,硫酸铵还可用于纺织、皮革、医药等方面。某化工厂以硫酸钙为原料制备硫酸铵,其工艺流程如图:
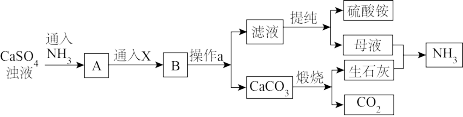
(1)X为_______ (填化学式),操作a名称为_______ 。
(2)NH3是工业制硝酸的重要原料,写出氨的催化氧化反应的化学方程式_______ 。
(3)煅烧CaCO3生成生石灰和CO2的反应为_______ 反应(填“吸热”或“放热”),欲加快该反应速率可采取的措施为_______ (写出一种即可)。
(4)上述流程中,可以循环使用的物质有_______ (填化学式)。
(5)从滤液中获得(NH4)2SO4晶体,必要的操作步骤是蒸发浓缩、_______ 、过滤等。

(1)X为
(2)NH3是工业制硝酸的重要原料,写出氨的催化氧化反应的化学方程式
(3)煅烧CaCO3生成生石灰和CO2的反应为
(4)上述流程中,可以循环使用的物质有
(5)从滤液中获得(NH4)2SO4晶体,必要的操作步骤是蒸发浓缩、
您最近一年使用:0次



