 固体发生如下转化。
固体发生如下转化。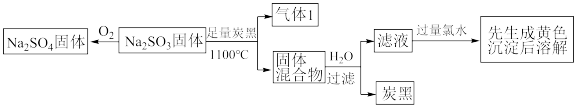
(1)
 固体中所含的化学键为
固体中所含的化学键为(2)下列说法不正确的是_______。
A. 的键角比 的键角比 的键角大 的键角大 |
B.只用稀硝酸不能验证 是否全部氧化为 是否全部氧化为 |
| C.气体1可用作高温炼铁的原料气 |
| D.过滤时,滤纸要对折两次后打开成圆锥形,放入漏斗且紧贴内壁 |
(3)请依据非氧化还原反应,设计实验验证“固体混合物”中含硫元素的微粒
(4)写出
 与足量炭黑反应的化学方程式
与足量炭黑反应的化学方程式
更新时间:2024-05-18 18:17:05
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某校课外活动小组为了验证铜与稀硝酸反应产生的是 气体,设计了如图实验。
气体,设计了如图实验。
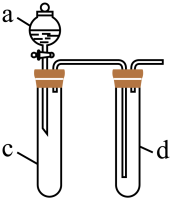
(1)仪器a的名称为_________ ;实验开始前,应进行的操作是_________ 。
(2)在d中加适量 溶液,c中放一小块铜片,由a向c中加入
溶液,c中放一小块铜片,由a向c中加入 稀硝酸,c中发生反应的化学方程式是
稀硝酸,c中发生反应的化学方程式是_________ 。
(3)制取硝酸铜的三种方案如表,最佳方案是方案__________________ 。
(4)硝酸工业产生的工业烟气中含有大量的氮氧化物,需要处理后才能排放。一种利用活性炭吸附脱硝的工艺如图。
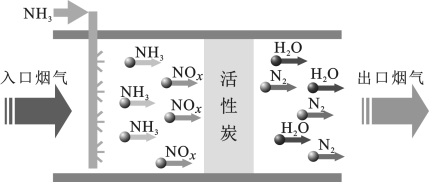
①该流程中活性炭的作用是_________ ,若入口烟气中 以
以 的形式参加反应,则相应的化学方程式为
的形式参加反应,则相应的化学方程式为_________ 。
②某同学选择如图装置(省略夹持仪器)对该方法进行模拟实验:
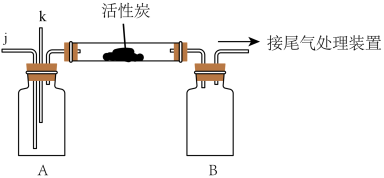
 和
和 从j和k通入A中。其中j通入的气体为
从j和k通入A中。其中j通入的气体为_________ (填化学式),解释其原因:_________ 。
 气体,设计了如图实验。
气体,设计了如图实验。
(1)仪器a的名称为
(2)在d中加适量
 溶液,c中放一小块铜片,由a向c中加入
溶液,c中放一小块铜片,由a向c中加入 稀硝酸,c中发生反应的化学方程式是
稀硝酸,c中发生反应的化学方程式是(3)制取硝酸铜的三种方案如表,最佳方案是方案
方案 | 反应物 |
甲 |
|
乙 |
|
丙 |
|

①该流程中活性炭的作用是
 以
以 的形式参加反应,则相应的化学方程式为
的形式参加反应,则相应的化学方程式为②某同学选择如图装置(省略夹持仪器)对该方法进行模拟实验:

 和
和 从j和k通入A中。其中j通入的气体为
从j和k通入A中。其中j通入的气体为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】亚氯酸钠是一种高效氧化剂、漂白剂,主要用于纸浆漂白、水处理等;工业上生产NaClO2有多种方法,某工业生产的流程如图所示:

请回答下列问题:
(1)电解槽中阳极上的电极反应式为___________ 。
(2)反应器Ⅰ中发生反应的化学方程式为___________ 。反应器Ⅱ中发生的反应中氧化剂与还原剂物质的量之比为___________ 。

请回答下列问题:
(1)电解槽中阳极上的电极反应式为
(2)反应器Ⅰ中发生反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】工业上以铬铁矿(FeO·Cr2O3,含Al2O3、SiO2等杂质)为主要原料制备红矾钠的工艺流程以及可溶性组分物质的量浓度c与pH的关系分别如图a、b。当c≦1.0×10-5mol·L-1时,可认为已除尽。回答下列问题:


(1)焙烧时将矿料磨碎且气体与矿料逆流而行,其目的是___________ 。
(2)焙烧的目的是将FeO·Cr2O3转化为Na2CrO4并将Al、Si氧化物转化为可溶性钠盐,写出焙烧时FeO·Cr2O3发生的化学方程式___________ 。
(3)中和时pH的理论范围为___________ ;酸化的目的是___________ 。
(4)副产品主要是___________ 。
(5)此方法生产过程中会产生大量含 的酸性废水,可以用如图c装置处理。向废水中加入适量的NaCl进行电解,
的酸性废水,可以用如图c装置处理。向废水中加入适量的NaCl进行电解, 被还原为Cr3+然后生成Cr(OH)3沉淀除去,废水则可以达到排放标准。已知Ksp(Cr(OH)3)=1.0×10-32;写出阳极的电极方程式:
被还原为Cr3+然后生成Cr(OH)3沉淀除去,废水则可以达到排放标准。已知Ksp(Cr(OH)3)=1.0×10-32;写出阳极的电极方程式:___________ ;若电解一段时间后,调节pH测得溶液中c(Fe3+)=1.0×10-12mol·L-1,则此时c(Cr3+)=___________ mol·L-1。


(1)焙烧时将矿料磨碎且气体与矿料逆流而行,其目的是
(2)焙烧的目的是将FeO·Cr2O3转化为Na2CrO4并将Al、Si氧化物转化为可溶性钠盐,写出焙烧时FeO·Cr2O3发生的化学方程式
(3)中和时pH的理论范围为
(4)副产品主要是
(5)此方法生产过程中会产生大量含
 的酸性废水,可以用如图c装置处理。向废水中加入适量的NaCl进行电解,
的酸性废水,可以用如图c装置处理。向废水中加入适量的NaCl进行电解, 被还原为Cr3+然后生成Cr(OH)3沉淀除去,废水则可以达到排放标准。已知Ksp(Cr(OH)3)=1.0×10-32;写出阳极的电极方程式:
被还原为Cr3+然后生成Cr(OH)3沉淀除去,废水则可以达到排放标准。已知Ksp(Cr(OH)3)=1.0×10-32;写出阳极的电极方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】寒冬袭来,病毒肆虐,含氯消毒剂在控制病原微生物污染和传播等方面有着重要作用。某校课外化学小组设计如图所示装置制备少量氯气并进行系列实验(夹持仪器已略)。
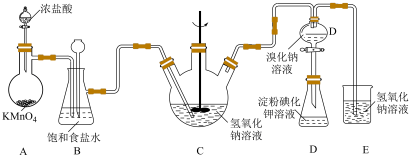
已知淀粉溶液遇碘单质变蓝;卤素单质在水中的颜色如表所示:
(1)请写出实验室用 与浓盐酸制氯气的化学方程式
与浓盐酸制氯气的化学方程式___________ ;
(2)装置B的作用是___________ ;
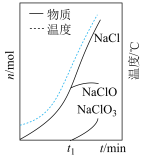
(3)装置C中生成各物质的物质的量和溶液的温度随时间的变化如下图所示。写出 分钟后氧化产物只有
分钟后氧化产物只有 的反应,对应的化学方程式
的反应,对应的化学方程式___________ ;
(4)设计装置D、E的目的是验证氧化性 。当向D中缓缓通入一定量氯气时,可以看到D中无色溶液逐渐变为
。当向D中缓缓通入一定量氯气时,可以看到D中无色溶液逐渐变为___________ 色,若打开装置D的活塞,使D中溶液滴入装置E,可以观察到的现象是___________ ,经认真考虑,有同学提出该实验方案仍有不足,你若同意该建议,请说明其中不足的原因是___________ ;(若不同意,则该空不用写)
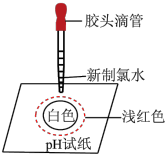
(5)某同学在pH试纸上滴几滴新制的氯水,现象如图所示,下列有关该实验的说法中正确的是___________。

已知淀粉溶液遇碘单质变蓝;卤素单质在水中的颜色如表所示:
| 卤素单质 |  |  |  |
| 水溶液颜色 | 黄绿色 | 橙黄色 | 棕黄色 |
(1)请写出实验室用
 与浓盐酸制氯气的化学方程式
与浓盐酸制氯气的化学方程式(2)装置B的作用是
(3)装置C中生成各物质的物质的量和溶液的温度随时间的变化如下图所示。写出
 分钟后氧化产物只有
分钟后氧化产物只有 的反应,对应的化学方程式
的反应,对应的化学方程式
(4)设计装置D、E的目的是验证氧化性
 。当向D中缓缓通入一定量氯气时,可以看到D中无色溶液逐渐变为
。当向D中缓缓通入一定量氯气时,可以看到D中无色溶液逐渐变为(5)某同学在pH试纸上滴几滴新制的氯水,现象如图所示,下列有关该实验的说法中正确的是___________。

A.该实验说明 分子具有漂白性 分子具有漂白性 |
B.该实验说明 扩散速率比HClO分子快 扩散速率比HClO分子快 |
| C.将实验后变白的pH试纸再滴入盐酸又会变红 |
| D.若用久置的氯水进行实验,现象相同 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.X、Y、Z是中学化学常见的三种物质,它们之间的相互转化关系如下(X、Y、Z为英文字母,部分反应条件及产物略去)
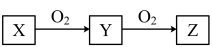
(1)若Y是一种易溶于水,且能使品红溶液褪色的无色刺激性气味的气体。
①则Y和新制氯水主要成分反应生成两种强酸的化学方程式___________ 。
②Y气体的大量排放会形成酸雨,在工业上可以用足量氨水吸收,化学方程式为___________ 。
(2)若Z是红棕色气体。试写出Z与水反应制备另一种强酸的化学方程式___________ 。
Ⅱ.根据所学有机化合物知识填空。
(3)下列各组物质:(填序号)
① 和
和 ②
② 和
和 ③金刚石和石墨
③金刚石和石墨
④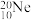 和
和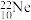 ⑤
⑤ 和丁烷 ⑥
和丁烷 ⑥ 和
和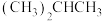
互为同分异构体的是___________ ,互为同系物的是___________ ,互为同位素的是___________ ,
互为同素异形体的是___________ ,是同一物质的是___________ 。
(4)某1mol烷烃完全燃烧需要消耗5mol氧气,写出该烷烃一氯代物的结构简式___________ 。

(1)若Y是一种易溶于水,且能使品红溶液褪色的无色刺激性气味的气体。
①则Y和新制氯水主要成分反应生成两种强酸的化学方程式
②Y气体的大量排放会形成酸雨,在工业上可以用足量氨水吸收,化学方程式为
(2)若Z是红棕色气体。试写出Z与水反应制备另一种强酸的化学方程式
Ⅱ.根据所学有机化合物知识填空。
(3)下列各组物质:(填序号)
①
 和
和 ②
② 和
和 ③金刚石和石墨
③金刚石和石墨④
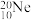 和
和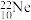 ⑤
⑤ 和丁烷 ⑥
和丁烷 ⑥ 和
和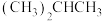
互为同分异构体的是
互为同素异形体的是
(4)某1mol烷烃完全燃烧需要消耗5mol氧气,写出该烷烃一氯代物的结构简式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】氯水的成分及探究
(1)新制氯水呈______ 色,或氯水能使淀粉碘化钾试纸变蓝,都可以说明__________ 存在
(2)氯水的pH值_______ 水,说明氯水呈______ 性
(3)向氯水中滴加紫色石蕊试液产生的现象是_____________ ,可以说明氯水中存在_________ 微粒
(4)在氯水中加入AgNO3溶液,产生的现象____________ 说明存在_________ 微粒
(5)可以用钢瓶来储存液氯,为了防止钢瓶的腐蚀,冲入氯气前必须_________
(6)在氯水中加入无水CuSO4固体,产生的现象_________________ 说明存在__________ 微粒
(1)新制氯水呈
(2)氯水的pH值
(3)向氯水中滴加紫色石蕊试液产生的现象是
(4)在氯水中加入AgNO3溶液,产生的现象
(5)可以用钢瓶来储存液氯,为了防止钢瓶的腐蚀,冲入氯气前必须
(6)在氯水中加入无水CuSO4固体,产生的现象
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】新型钙钛矿太阳能电池是近几年来的研究热点,具备更加清洁、便于应用、制造成本低和效率高等显著优点。回答下列问题:
(1)钾或钾盐的焰色反应为浅紫色(透过蓝色钴玻璃),下列有关原理分析的叙述正确的是_______ (填字母)。
a.电子从基态跃迁到较高的激发态 b.电子从较高的激发态跃迁到基态
c.焰色反应的光谱属于吸收光谱 d.焰色反应的光谱属于发射光谱
(2)基态Ca原子核外有_______ 种运动状态不同的电子,基态Pb原子核外电子排布,最后占据能级的电子云轮廓图形状为_______ 。
(3) 中N原子的杂化方式为
中N原子的杂化方式为_______ 。
(4) 中H—N—H的键角比
中H—N—H的键角比 中H—N—H的键角大的原因是
中H—N—H的键角大的原因是_______ 。
(5)如图所示,其中与 紧邻的
紧邻的 个数为
个数为_______ 。X射线衍射实验测得晶胞参数:密度为a g·cm-3,则晶胞的边长为_______ pm(该物质的相对分子质量为M, 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。

(1)钾或钾盐的焰色反应为浅紫色(透过蓝色钴玻璃),下列有关原理分析的叙述正确的是
a.电子从基态跃迁到较高的激发态 b.电子从较高的激发态跃迁到基态
c.焰色反应的光谱属于吸收光谱 d.焰色反应的光谱属于发射光谱
(2)基态Ca原子核外有
(3)
 中N原子的杂化方式为
中N原子的杂化方式为(4)
 中H—N—H的键角比
中H—N—H的键角比 中H—N—H的键角大的原因是
中H—N—H的键角大的原因是(5)如图所示,其中与
 紧邻的
紧邻的 个数为
个数为 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】铝硅酸盐型分子筛的吸附能力高、选择性强、耐高温。广泛用于有机化工和石油化工。钙铝硅酸盐型分子筛化学纠成可表示为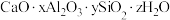 。回答下列问题:
。回答下列问题:
(1) 与
与 同主族,基态
同主族,基态 原子价电子的轨道表示式为
原子价电子的轨道表示式为___________ ,晶体硅和碳化硅熔点较高的是___________ (填化学式)。
(2)O元素能与卤素形成多种氧化物, 分子中
分子中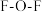 的键角
的键角___________ (填“大于”或“小于”) 分子中
分子中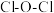 的键角,原因是
的键角,原因是___________ 。
(3)在多原子分子中如有相互平行的p轨道,它们连贯重叠在一起构成一个整体,p电子在多个原子间运动形成 型化学键,这种不局限在两个原子之间的
型化学键,这种不局限在两个原子之间的 键称为离域
键称为离域 键,或大
键,或大 键。下列微粒中不存在离域
键。下列微粒中不存在离域 键的是___________(填序号)
键的是___________(填序号)
(4)金属钙在空气中燃烧除有氧化物生成外,还有氮化物生成,因此在电子工业中常用钙除去体系中不必要的氧气和氮气。钙与氮气化合所得氮化钙的晶胞结构如图所示。该晶体属立方晶系, 的半径为
的半径为 ,晶胞棱边夹角均为90°。
,晶胞棱边夹角均为90°。 与
与 间的作用力为
间的作用力为___________ 。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点原子的分数坐标为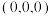 ,则B点原子的分数坐标为
,则B点原子的分数坐标为___________ 。阿伏加德罗常数的值为 ,该晶体的密度
,该晶体的密度___________  (写出表达式)。
(写出表达式)。

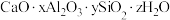 。回答下列问题:
。回答下列问题:(1)
 与
与 同主族,基态
同主族,基态 原子价电子的轨道表示式为
原子价电子的轨道表示式为(2)O元素能与卤素形成多种氧化物,
 分子中
分子中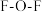 的键角
的键角 分子中
分子中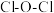 的键角,原因是
的键角,原因是(3)在多原子分子中如有相互平行的p轨道,它们连贯重叠在一起构成一个整体,p电子在多个原子间运动形成
 型化学键,这种不局限在两个原子之间的
型化学键,这种不局限在两个原子之间的 键称为离域
键称为离域 键,或大
键,或大 键。下列微粒中不存在离域
键。下列微粒中不存在离域 键的是___________(填序号)
键的是___________(填序号)A. | B.. (白磷分子) (白磷分子) | C. | D. |
 的半径为
的半径为 ,晶胞棱边夹角均为90°。
,晶胞棱边夹角均为90°。 与
与 间的作用力为
间的作用力为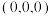 ,则B点原子的分数坐标为
,则B点原子的分数坐标为 ,该晶体的密度
,该晶体的密度 (写出表达式)。
(写出表达式)。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】硅是构成矿物和岩石的主要成分,单质硅及其化合物具有广泛的用途。某些硅酸盐具有筛选分子的功能,一种硅酸盐的组成为:M2O·R2O3·2SiO2·nH2O,已知元素M、R均位于元素周期表的第3周期。两元素原子的质子数之和为24。
(1)该硅酸盐中同周期元素原子半径由大到小的顺序为_______ ;
(2)常温下,不能与R单质发生反应的是_______(选填序号);
(3)写出M、R两种元素的最高价氧化物对应的水化物反应的离子方程式_______ 。
(4)氮化硅(Si3N4)陶瓷材料硬度大、熔点高。Si3N4晶体中只有极性共价键,则氮原子的化合价为_______ 。
(5)C3N4的结构与Si3N4相似。请比较二者熔点高低并说明理由:_______ 。
(6)可由下列反应制得Si3N4,配平该反应并标出电子转移的数目和方向:_______ 。
_______SiO2+_______C+_______N2 _______Si3N4+_______CO
_______Si3N4+_______CO
(7)如果上述反应在10L的密闭容器中进行,一段时间后测得气体密度增加了2.8g/L,则制得的Si3N4质量为_______ 。
(1)该硅酸盐中同周期元素原子半径由大到小的顺序为
(2)常温下,不能与R单质发生反应的是_______(选填序号);
| A.CuCl2溶液 | B.Fe2O3 | C.浓硫酸 | D.Na2CO3溶液 |
(4)氮化硅(Si3N4)陶瓷材料硬度大、熔点高。Si3N4晶体中只有极性共价键,则氮原子的化合价为
(5)C3N4的结构与Si3N4相似。请比较二者熔点高低并说明理由:
(6)可由下列反应制得Si3N4,配平该反应并标出电子转移的数目和方向:
_______SiO2+_______C+_______N2
 _______Si3N4+_______CO
_______Si3N4+_______CO(7)如果上述反应在10L的密闭容器中进行,一段时间后测得气体密度增加了2.8g/L,则制得的Si3N4质量为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】高温乃至室温超导一直是科学家不懈追求目标。科学家合成了一种高温超导材料,其晶胞结构如图所示(B和C原子均位于晶胞面上),该立方晶胞参数为apm。
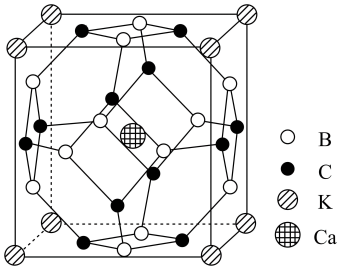
(1)该晶体的四种元素的电负性由大到小的顺序是___________ 。钙元素的焰色实验为砖红色,基于其原理可用于定性与定量分析,这种分析方法称为___________ 光谱。
(2)该晶体中,B原子的杂化轨道类型是_______ ,C原子的杂化轨道类型是________ 。
(3)该晶体中微粒间存在的化学键有_________ 、___________ 。
(4)该晶体的化学式为________ (化成最简整数比),密度为_________  (列出计算式,相对分子质量用M表示无需计算出数值)。
(列出计算式,相对分子质量用M表示无需计算出数值)。
(5)晶胞中B和C原子构成的多面体有_________ 个面
(6)比较 与
与 的沸点并解释原因
的沸点并解释原因_________ ;比较 与
与 的键角并解释原因
的键角并解释原因___________ 。

(1)该晶体的四种元素的电负性由大到小的顺序是
(2)该晶体中,B原子的杂化轨道类型是
(3)该晶体中微粒间存在的化学键有
(4)该晶体的化学式为
 (列出计算式,相对分子质量用M表示无需计算出数值)。
(列出计算式,相对分子质量用M表示无需计算出数值)。(5)晶胞中B和C原子构成的多面体有
(6)比较
 与
与 的沸点并解释原因
的沸点并解释原因 与
与 的键角并解释原因
的键角并解释原因
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】铬及其化合物在材料、颜料及超导等方面用途非常广泛。回答下列问题:
(1)基态Cr原子的价电子排布式为__ ;Cr成为阳离子时首先失去__ 轨道的电子。
(2)铬与钾均位于第四周期,铬的熔点和沸点均比钾的高,这是因为__ 。
(3)甘氨酸铬(结构如图)是一种配合物,其配位原子是__ 。

(4)反应:6KSCN+13K2Cr2O7+55H2SO4=13Cr2(SO4)3+6SO2↑+6CO2↑+16K2SO4+55H2O
①KSCN的四种组成元素中第一电离能最大的是__ (填元素符号);KSCN中阴离子的空间构型为___ 形,中心原子的杂化方式是__ 。
②分子中的大 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大 键可表示为
键可表示为 ),则NO2的大
),则NO2的大 键可表示为
键可表示为__ 。
(5)立方CrO2晶体的结构如图所示,晶胞参数为apm。

①设NA为阿伏加 德罗常数的值,则CrO2的密度为__ (列出计算式)g·cm-3。
②1、2号原子的坐标依次为(0,0,0)、( ,0,
,0, ),则原子坐标为(
),则原子坐标为(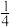 ,
,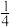 ,
,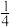 )和(
)和( ,
, ,
, )间的距离为
)间的距离为__ pm。
(1)基态Cr原子的价电子排布式为
(2)铬与钾均位于第四周期,铬的熔点和沸点均比钾的高,这是因为
(3)甘氨酸铬(结构如图)是一种配合物,其配位原子是

(4)反应:6KSCN+13K2Cr2O7+55H2SO4=13Cr2(SO4)3+6SO2↑+6CO2↑+16K2SO4+55H2O
①KSCN的四种组成元素中第一电离能最大的是
②分子中的大
 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大 键可表示为
键可表示为 ),则NO2的大
),则NO2的大 键可表示为
键可表示为(5)立方CrO2晶体的结构如图所示,晶胞参数为apm。

①设NA为阿伏加 德罗常数的值,则CrO2的密度为
②1、2号原子的坐标依次为(0,0,0)、(
 ,0,
,0, ),则原子坐标为(
),则原子坐标为(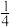 ,
,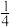 ,
,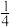 )和(
)和( ,
, ,
, )间的距离为
)间的距离为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知A、B、C、D和E五种分子所含原子的数目依次为1、2、3、4和6,且都含有18个电子,又知B、C和D是由两种元素的原子组成,且D分子中两种原子个数比为1∶1。请回答:
(1)组成A分子的原子的核外电子排布式是___________ ;
(2)B和C的分子式分别是___________ 和___________ ;C分子的空间构型为___________ 形
(3)向D的稀溶液中加入少量氯化铁溶液现象是___________ ,该反应的化学方程式为___________ 。
(1)组成A分子的原子的核外电子排布式是
(2)B和C的分子式分别是
(3)向D的稀溶液中加入少量氯化铁溶液现象是
您最近一年使用:0次

 、浓
、浓


