解题方法
1 . 雷雨天 转化为
转化为 的流程为:
的流程为: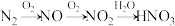
(1) 转化为NO的化学方程式是“
转化为NO的化学方程式是“_____ 。”
(2)NO转化为 的化学方程式是“
的化学方程式是“_____ 。”
(3) 转化为
转化为 的化学方程式是“
的化学方程式是“_____ 。”
 转化为
转化为 的流程为:
的流程为: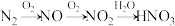
(1)
 转化为NO的化学方程式是“
转化为NO的化学方程式是“(2)NO转化为
 的化学方程式是“
的化学方程式是“(3)
 转化为
转化为 的化学方程式是“
的化学方程式是“
您最近一年使用:0次
解题方法
2 . 锌电解阳极泥(主要成分为 和
和 ,还有少量锰铅氧化物
,还有少量锰铅氧化物 和
和 )是冶锌过程中产生的废渣,一种回收锌电解阳极泥中金属元素锰、铅和银的工艺流程如图所示。回答下列问题:
)是冶锌过程中产生的废渣,一种回收锌电解阳极泥中金属元素锰、铅和银的工艺流程如图所示。回答下列问题: 易溶于水,不溶于乙醇
易溶于水,不溶于乙醇
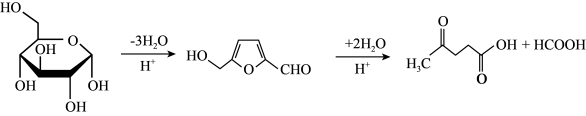
②在较高温度及酸性催化条件下,葡萄糖能发生如图反应: 时
时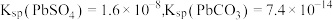
(1)已知 中
中 为
为 价,
价, 为
为 价和
价和 价,该氧化物中
价,该氧化物中 价和
价和 价
价 的物质的量之比为
的物质的量之比为_______ 。
(2)“还原酸浸”过程中主要反应的离子方程式为_______ ,该过程中实际葡萄糖加入量远大于理论需要量,其原因是_______ 。
(3)整个流程中可循环利用的物质是_______ (填名称)。获得 晶体的一系列操作是蒸发结晶、趁热过滤、洗涤、低温干燥,其中“洗涤”的具体操作是
晶体的一系列操作是蒸发结晶、趁热过滤、洗涤、低温干燥,其中“洗涤”的具体操作是_______ 。
(4)书写相关反应的离子方程式,并通过计算说明 时,可用
时,可用 溶液将“滤渣1”中的
溶液将“滤渣1”中的 完全转化为
完全转化为 的原因
的原因_______ 。
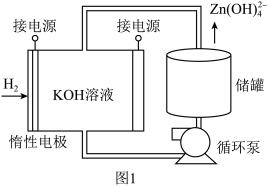
(5)通过氢电极增压法可制得单质锌,装置如图1所示。电解池工作时总反应的离子方程式为_______ 。 和
和 作为敏化剂的太阳能电池,能量转换效率已经超过其他类型太阳能电池。
作为敏化剂的太阳能电池,能量转换效率已经超过其他类型太阳能电池。
① 和
和 中
中 与
与 之间、
之间、 与
与 之间的离子键成分的百分数大小比较及解释
之间的离子键成分的百分数大小比较及解释_______ 。
② 晶胞结构如图2所示,其中
晶胞结构如图2所示,其中 代表
代表 。当
。当 位于晶胞的体心时,
位于晶胞的体心时, 于晶胞的
于晶胞的_______ 位置(填“顶点”“面心”“棱心”或“晶胞内”)。
 和
和 ,还有少量锰铅氧化物
,还有少量锰铅氧化物 和
和 )是冶锌过程中产生的废渣,一种回收锌电解阳极泥中金属元素锰、铅和银的工艺流程如图所示。回答下列问题:
)是冶锌过程中产生的废渣,一种回收锌电解阳极泥中金属元素锰、铅和银的工艺流程如图所示。回答下列问题: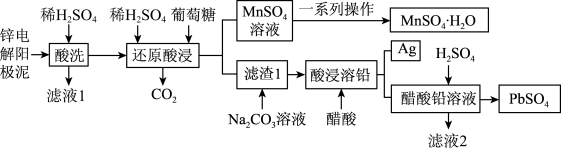
 易溶于水,不溶于乙醇
易溶于水,不溶于乙醇②在较高温度及酸性催化条件下,葡萄糖能发生如图反应:
 时
时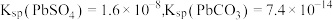
(1)已知
 中
中 为
为 价,
价, 为
为 价和
价和 价,该氧化物中
价,该氧化物中 价和
价和 价
价 的物质的量之比为
的物质的量之比为(2)“还原酸浸”过程中主要反应的离子方程式为
(3)整个流程中可循环利用的物质是
 晶体的一系列操作是蒸发结晶、趁热过滤、洗涤、低温干燥,其中“洗涤”的具体操作是
晶体的一系列操作是蒸发结晶、趁热过滤、洗涤、低温干燥,其中“洗涤”的具体操作是(4)书写相关反应的离子方程式,并通过计算说明
 时,可用
时,可用 溶液将“滤渣1”中的
溶液将“滤渣1”中的 完全转化为
完全转化为 的原因
的原因(5)通过氢电极增压法可制得单质锌,装置如图1所示。电解池工作时总反应的离子方程式为
 和
和 作为敏化剂的太阳能电池,能量转换效率已经超过其他类型太阳能电池。
作为敏化剂的太阳能电池,能量转换效率已经超过其他类型太阳能电池。①
 和
和 中
中 与
与 之间、
之间、 与
与 之间的离子键成分的百分数大小比较及解释
之间的离子键成分的百分数大小比较及解释②
 晶胞结构如图2所示,其中
晶胞结构如图2所示,其中 代表
代表 。当
。当 位于晶胞的体心时,
位于晶胞的体心时, 于晶胞的
于晶胞的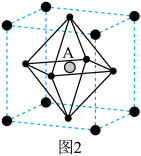
您最近一年使用:0次
3 . 写成电离方程式。
(1) =
=___________ 。
(2)HNO3=___________ 。
(1)
 =
=(2)HNO3=
您最近一年使用:0次
名校
解题方法
4 . 实验小组同学欲探究 的性质并测定空气中
的性质并测定空气中 的体积分数。他们设计了如图所示的实验装置,请你参与探究并回答问题。
的体积分数。他们设计了如图所示的实验装置,请你参与探究并回答问题。_______ 。
(2)装置E的作用是_______ 。(用离子方程式表示)
(3)装置D用于验证 的
的_______ 性,发生的化学方程式为_______ 。
(4)装置C中的现象是_______ ;若将C中的溴水改为酸性高锰酸钾溶液,现象为_______ ,发生的离子方程式为_______ 。
(5)如果用硫酸溶液和 固体反应制取
固体反应制取 装置如图所示。其中a导管的作用是
装置如图所示。其中a导管的作用是_______ 。 含量(假设空气中无其他还原性气体)。
含量(假设空气中无其他还原性气体)。

实验中若通过空气的体积为 (标准状况下),最终所得固体质量为0.466g,通过计算确定该空气中二氧化硫的含量是
(标准状况下),最终所得固体质量为0.466g,通过计算确定该空气中二氧化硫的含量是_______ 。(结果精确到0.001%)
 的性质并测定空气中
的性质并测定空气中 的体积分数。他们设计了如图所示的实验装置,请你参与探究并回答问题。
的体积分数。他们设计了如图所示的实验装置,请你参与探究并回答问题。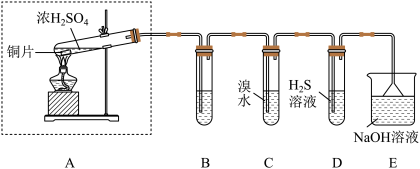
(2)装置E的作用是
(3)装置D用于验证
 的
的(4)装置C中的现象是
(5)如果用硫酸溶液和
 固体反应制取
固体反应制取 装置如图所示。其中a导管的作用是
装置如图所示。其中a导管的作用是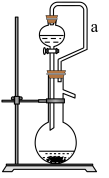
 含量(假设空气中无其他还原性气体)。
含量(假设空气中无其他还原性气体)。
实验中若通过空气的体积为
 (标准状况下),最终所得固体质量为0.466g,通过计算确定该空气中二氧化硫的含量是
(标准状况下),最终所得固体质量为0.466g,通过计算确定该空气中二氧化硫的含量是
您最近一年使用:0次
名校
5 . 依据如图中氮元素及其化合物的转化关系,回答问题:_______ 。
(2)回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为:_______ 。
②下列试剂用于干燥NH3的是_______ (填字母)。
A.浓硫酸 B.碱石灰 C.氯化钙固体
③氨气是重要的化工原料,可用于工业制硝酸,写出氨气催化氧化的化学方程式:_______ 。
(3)回答下列关于NO、NO2的问题:
①汽车尾气中的CO、NOx在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出NO2被CO还原的化学方程式:_______ 。
②用氨可将氮氧化物转化为无毒气体。如 ,该反应中,被氧化的物质是
,该反应中,被氧化的物质是_______ (填化学式),若反应中生成1molN2,则转移电子_______ mol。
(4)工业生产中利用氨水吸收SO2和NO2,原理如图所示:_______ 。
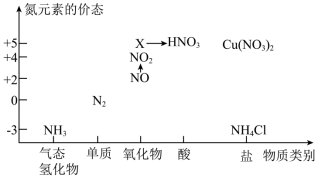
(2)回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为:
②下列试剂用于干燥NH3的是
A.浓硫酸 B.碱石灰 C.氯化钙固体
③氨气是重要的化工原料,可用于工业制硝酸,写出氨气催化氧化的化学方程式:
(3)回答下列关于NO、NO2的问题:
①汽车尾气中的CO、NOx在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出NO2被CO还原的化学方程式:
②用氨可将氮氧化物转化为无毒气体。如
 ,该反应中,被氧化的物质是
,该反应中,被氧化的物质是(4)工业生产中利用氨水吸收SO2和NO2,原理如图所示:
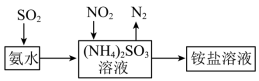
您最近一年使用:0次
6 . 针对表中10种元素及由这些元素形成的单质和化合物,用元素符号或者化学式填写以下空格。
(1)最活泼的金属元素是___________ ,最活泼的非金属元素是___________ ,最不活泼的元素是___________ 。
(2)碱性最强的最高价氧化物对应水化物是___________ ,酸性最强的最高价氧化物对应水化物是___________ ,最稳定的气态氢化物是___________ 。
(3)在④与⑤中,还原性较强的是___________ ,在⑧与⑨的单质中,氧化性较强的是___________ 。
(4)④的最高价氧化物对应的水化物和⑥的最高价氧化物对应的水化物相互反应的化学方程式为:___________ ;用电子式表示④和⑧形成的化合物的形成过程___________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 4 | ⑩ |
(2)碱性最强的最高价氧化物对应水化物是
(3)在④与⑤中,还原性较强的是
(4)④的最高价氧化物对应的水化物和⑥的最高价氧化物对应的水化物相互反应的化学方程式为:
您最近一年使用:0次
7 . a.有下列物质:①氢氧化钡 ②KHSO4 ③液态HCl ④稀硫酸 ⑤二氧化碳 ⑥铜 ⑦碳酸钠 ⑧蔗糖
请回答下列问题:
(1)属于电解质的有___________ (填序号)
(2)属于非电解质的有___________ (填序号)
b.某同学用如下实验探究 、
、 的性质。请回答下列问题:
的性质。请回答下列问题:
(3)在FeCl3溶液中需加入少量铁屑,发生反应的化学方程式为___________ 。FeCl3溶液,加入1滴___________ 溶液,溶液变___________ 。
(4)FeCl2溶液与氯水反应的化学方程式为___________ 。
(5)某同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程___________ 。
c.请回答下列问题:
(6)0.5 mol H2O含有H的物质的量___________ mol。含有O数目___________ 。
(7)100 mL 0.2 mol/L Na2SO4溶液中 的物质的量浓度为
的物质的量浓度为___________ 。
(8)标准状况下11.2 L的CO2的物质的量是___________ mol。
请回答下列问题:
(1)属于电解质的有
(2)属于非电解质的有
b.某同学用如下实验探究
 、
、 的性质。请回答下列问题:
的性质。请回答下列问题:(3)在FeCl3溶液中需加入少量铁屑,发生反应的化学方程式为
(4)FeCl2溶液与氯水反应的化学方程式为
(5)某同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程
c.请回答下列问题:
(6)0.5 mol H2O含有H的物质的量
(7)100 mL 0.2 mol/L Na2SO4溶液中
 的物质的量浓度为
的物质的量浓度为(8)标准状况下11.2 L的CO2的物质的量是
您最近一年使用:0次
解题方法
8 .  为阿伏加德罗常数,下列叙述错误的是
为阿伏加德罗常数,下列叙述错误的是
 为阿伏加德罗常数,下列叙述错误的是
为阿伏加德罗常数,下列叙述错误的是A.18 g H2O中含的质子数为 |
B.12 g金刚石含有 碳原子 碳原子 |
C.46 g NO2和N2O4混合气体中含有原子总数为 |
D.44 g CO2含有的氧原子数约为 |
您最近一年使用:0次
9 . 关于反应 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是| A.CO是氧化产物 | B.C单质被还原 | C.CO2是氧化剂 | D.C单质得电子 |
您最近一年使用:0次
解题方法
10 . 下列各组离子能在溶液中大量共存的是
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近一年使用:0次



