名校
1 . NA是阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下,11.2L氯仿含有氯原子1.5NA | B.31g白磷中共价键数目为3NA |
| C.1 mol重水比1 mol水多NA个质子 | D.12 g金刚石中含有2NA个C-C |
您最近一年使用:0次
2024-04-28更新
|
92次组卷
|
2卷引用: 吉林省梅河口市第五中学2023-2024学年高二下学期第一次月考化学试题
解题方法
2 . 下列化学用语表示正确的是
A.基态铜原子价电子的轨道表示式: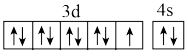 |
B.顺式聚2-甲基-1,3-丁二烯的结构简式: |
C.NaH的形成过程: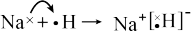 |
D.邻羟基苯甲醛的分子内氢键: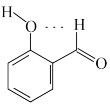 |
您最近一年使用:0次
名校
3 . 下列离子在指定溶液中一定能大量共存的是
A.无色透明的溶液中: 、 、 、 、 、 、 |
B.pH=3的溶液中: 、 、 、 、 、 、 |
C.使酚酞变红的溶液中: 、 、 、 、 、 、 |
D.含有大量 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
2024-04-25更新
|
505次组卷
|
5卷引用:吉林省长春市第五中学2023-2024学年高一下学期第一学程考试化学试题
4 . 为研究反应 (aq)+2I-(aq)=2
(aq)+2I-(aq)=2 (aq)+I2(aq)的反应进程中的能量变化,在
(aq)+I2(aq)的反应进程中的能量变化,在 和I-的混合溶液中加入Fe3+,过程变化如下:
和I-的混合溶液中加入Fe3+,过程变化如下:
第一步:2Fe3+(aq)+2I-(aq)= I2(aq) + 2Fe2+(aq)
第二步:2Fe2+(aq)+ (aq)=2Fe3+(aq)+2
(aq)=2Fe3+(aq)+2 (aq)
(aq)
下列有关该反应的说法正确的是
 (aq)+2I-(aq)=2
(aq)+2I-(aq)=2 (aq)+I2(aq)的反应进程中的能量变化,在
(aq)+I2(aq)的反应进程中的能量变化,在 和I-的混合溶液中加入Fe3+,过程变化如下:
和I-的混合溶液中加入Fe3+,过程变化如下: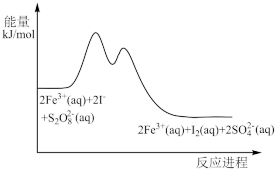
第一步:2Fe3+(aq)+2I-(aq)= I2(aq) + 2Fe2+(aq)
第二步:2Fe2+(aq)+
 (aq)=2Fe3+(aq)+2
(aq)=2Fe3+(aq)+2 (aq)
(aq) 下列有关该反应的说法正确的是
A. (已知其中有1个-O-O-结构)中S元素化合价为+7 (已知其中有1个-O-O-结构)中S元素化合价为+7 |
| B.总反应是吸热反应 |
| C.第一步基元反应是该反应的决速步骤 |
| D.Fe3+改变了总反应的反应历程和焓变 |
您最近一年使用:0次
名校
5 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.25℃时,1LpH=13的Ba(OH)2溶液中OH-的数目为0.2NA |
| B.密闭容器中1.2molN2与3molH2合成氨,平衡后容器内气体分子总数大于2.2NA |
| C.标准状况下,22.4LCl2与水反应,转移电子数为NA |
| D.1L0.1mol/L的NH4Cl溶液中NH4+的数目为0.1NA |
您最近一年使用:0次
名校
解题方法
6 . 常温下,下列各组离子在指定溶液中一定能大量共存的是
A.水电离产生的c(H+)=1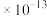 mol/L的溶液中:K+、Fe3+、Cl-、SO mol/L的溶液中:K+、Fe3+、Cl-、SO |
B.使甲基橙试液变红的溶液中:Ca2+、NH 、Cl-、HCO 、Cl-、HCO |
C.在加入铝粉能产生H2的溶液中:Fe2+、Mg2+、NO 、Na+ 、Na+ |
D.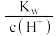 = 0.2mol/L的溶液:Na+、K+、SiO = 0.2mol/L的溶液:Na+、K+、SiO 、NO 、NO |
您最近一年使用:0次
名校
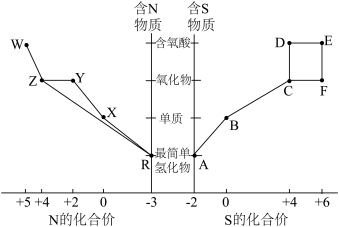
7 . 元素的“价类二维图”体现了化学变化之美。部分含硫、氮物质的类别与硫元素和氮元素化合价的对应关系如下图所示。回答下列问题: 反应的化学方程式
反应的化学方程式______
(2)下列有关图中所示含N、S物质的叙述,正确的是______ (填标号)。
a.在催化剂的作用下,R可将Y、Z还原为X
b.图中所示的物质中,只有W、D、E属于电解质
c.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生
d.Z、C、F均能与NaOH溶液反应,都是酸性氧化物
e.制备焦亚硫酸钠( ),从氧化还原反应的角度分析,可选择B和D反应
),从氧化还原反应的角度分析,可选择B和D反应
(3)写出B与氢氧化钠溶液反应的离子反应方程式______
(4)将物质W的稀溶液加入物质D的溶液中,可生成物质E,该反应的离子方程式是______ 。
(5) (S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入
(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入 的
的 溶液中,可制得该物质:
溶液中,可制得该物质: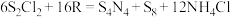 ,上述反应中,物质R体现的性质有
,上述反应中,物质R体现的性质有______ ,该反应每生成 转移电子
转移电子______ mol。
 反应的化学方程式
反应的化学方程式(2)下列有关图中所示含N、S物质的叙述,正确的是
a.在催化剂的作用下,R可将Y、Z还原为X
b.图中所示的物质中,只有W、D、E属于电解质
c.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生
d.Z、C、F均能与NaOH溶液反应,都是酸性氧化物
e.制备焦亚硫酸钠(
 ),从氧化还原反应的角度分析,可选择B和D反应
),从氧化还原反应的角度分析,可选择B和D反应(3)写出B与氢氧化钠溶液反应的离子反应方程式
(4)将物质W的稀溶液加入物质D的溶液中,可生成物质E,该反应的离子方程式是
(5)
 (S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入
(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入 的
的 溶液中,可制得该物质:
溶液中,可制得该物质: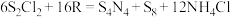 ,上述反应中,物质R体现的性质有
,上述反应中,物质R体现的性质有 转移电子
转移电子
您最近一年使用:0次
名校
解题方法
8 . 十九世纪初,科学家用氰酸银 与
与 在一定条件下反应制得尿素
在一定条件下反应制得尿素 实现了由无机物到有机物的合成。下列有关说法正确的是
实现了由无机物到有机物的合成。下列有关说法正确的是
 与
与 在一定条件下反应制得尿素
在一定条件下反应制得尿素 实现了由无机物到有机物的合成。下列有关说法正确的是
实现了由无机物到有机物的合成。下列有关说法正确的是A. 电子式为 电子式为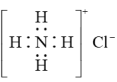 | B.第一电离能: |
| C.氰酸铵与尿素互为同分异构体 | D.尿素中所有原子可能处于同一平面 |
您最近一年使用:0次
2024-04-19更新
|
454次组卷
|
2卷引用:东北三省2023-2024学年高三下学期高考模拟试题(一)
名校
9 . 下列生产生活中的反应不涉及氧化还原反应的是
| A.常温下用铝制容器盛装浓硫酸 | B.ClO2用作自来水消毒剂 |
| C.实验室制备少量氨气 | D.豆科植物根瘤菌固氮 |
您最近一年使用:0次
2024-04-19更新
|
168次组卷
|
2卷引用:吉林省长春市第五中学2023-2024学年高一下学期第一学程考试化学试题
解题方法
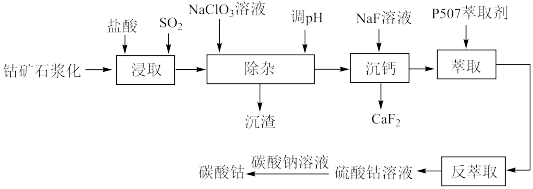
10 . 碳酸钴是一种无机化合物,其化学式为CoCO3。它是一种重要的钴盐,常用于电池、催化剂等领域。工业上以钴矿[主要成分是Co2O3]为原料制取碳酸钴的工艺流程如图: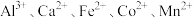 等阳离子
等阳离子
②25℃时,部分阳离子以氢氧化物形式沉淀时溶液的 见表:
见表:
③ 的
的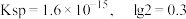
回答下列问题:
(1)Co原子的原子序数为27,其基态原子的价电子排布式为_______ 。
(2)浸取钴矿石前,需要浆化处理,原因是_______ 。
(3)除杂过程中,若加入过量 溶液会产生有毒气体
溶液会产生有毒气体 ,有人提出用压缩空气代替
,有人提出用压缩空气代替 溶液,则通入压缩空气后发生反应的离子方程式为
溶液,则通入压缩空气后发生反应的离子方程式为_______ ,调节 后,若溶液中
后,若溶液中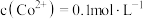 ,此时
,此时 的范围是
的范围是_______ 。
(4)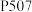 萃取剂
萃取剂 和
和 能发生反应:
能发生反应: 。萃取时,适当增大溶液
。萃取时,适当增大溶液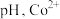 萃取率会增大,其原因是
萃取率会增大,其原因是_______ 。
(5)反萃取时需向萃取液中加入_______ (填写化学式),该工艺中设计萃取、反萃取的目的是_______ 。
(6)一种含 的氧化物晶胞结构如图所示,已知在该氧化物中
的氧化物晶胞结构如图所示,已知在该氧化物中 原子半径为
原子半径为 原子半径为
原子半径为 ,它们在晶体中是紧密接触的。用
,它们在晶体中是紧密接触的。用 表示阿伏加德罗常数的值,则该晶体密度为
表示阿伏加德罗常数的值,则该晶体密度为_______  (列出计算式即可)。
(列出计算式即可)。
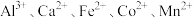 等阳离子
等阳离子②25℃时,部分阳离子以氢氧化物形式沉淀时溶液的
 见表:
见表:| 金属离子 |  |  |  |  |
沉淀完全的 | 8.3 | 2.8 | 4.7 | 9.8 |
 的
的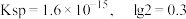
回答下列问题:
(1)Co原子的原子序数为27,其基态原子的价电子排布式为
(2)浸取钴矿石前,需要浆化处理,原因是
(3)除杂过程中,若加入过量
 溶液会产生有毒气体
溶液会产生有毒气体 ,有人提出用压缩空气代替
,有人提出用压缩空气代替 溶液,则通入压缩空气后发生反应的离子方程式为
溶液,则通入压缩空气后发生反应的离子方程式为 后,若溶液中
后,若溶液中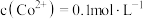 ,此时
,此时 的范围是
的范围是(4)
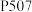 萃取剂
萃取剂 和
和 能发生反应:
能发生反应: 。萃取时,适当增大溶液
。萃取时,适当增大溶液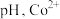 萃取率会增大,其原因是
萃取率会增大,其原因是(5)反萃取时需向萃取液中加入
(6)一种含
 的氧化物晶胞结构如图所示,已知在该氧化物中
的氧化物晶胞结构如图所示,已知在该氧化物中 原子半径为
原子半径为 原子半径为
原子半径为 ,它们在晶体中是紧密接触的。用
,它们在晶体中是紧密接触的。用 表示阿伏加德罗常数的值,则该晶体密度为
表示阿伏加德罗常数的值,则该晶体密度为 (列出计算式即可)。
(列出计算式即可)。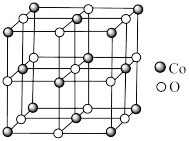
您最近一年使用:0次



