23-24高二上·湖南邵阳·期末
名校
解题方法
1 . 下列说法正确的是
A.基态Cu的核外电子排布式为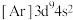 |
B. 中心原子为 中心原子为 杂化,VSEPR模型为四面体形 杂化,VSEPR模型为四面体形 |
C. 和 和 都是正四面体形微粒,其键角都为60° 都是正四面体形微粒,其键角都为60° |
D. 、 、 分子中所有原子的最外层都满足8电子稳定结构 分子中所有原子的最外层都满足8电子稳定结构 |
您最近一年使用:0次
23-24高二上·山东青岛·期末
2 .  可发生水解反应
可发生水解反应 .下列说法错误的是
.下列说法错误的是
 可发生水解反应
可发生水解反应 .下列说法错误的是
.下列说法错误的是A. 、 、 分子中键角较大的是 分子中键角较大的是 | B. 是由极性键构成的极性分子 是由极性键构成的极性分子 |
C.质量数为35的Cl原子可表示为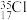 | D.HClO的电子式为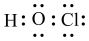 |
您最近一年使用:0次
2024-02-22更新
|
170次组卷
|
3卷引用:2.3.1 共价键的极性(基础)
22-23高二下·上海浦东新·期末
3 . 元素周期表是元素周期律的具体表现形式,是学习和研究化学的重要工具,下图是元素周期表的一部分。

(1)氧元素在周期表中的位置是第_______ 周期_______ 族,氧原子的电子式为_______ 。
(2)某元素的结构示意图为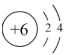 ,请在上图相应位置填入该元素的元素符号
,请在上图相应位置填入该元素的元素符号_______ 。
(3)元素性质呈现周期性变化的根本原因是_______。

(1)氧元素在周期表中的位置是第
(2)某元素的结构示意图为
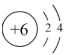 ,请在上图相应位置填入该元素的元素符号
,请在上图相应位置填入该元素的元素符号(3)元素性质呈现周期性变化的根本原因是_______。
| A.元素相对原子质量的递增 |
| B.元素原子半径呈现周期性变化 |
| C.元素原子核外电子排布呈现周期性变化 |
| D.元素金属性和非金属性呈现周期性变化 |
您最近一年使用:0次
23-24高二上·上海静安·期中
4 . 下列关于互为同系物的两种有机物的说法不正确的是
| A.通式一定相同 | B.最简式可能相同 |
| C.一定不互为同分异构体 | D.能发生的反应类型一定相同 |
您最近一年使用:0次
22-23高二上·宁夏石嘴山·期中
名校
5 . 已知H与O可以形成H2O和H2O2两种化合物。请完成下列空白:
(1)H2O内的O—H、水分子间的范德华力和氢键,三种作用从强到弱依次为___________ 。 可与H2O形成
可与H2O形成 ,
, 中O采用
中O采用___________ 杂化。 中
中 键角比CH4中的键角
键角比CH4中的键角___________ (填“大”或“小”),原因为_______ 。
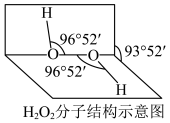
(2) 是常用的氧化剂,其分子结构如图所示,两个氢原子犹如在半展开的书的两面上。
是常用的氧化剂,其分子结构如图所示,两个氢原子犹如在半展开的书的两面上。 的电子式是
的电子式是___________ 。 是
是___________ 分子(填“极性”或“非极性”)。 能与水混溶,却不溶于
能与水混溶,却不溶于 ,请予以解释:
,请予以解释:___________ 。
(1)H2O内的O—H、水分子间的范德华力和氢键,三种作用从强到弱依次为
 可与H2O形成
可与H2O形成 ,
, 中O采用
中O采用 中
中 键角比CH4中的键角
键角比CH4中的键角(2)
 是常用的氧化剂,其分子结构如图所示,两个氢原子犹如在半展开的书的两面上。
是常用的氧化剂,其分子结构如图所示,两个氢原子犹如在半展开的书的两面上。 的电子式是
的电子式是 是
是 能与水混溶,却不溶于
能与水混溶,却不溶于 ,请予以解释:
,请予以解释:
您最近一年使用:0次
6 . 21世纪的新领域纳米技术正日益受到各国科学家的关注,请回答下列问题:
(1)纳米是_______ 单位,1 nm等于_______ m。纳米科学与技术是研究结构尺寸在1~100 nm 范围内材料的性质与应用。它与_______ 分散质的粒子大小一样。
(2)世界上最小的马达,只有千万分之一个蚊子那么大,如图,这种分子马达将来可用于消除体内垃圾。

①该图是马达分子的_______ 。
②该分子中含有的组成环的原子是_______ 元素的原子,分子中共有_______ 个该原子。
(1)纳米是
(2)世界上最小的马达,只有千万分之一个蚊子那么大,如图,这种分子马达将来可用于消除体内垃圾。

①该图是马达分子的
②该分子中含有的组成环的原子是
您最近一年使用:0次
名校
解题方法
7 . 下列结构式中,从成键情况看不合理的是
A. 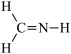 | B. 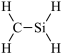 | C. 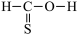 | D. 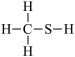 |
您最近一年使用:0次
2023-05-15更新
|
172次组卷
|
8卷引用:课时1 共价键——A学习区 夯实基础(鲁科版选修3)
课时1 共价键——A学习区 夯实基础(鲁科版选修3)(人教版2019)选择性必修2 第二章 分子结构与性质 第一节 共价键 第1课时 共价键(已下线)2011-2012年云南省昆明三中、滇池中学高二上学期期中联考化学试卷2014-2015江苏省扬州市高二上学期期末考试化学试卷(已下线)狂刷02 有机化合物的结构特点—《小题狂刷》2017-2018学年高二化学人教选修5【市级联考】江苏省高邮市2018-2019学年高二上学期期中考试化学试题2.1.1有机物中碳原子的成键特点 课前广东省广州大同中学2022-2023学年高一下学期期中考试化学试题
22-23高二·全国·课时练习
解题方法
8 . “根”与“基”的区别
| 氢氧根(OH-) | 羟基(-OH) | |
| 电子式 | ||
| 电性 | ||
| 稳定性 | ||
| 能否独立存在 |
您最近一年使用:0次
2023高二下·云南·学业考试
解题方法
9 . 元素在周期表中的位置反映了元素的原子结构和性质。下图是元素周期表的一部分,请按要求回答下列问题:
(1)元素①位于元素周期表的第_______ 周期第_______ 族,它是形成化合物种类最多的元素。
(2)写出②的元素符号_______ 。
(3)画出元素④的原子结构示意图_______ 。
(4)元素③和⑤的最高价氧化物对应的水化物中碱性较强的是_______ (填化学式)。
(5)比较⑦和⑧的简单离子半径大小_______ >_______ (填离子符号)。
(6)写出元素⑧的单质与水反应的化学方程式:_______ 。
族 周期 | IA | 0 | |||||||
| 1 | IIA | IIIA | IVA | VA | VIA | VIIA | |||
| 2 | ① | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
(2)写出②的元素符号
(3)画出元素④的原子结构示意图
(4)元素③和⑤的最高价氧化物对应的水化物中碱性较强的是
(5)比较⑦和⑧的简单离子半径大小
(6)写出元素⑧的单质与水反应的化学方程式:
您最近一年使用:0次
2023高二·北京·学业考试
名校
解题方法
10 . 某元素的原子结构示意图为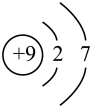 。下列关于该元素的说法
。下列关于该元素的说法
| A.元素符号是F |
| B.最低负化合价是-1价 |
| C.其原子在化学反应中容易失去电子 |
| D.在元素周期表中的位置是第二周期第VIIA族 |
您最近一年使用:0次
2023-03-15更新
|
844次组卷
|
4卷引用:1.2.1 原子结构与元素周期表(巩固)



