1 . (1)气态氢化物热稳定性 大于
大于 的主要原因是
的主要原因是__________ 。
(2) 是离子化合物,各原子均满足8电子稳定结构,
是离子化合物,各原子均满足8电子稳定结构, 的电子式是
的电子式是_______ 。
(3)常温下,在水中的溶解度乙醇大于氯乙烷,原因是__________ 。
 大于
大于 的主要原因是
的主要原因是(2)
 是离子化合物,各原子均满足8电子稳定结构,
是离子化合物,各原子均满足8电子稳定结构, 的电子式是
的电子式是(3)常温下,在水中的溶解度乙醇大于氯乙烷,原因是
您最近一年使用:0次
2020-07-11更新
|
3843次组卷
|
8卷引用:2020年浙江省高考化学试卷(7月选考)
2020年浙江省高考化学试卷(7月选考)(已下线)专题17 物质结构与性质(选修)-2020年高考真题和模拟题化学分项汇编河南省鹤壁市高级中学2020-2021学年高二上学期阶段性检测(二)化学试题(人教版2019)选择性必修2 第二章 分子结构与性质 C高考挑战区(已下线)考点08 微粒间作用力-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题08.微粒间相互作用力-十年(2012-2021)高考化学真题分项汇编(浙江专用)(已下线)【知识图鉴】单元讲练测选择性必修2第二章03单元测广东省东莞市东华高级中学2022-2023学年高二下学期3月月考化学试题
2023高一下·浙江杭州·期中
名校
解题方法
2 . 按要求完成下列各题:
(1)写出下图对应有机物的结构式___________ 。
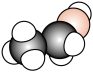
(2)CH2=CH2的电子式为___________ ,其使溴的四氯化碳溶液褪色的化学方程式为___________ 。
(3)某烷烃相对分子质量为72,其一氯代物有四种,它的结构简式为:___________ 。
(4)有下列结构的物质:
①CH3(CH2)3CH3②CH2=CHCH2CH2CH3③CH3CH2CH2CH2CH2CH3④CH2=CHCH2CH=CH2⑤CH3CH2CH2CH(CH3)CH3⑥CH2=CHCH2CH(CH3)2⑦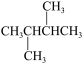 ⑧CH2=CHCH2CH2CH3
⑧CH2=CHCH2CH2CH3
其中属于同系物的是___________ ;
A.③⑤ B.②③ C.②⑥ D.①③ E.③⑦ F.④⑥
(5)聚氯乙烯(PVC)是生活中常用的塑料,写出由氯乙烯合成聚氯乙烯的化学方程式___________ ,反应类型为___________ 。
(1)写出下图对应有机物的结构式

(2)CH2=CH2的电子式为
(3)某烷烃相对分子质量为72,其一氯代物有四种,它的结构简式为:
(4)有下列结构的物质:
①CH3(CH2)3CH3②CH2=CHCH2CH2CH3③CH3CH2CH2CH2CH2CH3④CH2=CHCH2CH=CH2⑤CH3CH2CH2CH(CH3)CH3⑥CH2=CHCH2CH(CH3)2⑦
 ⑧CH2=CHCH2CH2CH3
⑧CH2=CHCH2CH2CH3其中属于同系物的是
A.③⑤ B.②③ C.②⑥ D.①③ E.③⑦ F.④⑥
(5)聚氯乙烯(PVC)是生活中常用的塑料,写出由氯乙烯合成聚氯乙烯的化学方程式
您最近一年使用:0次
2023-04-25更新
|
993次组卷
|
3卷引用:【2023】【高一下】【期中考】【杭四吴山】【高中化学】【赵涛收集】
(已下线)【2023】【高一下】【期中考】【杭四吴山】【高中化学】【赵涛收集】广东省汕尾市华大实验学校2022-2023学年高一下学期5月月考化学试题河北省行唐县启明中学2022-2023学年高一下学期5月月考化学试题
22-23高一·全国·课时练习
3 . 按要求填写下列空白:
(1)乙烷的结构式:_______ 。
(2)分子中含30个氢原子的烷烃的分子式_______ 。
(3)相对分子质量为58的烷烃的结构有_______ 种,试分别写出它们的结构简式:_______ 。
(4)分子式为C5H12的直链烷烃的习惯命名为_______ ,其一氯代物只有一种的结构简式为_______ 。
(1)乙烷的结构式:
(2)分子中含30个氢原子的烷烃的分子式
(3)相对分子质量为58的烷烃的结构有
(4)分子式为C5H12的直链烷烃的习惯命名为
您最近一年使用:0次
解题方法
4 . 元素周期表的发现是近现代化学理论诞生的标志,全世界几乎所有化学教科书后都附有元素周期表。下表为元素周期表的一部分,请回答下列有关问题。
(1)由元素①和④可形成四核 的分子,写出该分子的电子式
的分子,写出该分子的电子式_______ 。
(2)元素④和⑤可构成一种淡黄色固体化合物,写出该化合物与②的最高价氧化物反应的化学方程式_______ 。
(3)元素②、③、④简单氢化物的稳定性由高到低顺序为_______ (用化学式表示)。
(4)元素⑦、⑧、⑨的简单离子半径由大到小顺序为_______ (用离子符号表示)。
(5)写出单质⑥与元素⑤的最高价氧化物对应水化物反应的化学方程式_______ 。
(6)元素的非金属性:⑧_______ ⑩(填“>”或“<”),下列事实不能说明上述结论的是_______ 。
A.元素⑧的单质与⑩的氢化物的水溶液发生反应,溶液变为橙黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
F.常温下单质⑧为气态,单质⑩为液态
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
 的分子,写出该分子的电子式
的分子,写出该分子的电子式(2)元素④和⑤可构成一种淡黄色固体化合物,写出该化合物与②的最高价氧化物反应的化学方程式
(3)元素②、③、④简单氢化物的稳定性由高到低顺序为
(4)元素⑦、⑧、⑨的简单离子半径由大到小顺序为
(5)写出单质⑥与元素⑤的最高价氧化物对应水化物反应的化学方程式
(6)元素的非金属性:⑧
A.元素⑧的单质与⑩的氢化物的水溶液发生反应,溶液变为橙黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
F.常温下单质⑧为气态,单质⑩为液态
您最近一年使用:0次
2023-01-04更新
|
730次组卷
|
3卷引用:辽宁省重点高中2022-2023学年高一上学期期末联考化学试题
5 . 硅、硫、氮是重要的非金属元素。回答下列问题:
(1)SiO2属于___________ (填“酸性”“碱性”或“两性”)氧化物。盛装NaOH等碱性溶液的试剂瓶不能用玻璃塞,其原因为___________ (用化学方程式表示)。
(2)工业上用石英砂和焦炭混合高温制取粗硅,其反应的化学方程式为___________ ;硅的用途有___________ (任写1个)。
(3)由SO3制备H2SO4的过程中,一般用98.3%的浓硫酸吸收SO3,而不是直接用蒸馏水吸收的原因是___________ 。
(4)实验室利用含Fe3+的溶液吸收SO2,从而实现SO2的回收利用。写出Fe3+与SO2在水溶液中发生反应的离子方程式:___________ ;每消耗32gSO2,转移电子的物质的量为___________ mol。
(5)氨气遇氯化氢时会产生白烟,写出白烟化学成分的电子式:___________ 。
(1)SiO2属于
(2)工业上用石英砂和焦炭混合高温制取粗硅,其反应的化学方程式为
(3)由SO3制备H2SO4的过程中,一般用98.3%的浓硫酸吸收SO3,而不是直接用蒸馏水吸收的原因是
(4)实验室利用含Fe3+的溶液吸收SO2,从而实现SO2的回收利用。写出Fe3+与SO2在水溶液中发生反应的离子方程式:
(5)氨气遇氯化氢时会产生白烟,写出白烟化学成分的电子式:
您最近一年使用:0次
名校
6 . I.几种烷烃分子的球棍模型如图:

(1)E的分子式是_____________ 。
(2)与C互为同分异构体的有_____________ (填标号,下同),其中沸点最低的是_____________ 。
(3)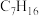 有多种同分异构体,其中主链含有五个碳原子,有两个甲基作支链的烷烃有
有多种同分异构体,其中主链含有五个碳原子,有两个甲基作支链的烷烃有_____________ 种,其中有一种同分异构体的一氯代物有4种同分异构体,请写出其结构简式_____________ 。
II.现有A、B、C三种烃,其球棍模型如图:

(4)等质量的以上物质完全燃烧时耗去 的量最多的是
的量最多的是_____________ (填对应字母)
(5)B在一定条件可以发生生成聚乙烯,其反应的方程式为_______________________________________ ,其反应类型_____________ 。
(6)除去C中少量B选用的最佳试剂_____________ 。

(1)E的分子式是
(2)与C互为同分异构体的有
(3)
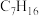 有多种同分异构体,其中主链含有五个碳原子,有两个甲基作支链的烷烃有
有多种同分异构体,其中主链含有五个碳原子,有两个甲基作支链的烷烃有II.现有A、B、C三种烃,其球棍模型如图:

(4)等质量的以上物质完全燃烧时耗去
 的量最多的是
的量最多的是(5)B在一定条件可以发生生成聚乙烯,其反应的方程式为
(6)除去C中少量B选用的最佳试剂
您最近一年使用:0次
7 . 本题主要考查有机化学基础知识,请按要求作答。
(1)羟基的电子式___________ 。
(2)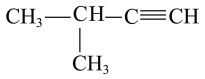 的系统命名是
的系统命名是___________ 。
(3)有机物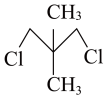 的核磁共振氢谱出现的峰面积之比为
的核磁共振氢谱出现的峰面积之比为___________ 。
(4)某烷烃C7H16,主链上有5个碳原子的同分异构体有___________ 种。
(5)写出乙苯、纯溴、铁粉反应的反应方程式___________ 。
(6)写出该有机物含有的官能团名称___________ 。
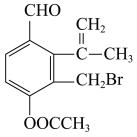
(7)写出丙烯发生加成聚合的反应方程式___________ 。
(1)羟基的电子式
(2)
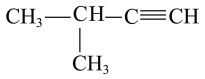 的系统命名是
的系统命名是(3)有机物
 的核磁共振氢谱出现的峰面积之比为
的核磁共振氢谱出现的峰面积之比为(4)某烷烃C7H16,主链上有5个碳原子的同分异构体有
(5)写出乙苯、纯溴、铁粉反应的反应方程式
(6)写出该有机物含有的官能团名称

(7)写出丙烯发生加成聚合的反应方程式
您最近一年使用:0次
解题方法
8 . 请回答下列问题:
(1)已知某粒子的结构示意图为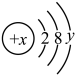 。试回答:
。试回答:
①当x-y=10时,该粒子为___________ (填“原子”“阳离子”或“阴离子”)。
②当y=8时,粒子可能为(填符号):___________ 、___________ 、___________ 、___________ 。
③写出y=1与y=6的元素最高价氧化物对应的水化物之间发生反应的离子方程式:___________ 。
(2)阿伏加德罗常数为NA,某元素的一种核素X原子的质量数为A,含N个中子,它与1H原子构成HmX分子。ag HmX的物质的量为___________ ,所含中子的物质的量为___________ ,所含质子的数目为___________ 。
(1)已知某粒子的结构示意图为
 。试回答:
。试回答:①当x-y=10时,该粒子为
②当y=8时,粒子可能为(填符号):
③写出y=1与y=6的元素最高价氧化物对应的水化物之间发生反应的离子方程式:
(2)阿伏加德罗常数为NA,某元素的一种核素X原子的质量数为A,含N个中子,它与1H原子构成HmX分子。ag HmX的物质的量为
您最近一年使用:0次
2021-12-09更新
|
1647次组卷
|
4卷引用:辽宁省沈阳市重点高中联合体2021-2022学年高一12月考试化学试题
辽宁省沈阳市重点高中联合体2021-2022学年高一12月考试化学试题专题八 原子结构与元素周期表(A卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)第四章 物质结构 元素周期律(已下线)专题突破卷05?物质结构 元素周期律?-2024年高考化学一轮复习考点通关卷(新教材新高考)
名校
解题方法
9 . 下面是同学们熟悉的微粒,完成下列问题
①N2H4 ②HBrO ③BaCl2 ④Ne ⑤NH4Cl ⑥Na2O2
(1)这些物质中,只含有共价键的是_______ (填序号,下同);只含有离子键的是_______ ;既含有极性共价键又含有离子键的是_______ ;既含有非极性共价键又含有离子键的是_______ ;属于离子化合物的是_______ 。
(2)①的结构式是_______ ;⑥的电子式是_______ 。
(3)用电子式表示NH3的形成_______ 。
(4)在下列变化中,①液溴的挥发 ②烧碱熔化 ③H2S溶于水 ④Na2O2溶于水,未发生化学键破坏的是_______ (填序号,下同),仅发生离子键破坏的是_______ ;仅发生共价键破坏的是_______ ,既发生离子键破坏又发生共价键破坏的是_______ 。
(5)下列各组微粒:① 与
与 ②
②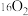 和
和 ③H2、D2、T2 ④金刚石和石墨 ⑤
③H2、D2、T2 ④金刚石和石墨 ⑤ 和
和 ,互为同位素的是
,互为同位素的是_______ ;互为同素异形体的是_______ ;质量数相等,但不能互称为同位素的是_______ 。
①N2H4 ②HBrO ③BaCl2 ④Ne ⑤NH4Cl ⑥Na2O2
(1)这些物质中,只含有共价键的是
(2)①的结构式是
(3)用电子式表示NH3的形成
(4)在下列变化中,①液溴的挥发 ②烧碱熔化 ③H2S溶于水 ④Na2O2溶于水,未发生化学键破坏的是
(5)下列各组微粒:①
 与
与 ②
②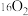 和
和 ③H2、D2、T2 ④金刚石和石墨 ⑤
③H2、D2、T2 ④金刚石和石墨 ⑤ 和
和 ,互为同位素的是
,互为同位素的是
您最近一年使用:0次
24-25高一上·全国·假期作业
名校
10 . 根据下列提供的物质回答问题:
① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨
⑨ ⑩
⑩
(1)仅含共价键的是___________ ;既有离子键又有共价键的是___________ (用序号表示)。
(2)离子化合物是___________ ;共价化合物是___________ (用序号表示)。
(3) 的电子式:
的电子式:___________ ; 的电子式:
的电子式:___________ ; 的电子式:
的电子式:___________ 。
①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨
⑨ ⑩
⑩
(1)仅含共价键的是
(2)离子化合物是
(3)
 的电子式:
的电子式: 的电子式:
的电子式: 的电子式:
的电子式:
您最近一年使用:0次
2023-11-25更新
|
586次组卷
|
3卷引用:BBWYhjhx1010.pdf



