名校
解题方法
1 . 2016年IUPAC确认了四种新元素,其中一种为Mc,中文名为“镆”元素Mc可由反应: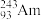 +
+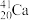 =
=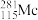 +3
+3 得到。
得到。
(1)该元素的质子数为___________ 。287Mc与288Mc互为________ 。
(2)Mc位于元素周期表中第ⅤA族,同族元素N的一种氢化物为H2N-NH2,写出该化合物分子的电子式:__________ ,该分子内存在的共价键类型有___________ 。
(3)该族中的另一元素P能呈现多种化合价,其中+3价氧化物的化学式为_______ ,+5价简单含氧酸的化学式为_________ 。
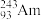 +
+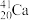 =
=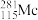 +3
+3 得到。
得到。(1)该元素的质子数为
(2)Mc位于元素周期表中第ⅤA族,同族元素N的一种氢化物为H2N-NH2,写出该化合物分子的电子式:
(3)该族中的另一元素P能呈现多种化合价,其中+3价氧化物的化学式为
您最近一年使用:0次
名校
2 . 氮化钠(Na3N)是用科学方法制备的一种重要化合物,它与水作用产生NH3。请回答下列问题:
(1)Na3N的电子式是____________ ,该化合物由______ 键形成。
(2)Na3N与盐酸反应生成________ 种盐,其电子式分别为______________ 。
(1)Na3N的电子式是
(2)Na3N与盐酸反应生成
您最近一年使用:0次
解题方法
3 . 亚硝酰氯(NOCl)是有机药物制备的重要试剂,可按以下流程合成和利用。
请回答:
(1)NOCl的电子式为_______ ,化合物X的结构简式为_______ 。
(2)下列说法正确的是_______。
(3)已知浓盐酸和浓硝酸混合配制王水时会产生亚硝酰氯,写出该反应的化学方程式_______ 。

请回答:
(1)NOCl的电子式为
(2)下列说法正确的是_______。
| A.NOCl中的氮元素呈正价 |
| B.NOCl分子的空间结构为V形 |
C.化合物X的沸点低于氯乙酰胺( ) ) |
| D.工业上可以用蒸馏水吸收多余的NOCl,防止污染环境 |
您最近一年使用:0次
名校
解题方法
4 . 下表是某些短周期元素的电负性(x)值:
(1)根据上表试推测,元素周期表中除放射性元素外,电负性最小的元素与电负性最大的元素形成的化合物的电子式为___________ 。
(2)已知: 。
。
①若 最初水解产物是
最初水解产物是 和HClO,根据
和HClO,根据 的化合价推测
的化合价推测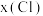 的范围是
的范围是___________ (填表中数值);
② 水解的化学反应方程式是
水解的化学反应方程式是___________ 。
(3)一般认为:如果两个成键元素间的电负性差值大于1.7,它们之间通常形成离子键,小于1.7通常形成共价键,结合问题(2)①进行分析, 属于
属于___________ (填“离子化合物”或“共价化合物”),可设计实验证明,如测定___________ 。
| 元素符号 | Li | Be | N | O | F | Na | Mg | Al | P | S |
| x值 | 1.0 | 1.5 | 3.0 | a | 4.0 | 0.9 | 1.2 | 1.5 | 2.1 | 2.5 |
(2)已知:
 。
。①若
 最初水解产物是
最初水解产物是 和HClO,根据
和HClO,根据 的化合价推测
的化合价推测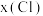 的范围是
的范围是②
 水解的化学反应方程式是
水解的化学反应方程式是(3)一般认为:如果两个成键元素间的电负性差值大于1.7,它们之间通常形成离子键,小于1.7通常形成共价键,结合问题(2)①进行分析,
 属于
属于
您最近一年使用:0次
名校
5 . 研究含氮元素物质的反应对生产、生活、科研等方面具有重要的意义。请回答下列问题: 不稳定,在水溶液中就会发生歧化反应,其中一种产物为
不稳定,在水溶液中就会发生歧化反应,其中一种产物为 。
。
请回答:
(1)写出肼的电子式______ 。
(2)写出反应I的化学方程式______ 。
(3)下列说法正确的是______。
(4)已知: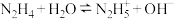 ,
, 与
与 溶液作用,产生常见气体M,并生成一种溶于稀硝酸的白色沉淀N。
溶液作用,产生常见气体M,并生成一种溶于稀硝酸的白色沉淀N。
①生成的气体M和白色沉淀N的成分分别是______ 、______ (填化学式)。
②请设计实验验证白色沉淀N的组成元素______ 。

已知:①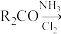
 (异肼)
(异肼)
 不稳定,在水溶液中就会发生歧化反应,其中一种产物为
不稳定,在水溶液中就会发生歧化反应,其中一种产物为 。
。请回答:
(1)写出肼的电子式
(2)写出反应I的化学方程式
(3)下列说法正确的是______。
A.碱性: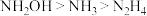 |
| B.肼可以用做还原剂,也可用做配合物的配体 |
| C.肼在水中的溶解度小于在苯中的溶解度 |
| D.反应Ⅱ中的产物之一可以循环利用 |
(4)已知:
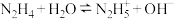 ,
, 与
与 溶液作用,产生常见气体M,并生成一种溶于稀硝酸的白色沉淀N。
溶液作用,产生常见气体M,并生成一种溶于稀硝酸的白色沉淀N。①生成的气体M和白色沉淀N的成分分别是
②请设计实验验证白色沉淀N的组成元素
您最近一年使用:0次
名校
6 . 2019年诺贝尔化学奖颁发给JohnB.Goodenough、M.StanleyWhittingham和Akira Yoshino,用于“表彰锂离子电池的开发”。一种锂-空气电池的工作原理如图所示。其中多孔电极材料选用纳米多孔金时,该电池表现出良好的循环性能。电池反应为: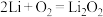 。
。___________ ,写出过氧化锂的电子式___________ 。
2.该电池工作时,正极反应经过两个过程:
第一个过程的电极反应式为: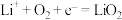 ;则第二个过程的电极反应式为:
;则第二个过程的电极反应式为:___________
3.应用该电池电镀铜,阴极质量增加64g,理论上负极将消耗___________ g Li。
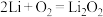 。
。
2.该电池工作时,正极反应经过两个过程:
第一个过程的电极反应式为:
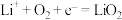 ;则第二个过程的电极反应式为:
;则第二个过程的电极反应式为:3.应用该电池电镀铜,阴极质量增加64g,理论上负极将消耗
您最近一年使用:0次
名校
7 . 海洋化学资源的研究和合理利用具有广阔前景,从海水中可提取氯、溴、碘等卤族元素。
1.氯离子结构示意图为___________ ,碘在元素周期表中的位置是___________ 。
2.氯气可用来制取漂白粉,漂白粉的有效成分是___________ 。
3.次氯酸钠可用于去除废水中的铵态氮,配平离子方程式并标出电子转移方向和数目。___________
___________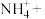 ___________
___________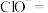 ___________
___________ ___________
___________ ___________
___________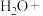 ___________
___________
1.氯离子结构示意图为
2.氯气可用来制取漂白粉,漂白粉的有效成分是
3.次氯酸钠可用于去除废水中的铵态氮,配平离子方程式并标出电子转移方向和数目。
___________
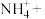 ___________
___________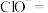 ___________
___________ ___________
___________ ___________
___________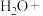 ___________
___________
您最近一年使用:0次
8 .  是一种常见的催化剂,在氯酸钾分解、双氧水分解的反应中作催化作用。
是一种常见的催化剂,在氯酸钾分解、双氧水分解的反应中作催化作用。
1.基态Mn原子的价电子轨道表示式为___________ ;其核外有___________ 种不同能量的电子。
2.氯酸钾熔融状态下的电离方程式为___________ ;双氧水的电子式为___________ 。
 是一种常见的催化剂,在氯酸钾分解、双氧水分解的反应中作催化作用。
是一种常见的催化剂,在氯酸钾分解、双氧水分解的反应中作催化作用。1.基态Mn原子的价电子轨道表示式为
2.氯酸钾熔融状态下的电离方程式为
您最近一年使用:0次
解题方法
9 . 下图是氮的化合物的“价类二维图”。______ ,该物质的电子式_____ 。
(2)写出实验室制取氨气的化学方程式:______ 。
(3)实验室中硝酸通常保存在棕色瓶中,硝酸保存在棕色瓶中的原因:____ (请用方程式解释。)
(4)使用浓硝酸进行实验:反应剧烈进行,铜丝逐渐变细,溶液变绿,试管上方出现红棕色气体。铜与浓硝酸反应的化学方程式为_____ ;以上反应中酸性与氧化性硝酸的物质的量之比_____ 。
(5)工业生产中为了盛装大量浓硝酸,可选择_____ 作为罐体材料。
a.铜 b.铝 c.铂 d.镁
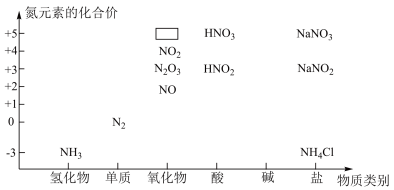
(2)写出实验室制取氨气的化学方程式:
(3)实验室中硝酸通常保存在棕色瓶中,硝酸保存在棕色瓶中的原因:
(4)使用浓硝酸进行实验:反应剧烈进行,铜丝逐渐变细,溶液变绿,试管上方出现红棕色气体。铜与浓硝酸反应的化学方程式为
(5)工业生产中为了盛装大量浓硝酸,可选择
a.铜 b.铝 c.铂 d.镁
您最近一年使用:0次
解题方法
10 . 回答下列问题
(1)用做消化系统X射线检查的内服药剂“钡餐”的化学式为___________ 。
(2)酸雨的
___________ 5.6(填“>”、“<”、“=”)。
(3) 的电子式
的电子式___________ 。
(4)工业上用焦炭还原石英砂可以制得含有少量杂质的粗硅,化学方程式为___________ 。
(5)己知:①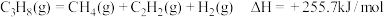
②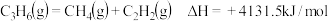
则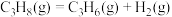 的
的
___________ 。
(1)用做消化系统X射线检查的内服药剂“钡餐”的化学式为
(2)酸雨的

(3)
 的电子式
的电子式(4)工业上用焦炭还原石英砂可以制得含有少量杂质的粗硅,化学方程式为
(5)己知:①
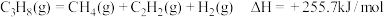
②
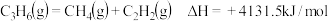
则
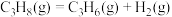 的
的
您最近一年使用:0次



