名校
解题方法
1 . 下列化学用语表示错误的是
| A.基态镓原子的电子排布式为[Ar]4s24p1 |
B.60gSiO2中含有Si-O键数目为 |
C.砷化氢(AsH3)分子的球棍模型: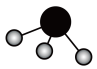 |
D.过氧化钠(Na2O2)的电子式: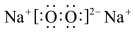 |
您最近一年使用:0次
2 . 下列化学用语或图示表达正确的是
A.乙烯的结构简式: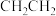 | B.碳化硅的分子式:SiC |
C.Cr的核外电子排布式: | D.乙醇的核磁共振氢谱图: |
您最近一年使用:0次
3 . 下列图示正确的是
A.中子数为16的硫原子: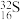 |
B. 电子的电子云轮廓图: 电子的电子云轮廓图: |
C. 的形成过程: 的形成过程: |
D.测定 相对分子质量的质谱图: 相对分子质量的质谱图: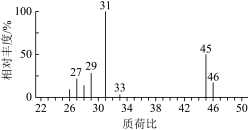 |
您最近一年使用:0次
2023-02-18更新
|
663次组卷
|
3卷引用:湖南省长沙市麓山国际实验学校2022-2023学年高三下学期3月月考化学试题
解题方法
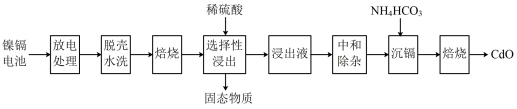
4 . 镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知镍镉电池的电池总反应为: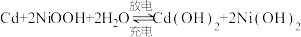 ,利用废旧镍镉电池回收铬的流程如下:
,利用废旧镍镉电池回收铬的流程如下:
已知:中和除杂后的溶液中主要含有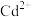 、
、 、
、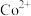 。
。
回答下列问题:
(1)NiOOH中,Ni的化合价为:______ 。
(2)写出“焙烧”过程中含镍物质变化的化学反应方程式:______ 。
(3)在“选择性浸出”一步中,40℃时,不同的金属氧化物在稀 中2小时后的浸出率随PH的变化如下图1所示,则:
中2小时后的浸出率随PH的变化如下图1所示,则:

①“选择性浸出”时,最适宜的pH为______ (填选项字母),写出在此pH下发生的主要离子方程式:______ 。
A.5 B.4 C.3 D.2
②浸出液中各元素含量如表1所示。Co的浓度比镍还小的原因可能是:______ 。
表1 浸出液组成
(4)沉铬时生成 的离子反应方程式:
的离子反应方程式:______ 。
(5)镍铬电池充电时, 移向
移向______ (填“明极”或“阳极”),写出阳极的电极反应式:______ 。
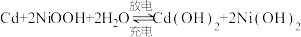 ,利用废旧镍镉电池回收铬的流程如下:
,利用废旧镍镉电池回收铬的流程如下:
已知:中和除杂后的溶液中主要含有
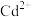 、
、 、
、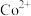 。
。回答下列问题:
(1)NiOOH中,Ni的化合价为:
(2)写出“焙烧”过程中含镍物质变化的化学反应方程式:
(3)在“选择性浸出”一步中,40℃时,不同的金属氧化物在稀
 中2小时后的浸出率随PH的变化如下图1所示,则:
中2小时后的浸出率随PH的变化如下图1所示,则:
①“选择性浸出”时,最适宜的pH为
A.5 B.4 C.3 D.2
②浸出液中各元素含量如表1所示。Co的浓度比镍还小的原因可能是:
| 元素Elements | Cd | Ni | Co | Fe |
浓度(Concentrations/( ) ) | 77.5 | 2.61 | 0.406 | 0.176 |
表1 浸出液组成
(4)沉铬时生成
 的离子反应方程式:
的离子反应方程式:(5)镍铬电池充电时,
 移向
移向
您最近一年使用:0次
2022-08-18更新
|
156次组卷
|
2卷引用:贵州省思南县梵净山中学2022-2023学年高三上学期11月月考化学试题
5 . 工业上利用氧化铝基废催化剂(主要成分为Al2O3,少量Pd)回收Al2(SO4)3及Pd 流程如图:

说明:上述流程中焙烧温度不宜过高,否则会导致硫酸铵固体的分解。
(1)焙烧时产生气体X的结构式为________ 。
(2)水浸分离中,滤渣Pd的颗粒比较大,一般可以采用的分离方法是_________ (填字母)
A.过滤 B.抽滤 C.倾析 D.渗析
(3)写出酸浸时发生反应的离子方式______ (已知氯钯酸为弱酸)
(4)某同学在实验室用如下图所示装置完成Pd的热还原实验,并计算滤渣中 (NH4)2PdCl6的百分含量(滤渣中的杂质不参与热还原反应)。

①写出热还原法过程中发生反应的化学方程式________ 。
②i.将石英玻璃管中(带开关;K1和K2)(设为装置A )称重,记为mi g。将滤渣 [(NH4)2PdCl6]装入石英玻璃管中,再次将装置A称重,记为m2 g。
ii.连接好装置后,按d→ → →b→ →e(填标号)顺序进行实验。_______
a.关闭K1和K2 b.熄灭酒精灯 c.点燃酒精灯,加热
d.打开K1和K2 e.称量A f.缓缓通入H2 g.冷却至室温
iii.重复上述操作步骤,直至A恒重,记为m3g。
③根据实验记录,计算滤渣中(NH4)2PdCl6的百分含量__________ [列式表示,其中(NH4)2PdCl6相对分子质量为355]。
④实验结束时,发现硬质试管右端有少量白色固体,可能是____ (填化学式),这种情况导致实验结果_________ (填“偏高”、“偏低”、“无影响”)

说明:上述流程中焙烧温度不宜过高,否则会导致硫酸铵固体的分解。
(1)焙烧时产生气体X的结构式为
(2)水浸分离中,滤渣Pd的颗粒比较大,一般可以采用的分离方法是
A.过滤 B.抽滤 C.倾析 D.渗析
(3)写出酸浸时发生反应的离子方式
(4)某同学在实验室用如下图所示装置完成Pd的热还原实验,并计算滤渣中 (NH4)2PdCl6的百分含量(滤渣中的杂质不参与热还原反应)。

①写出热还原法过程中发生反应的化学方程式
②i.将石英玻璃管中(带开关;K1和K2)(设为装置A )称重,记为mi g。将滤渣 [(NH4)2PdCl6]装入石英玻璃管中,再次将装置A称重,记为m2 g。
ii.连接好装置后,按d→ → →b→ →e(填标号)顺序进行实验。
a.关闭K1和K2 b.熄灭酒精灯 c.点燃酒精灯,加热
d.打开K1和K2 e.称量A f.缓缓通入H2 g.冷却至室温
iii.重复上述操作步骤,直至A恒重,记为m3g。
③根据实验记录,计算滤渣中(NH4)2PdCl6的百分含量
④实验结束时,发现硬质试管右端有少量白色固体,可能是
您最近一年使用:0次
2020-01-01更新
|
503次组卷
|
2卷引用:辽宁省实验中学2022届高三第一次阶段性考试化学试题



