名校
解题方法
1 . 二氧化硫能与硫化氢反应: ,产生淡黄色固体。下列有关化学用语的表述正确的是
,产生淡黄色固体。下列有关化学用语的表述正确的是
 ,产生淡黄色固体。下列有关化学用语的表述正确的是
,产生淡黄色固体。下列有关化学用语的表述正确的是A.S的原子结构示意图: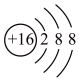 |
B. 结构式: 结构式: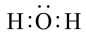 |
C. 和 和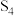 互为同位素 互为同位素 |
D.用电子式表示 形成过程: 形成过程: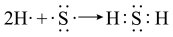 |
您最近一年使用:0次
名校
解题方法
2 . 已知: ,下列说法错误的是
,下列说法错误的是
 ,下列说法错误的是
,下列说法错误的是A.Na原子的结构示意图为: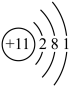 |
| B.Cl2的结构式为:Cl—Cl |
C.NaCl的电子式为: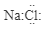 |
| D.该反应既是化合反应,又是氧化还原反应 |
您最近一年使用:0次
名校
解题方法
3 . 卤族元素相关物质在生产、生活中应用广泛。回答下列问题:
(1) 的离子结构示意图为
的离子结构示意图为______ 。
(2)卤素单质有着相似的化学性质,但同时也有差别。比如 与NaOH反应生成NaCl、NaClO和水,而
与NaOH反应生成NaCl、NaClO和水,而 与NaOH发生如下反应:
与NaOH发生如下反应: 。其中
。其中 的电子式为
的电子式为______ ,用电子式描述NaF的形成过程:______ 。
(3)根据卤族元素性质的相似性和递变性,推测元素砹(At)的单质为有色固体,HAt的稳定性______ (填“大于”或“小于”)HI的稳定性,AgAt______ (填“易”或“难”)溶于水。
(4)不同卤素原子之间以共价键相结合形成的化合物称为卤素互化物,如 等。它们与卤素单质性质相似。
等。它们与卤素单质性质相似。
① 与水反应的产物可能为
与水反应的产物可能为______ (填化学式)。
②下列说法不正确的是______ 。
A.HF、HCl、HBr的沸点依次升高
B. 沸点依次升高
沸点依次升高
C.已知离子半径大小会影响离子键的强弱,从而影响物质的熔点:若离子半径越大,离子键越弱。据此推测NaF、NaCl、NaBr熔点依次降低
D. (X代表F、Cl、Br)的酸性随着X的原子序数递增逐渐减弱
(X代表F、Cl、Br)的酸性随着X的原子序数递增逐渐减弱
(1)
 的离子结构示意图为
的离子结构示意图为(2)卤素单质有着相似的化学性质,但同时也有差别。比如
 与NaOH反应生成NaCl、NaClO和水,而
与NaOH反应生成NaCl、NaClO和水,而 与NaOH发生如下反应:
与NaOH发生如下反应: 。其中
。其中 的电子式为
的电子式为(3)根据卤族元素性质的相似性和递变性,推测元素砹(At)的单质为有色固体,HAt的稳定性
(4)不同卤素原子之间以共价键相结合形成的化合物称为卤素互化物,如
 等。它们与卤素单质性质相似。
等。它们与卤素单质性质相似。①
 与水反应的产物可能为
与水反应的产物可能为②下列说法不正确的是
A.HF、HCl、HBr的沸点依次升高
B.
 沸点依次升高
沸点依次升高C.已知离子半径大小会影响离子键的强弱,从而影响物质的熔点:若离子半径越大,离子键越弱。据此推测NaF、NaCl、NaBr熔点依次降低
D.
 (X代表F、Cl、Br)的酸性随着X的原子序数递增逐渐减弱
(X代表F、Cl、Br)的酸性随着X的原子序数递增逐渐减弱
您最近一年使用:0次
2024-04-04更新
|
197次组卷
|
2卷引用:重庆市巴蜀中学校2023-2024学年高一下学期3月月考化学试题
真题
名校
4 . 化学用语可以表达化学过程,下列化学用语的表达错误的是
A.用电子式表示 的形成: 的形成: |
B.用离子方程式表示 溶于烧碱溶液: 溶于烧碱溶液: |
C.用电子云轮廓图表示H-H的s-sσ键形成的示意图: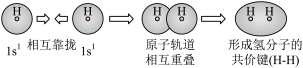 |
D.用化学方程式表示尿素与甲醛制备线型脲醛树脂: |
您最近一年使用:0次
2023-06-14更新
|
8721次组卷
|
14卷引用:福建省宁德第一中学2024届高三上学期第一次检测化学试题
福建省宁德第一中学2024届高三上学期第一次检测化学试题2023年高考湖北卷化学真题(已下线)专题02 化学用语(已下线)T5-化学用语(已下线)专题02 化学用语(已下线)专题02 化学用语(已下线)考点08 微粒间相互作用力(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第3讲 化学键 共价键的类型及键参数(已下线)专题02 化学用语的正误判断-2023年高考化学真题题源解密(全国通用)(已下线)专题02 化学用语及其应用-2023年高考化学真题题源解密(新高考专用)(已下线)选择题1-5江西省宜春市宜丰中学创新部2023-2024学年高三上学期期中考试化学试题(已下线)题型01 物质的组成与分类 传统文化 化学用语-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)河南省信阳高级中学2023-2024学年高三上学期11月一模考试化学试题
5 . 四川广汉“三星堆”遗址出土了大量距今3000多年前的象牙,科考人员采用纤维布和聚氨酯树脂混合制成的医用高分子绷带固定保存。合成聚氨酯的一种原料是多异氰酸酯。一种异氰酸酯分子的键线式如下图。

【资料】表示有机化合物的组成和结构时,若将碳、氢元素符号省略,只表示分子中键的链接情况和官能团,每个拐点或终点均表示一个碳原子,则得到键线式。如丙烯可表示为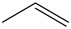 ,乙醇可表示为
,乙醇可表示为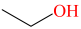 。
。
下列说法不正确的是

【资料】表示有机化合物的组成和结构时,若将碳、氢元素符号省略,只表示分子中键的链接情况和官能团,每个拐点或终点均表示一个碳原子,则得到键线式。如丙烯可表示为
 ,乙醇可表示为
,乙醇可表示为 。
。下列说法不正确的是
| A.N在元素周期表中位于第二周期ⅤA族 |
B.图中所示分子的分子式为 |
C.基团“-N=C=O”的电子式为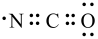 |
D.图中所示分子存在含氨基(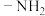 )、碳碳双键、醛基的同分异构体 )、碳碳双键、醛基的同分异构体 |
您最近一年使用:0次
解题方法
6 . 下列说法正确的是
A.同位素示踪会用到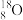 ,该氧原子有8个中子 ,该氧原子有8个中子 | B.NH3分子中只含有极性共价键 |
C. 的电子式: 的电子式: | D.丙炔的结构简式:CHCHCH3 |
您最近一年使用:0次
7 . 电子在原子核外的区域内作高速运动,根据电子的能量高低划分为电子层,在各电子层上电子的排布也遵循着一定的规律。
(1)下列所列各项中,与元素的化学性质关系最密切的是
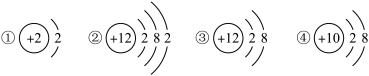
(2)下列是几种粒子的结构示意图,有关说法正确的是
(3)反应8NH3+3Cl2=6NH4Cl+N2可用于氯气管道的检漏。下列表示相关微粒的表示或说法正确的是
(1)下列所列各项中,与元素的化学性质关系最密切的是
| A.元素的相对原子质量 | B.元素的核电荷数 |
| C.原子的核外电子数 | D.原子的最外层电子数 |

| A.①和②两种粒子的化学性质相似 | B.③和④均属于离子结构示意图 |
| C.粒子②在化学反应中容易失去电子 | D.①②③④共表示四种元素的粒子 |
A.中子数为9的氮原子: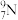 | B.每个NH3分子中含10个电子 |
C.N原子的电子式: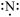 | D.Cl的结构示意图: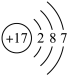 |
您最近一年使用:0次
名校
解题方法
8 . 实验室常用稀硫酸与锌反应来制备氢气,发生反应的化学方程式为 (稀)
(稀)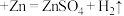 ,下列说法正确的是
,下列说法正确的是
 (稀)
(稀)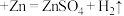 ,下列说法正确的是
,下列说法正确的是A.中子数为2的H原子: | B. 的结构示意图: 的结构示意图: |
C.简单离子半径: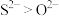 | D. 为共价化合物 为共价化合物 |
您最近一年使用:0次
2023-03-17更新
|
382次组卷
|
3卷引用:山西省2022-2023学年高一下学期3月联合考试化学试题
名校
解题方法
9 . 原子结构与化学键
人们运用化学科学,从分子、原子水平上研究了物质及其变化规律。原子结构理论和化学键理论从微观层次揭示了物质的结构。
(1)日本的福岛核废水中含有一种对环境有害的放射性核素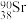 ,关于该核素说法错误是___________。
,关于该核素说法错误是___________。
(2)硒是人体必需的微量元素,如图是元素硒的信息,关于硒元素的说法错误的是___________。

(3)下列性质的比较,不能用元素周期律解释的是___________。
(4)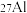 是地壳中最丰富的金属元素,其原子含有中子数为
是地壳中最丰富的金属元素,其原子含有中子数为___________ ,与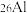 互为
互为___________ 。用化学符号表示铝离子的结构示意图___________ 。A1与 两种微粒在结构上相同的是
两种微粒在结构上相同的是___________ (填选项字母)。
A.质子数 B.核外电子数 C.电子层数 D.最外层电子数
(5)汽车安全气囊中的填充物有 (叠氮酸钠)、
(叠氮酸钠)、 、
、 等物质,
等物质, 遇撞击时能生成金属钠和
遇撞击时能生成金属钠和 ,气囊的体积迅速膨胀,达到保护驾乘人员的目的。
,气囊的体积迅速膨胀,达到保护驾乘人员的目的。
①写出 的电子式
的电子式___________ 。
② 是由一种单原子离子和一种多原子离子以1∶1的比例构成的化合物。
是由一种单原子离子和一种多原子离子以1∶1的比例构成的化合物。 晶体中存在的化学键类型是
晶体中存在的化学键类型是___________ 。
③汽车安全气囊填充物的三种物质中属于共价化合物的是___________ (填化学式),所涉及的5种元素中,原子半径最大的是___________ (填元素符号)。
④某品牌汽车的安全气囊中若有13g ,遇撞击时能产生气体
,遇撞击时能产生气体___________ L(标准状况下),转移电子___________ mol。
(6) 、
、 能与金属钠发生反应生成
能与金属钠发生反应生成 ,化学方程式如下所示:
,化学方程式如下所示:
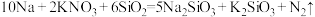
①用单线桥法在上述的化学方程式中标出电子转移的方向和数目___________ 。
②上述反应中氧化剂是___________ (填写化学式,下同),氧化产物是___________ 。
人们运用化学科学,从分子、原子水平上研究了物质及其变化规律。原子结构理论和化学键理论从微观层次揭示了物质的结构。
(1)日本的福岛核废水中含有一种对环境有害的放射性核素
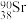 ,关于该核素说法错误是___________。
,关于该核素说法错误是___________。A.与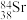 的化学性质几乎相同 的化学性质几乎相同 | B.中子数与质子数之差为52 |
C.与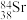 互为同位素 互为同位素 | D.Sr在元素周期表中位于ⅡA族 |

| A.位于ⅥA族 | B.质量数为34 |
| C.位于第四周期 | D.相对原子质量为78.96 |
| A.非金属性:F>O>N |
| B.碱性:KOH>NaOH>LiOH |
C.热稳定性: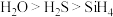 |
D.酸性: |
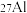 是地壳中最丰富的金属元素,其原子含有中子数为
是地壳中最丰富的金属元素,其原子含有中子数为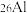 互为
互为 两种微粒在结构上相同的是
两种微粒在结构上相同的是A.质子数 B.核外电子数 C.电子层数 D.最外层电子数
(5)汽车安全气囊中的填充物有
 (叠氮酸钠)、
(叠氮酸钠)、 、
、 等物质,
等物质, 遇撞击时能生成金属钠和
遇撞击时能生成金属钠和 ,气囊的体积迅速膨胀,达到保护驾乘人员的目的。
,气囊的体积迅速膨胀,达到保护驾乘人员的目的。①写出
 的电子式
的电子式②
 是由一种单原子离子和一种多原子离子以1∶1的比例构成的化合物。
是由一种单原子离子和一种多原子离子以1∶1的比例构成的化合物。 晶体中存在的化学键类型是
晶体中存在的化学键类型是③汽车安全气囊填充物的三种物质中属于共价化合物的是
④某品牌汽车的安全气囊中若有13g
 ,遇撞击时能产生气体
,遇撞击时能产生气体(6)
 、
、 能与金属钠发生反应生成
能与金属钠发生反应生成 ,化学方程式如下所示:
,化学方程式如下所示: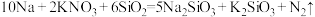
①用单线桥法在上述的化学方程式中标出电子转移的方向和数目
②上述反应中氧化剂是
您最近一年使用:0次
10 . 氢氟酸是芯片加工的重要试剂,可通过反应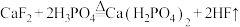 制取。下列说法正确的是
制取。下列说法正确的是
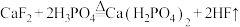 制取。下列说法正确的是
制取。下列说法正确的是A.基态 原子的电子排布式为 原子的电子排布式为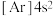 | B. 的电子式为 的电子式为 |
C.中子数为15的P可以表示为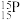 | D. 的电离方程式为 的电离方程式为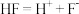 |
您最近一年使用:0次
2023-03-09更新
|
346次组卷
|
2卷引用:江苏省南通市崇川区等5地2022-2023学年高三下学期3月月考化学试题



