解题方法
1 . 化学语言与概念是高考评价体系中要求的必备知识之一,下列关于化学语言与概念的表述正确的是
A.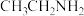 的化学名称:乙氨 的化学名称:乙氨 | B. 的化学名称:二乙酸 的化学名称:二乙酸 |
C.乙醛的球棍模型: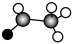 | D.乙醚的分子式: |
您最近一年使用:0次
2 . 科学研究表明,多聚磷酸的结构如图所示: 试从物质的结构分析,下列推测不正确的是
试从物质的结构分析,下列推测不正确的是
| A.多聚磷酸分子间存在氢键,可能为黏稠状的液体 |
B.焦磷酸(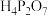 )为常见多磷酸,可以由正磷酸分子间脱水而来 )为常见多磷酸,可以由正磷酸分子间脱水而来 |
C.多磷酸钠(多磷酸对应的正盐)的化学式为 |
| D.三聚磷酸分子中存在两种H原子,比例为2:3 |
您最近一年使用:0次
2022-11-23更新
|
925次组卷
|
4卷引用:浙江省绍兴市2022-2023学年高三上学期11月份选考科目诊断性考试(一模)化学试题
浙江省绍兴市2022-2023学年高三上学期11月份选考科目诊断性考试(一模)化学试题(已下线)【知识图鉴】单元讲练测选择性必修2第二章02练基础辽宁省实验中学2022-2023学年高二下学期阶段测试化学试题(已下线)2.3.2 分子间作用力、分子的手性课堂例题
3 . 在牙膏中添加氟化物能起到预防龋齿的作用,原理是生成了更能抵抗酸蚀的氟磷灰石 ,下列有关化学用语正确的是
,下列有关化学用语正确的是
 ,下列有关化学用语正确的是
,下列有关化学用语正确的是A.基态F原子价电子排布图: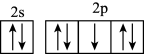 | B. 的结构示意图: 的结构示意图: |
C.中子数为16的磷核素: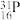 | D. 的电子式为: 的电子式为: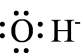 |
您最近一年使用:0次
2022-05-12更新
|
496次组卷
|
4卷引用:辽宁省部分重点中学协作体2022届高三第二次模拟考试化学试题
4 . 3D打印对钛粉末的要求很高。熔盐电解精炼是制取钛粉的有效途径。精炼时一般采用等摩尔比的KCl-NaCl熔盐,其中含有一定浓度的低价氯化钛(TiClx,x=2、3)。(已知:①熔盐中Ti3+少,Ti2+多熔盐电解精炼制得的钛粉颗粒相对粗大;②钛的熔点为1668℃,TiCl4熔点-24. 1℃、沸点136. 4℃)。
(1)精炼时,粗品质的海绵钛、废钛材等做电解池的_______ 极。
(2)采用海绵钛与TiCl4制取低价钛离子的电解质熔盐时,熔盐中存下如下4个反应:
ⅰ.3Ti4++Ti0→4Ti3+△H1
ⅱ.Ti4++Ti0→2Ti2+△H2
ⅲ.Ti4++Ti2+→2Ti3+△H3
ⅳ._______ △H4
①反应ⅳ的化学方程式为_______ 。
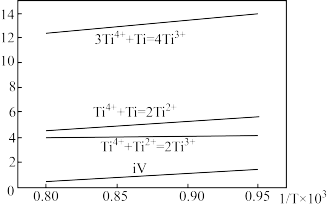
②上述4个反应的平衡常数与温度的关系如下图。由此可知△H1_______ 3△H2(填“>”、“<”或“=”)。
③有助于制取低价钛离子的电解质熔盐的措施为_______ 。
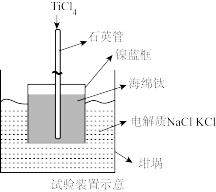
(3)向下图装置中加入海绵钛,从石英管中缓慢加入a mol TiCl4,恒温条件下进行反应。
①平衡时,测得消耗海绵钛及TiCl4的物质的量分别为b mol、c mol。熔盐中低价钛离子的平均价态为_______ 。
②用各离子的物质的量分数表示平衡浓度,则反应ⅲ的平衡常数K3=_______ 。
③若向此平衡体系中继续注入TiCl4,则再次平衡后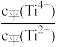
_______ (填“增大”、“减小”或“不变”)
(4)电解精炼制钛粉,偶尔会得到一些相对粗大的钛粉颗粒而影响产品质量,请分析产生的原因_______ (写出1条原因,合理即可。)
(1)精炼时,粗品质的海绵钛、废钛材等做电解池的
(2)采用海绵钛与TiCl4制取低价钛离子的电解质熔盐时,熔盐中存下如下4个反应:
ⅰ.3Ti4++Ti0→4Ti3+△H1
ⅱ.Ti4++Ti0→2Ti2+△H2
ⅲ.Ti4++Ti2+→2Ti3+△H3
ⅳ._______ △H4
①反应ⅳ的化学方程式为
②上述4个反应的平衡常数与温度的关系如下图。由此可知△H1

③有助于制取低价钛离子的电解质熔盐的措施为
(3)向下图装置中加入海绵钛,从石英管中缓慢加入a mol TiCl4,恒温条件下进行反应。

①平衡时,测得消耗海绵钛及TiCl4的物质的量分别为b mol、c mol。熔盐中低价钛离子的平均价态为
②用各离子的物质的量分数表示平衡浓度,则反应ⅲ的平衡常数K3=
③若向此平衡体系中继续注入TiCl4,则再次平衡后
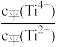
(4)电解精炼制钛粉,偶尔会得到一些相对粗大的钛粉颗粒而影响产品质量,请分析产生的原因
您最近一年使用:0次
5 . 北京冬奥会使用了更节能环保的CO2跨临界直冷制冰技术。下列关于CO2的说法正确的是
| A.结构式:O-C-O | B.电子式: |
| C.分子构型:直线形 | D.球棍模型: |
您最近一年使用:0次
6 . 下列物质的结构简式和名称对应错误的是
| A | B | C | D | |
| 结构简式 | 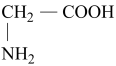 | 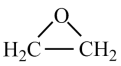 | 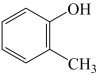 | 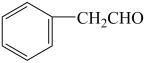 |
| 名称 | 甘氨酸 | 环氧乙烷 | 邻甲基苯酚 | 苯甲醛 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 可用“沉淀法”除去粗盐中的 、
、 、
、 杂质。某小组探究沉淀剂添加顺序及过滤方式对产品中硫酸根杂质含量的影响,实验流程及结果如下。
杂质。某小组探究沉淀剂添加顺序及过滤方式对产品中硫酸根杂质含量的影响,实验流程及结果如下。
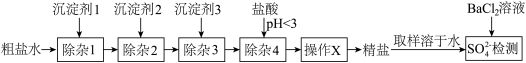
(1)实验1中加入沉淀剂3后会生成_______ (填化学式)。
(2)“除杂4”发生反应的离子方程式有_______ 。
(3)“操作X”为_______ 。
(4)查阅资料:难溶电解质的溶解度会受到溶液中其它离子的影响。加入与难溶电解质相同离子的电解质,因“同离子效应”溶解度降低;加入与难溶电解质不同离子的电解质,因“盐效应”溶解度增大。
①提出假设:
②设计实验:探究不同试剂对硫酸钡溶解度的影响程度
“滤液处理”需用到的试剂有_______ 。
③实验分析:实验3中 溶液的用量为理论值的1.5倍,最后仍检出
溶液的用量为理论值的1.5倍,最后仍检出 的原因是该体系中“同离子效应”
的原因是该体系中“同离子效应”_______ “盐效应”(填“大于”或“小于”)。
④实验结论:粗盐提纯时,为了有效降低产品中 含量,必须
含量,必须_______ 。
 、
、 、
、 杂质。某小组探究沉淀剂添加顺序及过滤方式对产品中硫酸根杂质含量的影响,实验流程及结果如下。
杂质。某小组探究沉淀剂添加顺序及过滤方式对产品中硫酸根杂质含量的影响,实验流程及结果如下。
| 沉淀剂1 | 沉淀剂1 | 沉淀剂1 | 过滤方式 |  检测结果 检测结果 | |
| 实验1 |  溶液 溶液 | NaOH溶液 |  溶液 溶液 | 逐一过滤 | 少量浑浊 |
| 实验2 |  溶液 溶液 |  溶液 溶液 | NaOH溶液 | 逐一过滤 | 少量浑浊 |
| 实验3 | NaOH溶液 |  溶液 溶液 |  溶液 溶液 | 逐一过滤 | 大量沉淀 |
| 实验4 |  溶液 溶液 | NaOH溶液 |  溶液 溶液 | 一起过滤 | 大量沉淀 |
(2)“除杂4”发生反应的离子方程式有
(3)“操作X”为
(4)查阅资料:难溶电解质的溶解度会受到溶液中其它离子的影响。加入与难溶电解质相同离子的电解质,因“同离子效应”溶解度降低;加入与难溶电解质不同离子的电解质,因“盐效应”溶解度增大。
①提出假设:
| 依据 | 假设 | |
| 假设1 | 实验1和2中 检测时出现少量浑浊 检测时出现少量浑浊 |  溶解度 溶解度 |
| 假设2 | 实验3中 检出量明显高于1和2 检出量明显高于1和2 | NaOH能明显增大 溶解度 溶解度 |
| 假设3 | NaOH或 能明显增大 能明显增大 溶解度 溶解度 |
| 探究1 | 探究2 | 探究3 | 探究4 | |
| 实验流程 | 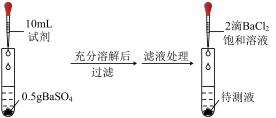 | |||
| 试剂 | 饱和食盐水 | 2 NaOH溶液 NaOH溶液 | 0.5  溶液 溶液 | 蒸馏水 |
| 现象 | 少量浑浊 | 大量沉淀 | 大量沉淀 | 无明显现象 |
③实验分析:实验3中
 溶液的用量为理论值的1.5倍,最后仍检出
溶液的用量为理论值的1.5倍,最后仍检出 的原因是该体系中“同离子效应”
的原因是该体系中“同离子效应”④实验结论:粗盐提纯时,为了有效降低产品中
 含量,必须
含量,必须
您最近一年使用:0次
2022-04-02更新
|
493次组卷
|
2卷引用:福建省八地市(福州、厦门、泉州、莆田、南平、宁德、三明、龙岩)2022届高三毕业班4月诊断性联考化学试题
名校
8 . 下列化学用语对事实的表述正确的是
A.用碳酸钠溶液处理锅炉水垢:Ca2++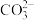  CaCO3↓ CaCO3↓ |
B.由Na和Cl形成离子键的过程: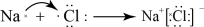 |
| C.三价铁腐蚀铜的电路板:2Fe3++3Cu=2Fe+3Cu2+ |
| D.电解饱和食盐水阳极的电极反应:2H2O+2e−=2OH−+H2↑ |
您最近一年使用:0次
2022-04-02更新
|
464次组卷
|
5卷引用:北京市石景山区2022届高三一模化学试题
北京市石景山区2022届高三一模化学试题(已下线)秘籍03 化学用语-备战2022年高考化学抢分秘籍(全国通用)广东省揭阳市普宁市华侨中学2021-2022学年高二下学期第三次月考化学试题山西省晋中市祁县中学2022-2023学年高三上学期10月月考化学试题(已下线)河北省石家庄市2022届高三毕业班教学质量检测二(一模)(选择题1-5)
解题方法
9 . 砷的化合物可用于半导体领域,如我国“天宫”空间站的核心舱“天和号”就是采用砷化镓薄膜电池来供电。一种从酸性高浓度含砷废水[砷主要以亚砷酸( )形式存在]中回收砷的工艺流程如下:
)形式存在]中回收砷的工艺流程如下:
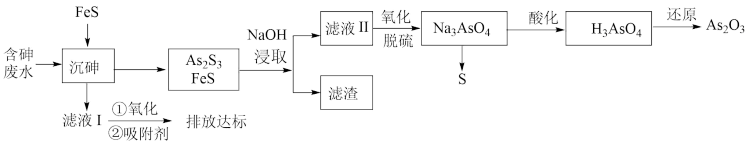
已知:
Ⅰ.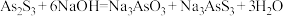
Ⅱ.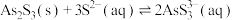
Ⅲ.砷酸( )在酸性条件下有强氧化性,能被
)在酸性条件下有强氧化性,能被 、氢碘酸等还原
、氢碘酸等还原
(1) 中砷元素的化合价为
中砷元素的化合价为___________ 价。
(2)“沉砷”过程中FeS是否可以用过量的 替换
替换___________ (填“是”或“否”);请从平衡移动的角度解释原因:___________ 。
(3)向滤液Ⅱ中通入氧气进行“氧化脱硫”,请写出脱硫的离子反应方程式___________ 。
(4)用 “还原”过程中,若需检验还原后溶液中是否仍存在砷酸。则还需要的实验试剂有
“还原”过程中,若需检验还原后溶液中是否仍存在砷酸。则还需要的实验试剂有___________ 。
(5)已知:常温下,pH>7.1时,吸附剂表面带负电,pH越大,吸附剂表面带的负电荷越多;pH<7.1时,吸附剂表面带正电,pH越小,吸附剂表面带的正电荷越多。
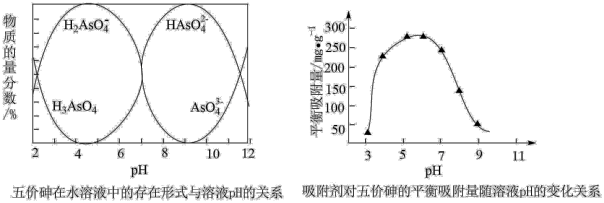
当溶液pH介于7~9,吸附剂对五价砷的平衡吸附量随pH的升高而下降,试分析其原因_____ 。
(6)含砷废水也可采用另一种化学沉降法处理:向废水中先加入适量氧化剂,再加入生石灰调节pH,将砷元素转化为 沉淀。若沉降后上层清液中
沉淀。若沉降后上层清液中 为
为 mol/L,则溶液中
mol/L,则溶液中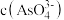 的浓度为
的浓度为_____ mol/L。该处理后的溶液是否符合国家排放标准___________ (填“是”或“否”)。(已知: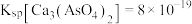 ,国家规定工业废水排放中砷元素含量<0.5mg/L)
,国家规定工业废水排放中砷元素含量<0.5mg/L)
 )形式存在]中回收砷的工艺流程如下:
)形式存在]中回收砷的工艺流程如下:
已知:
Ⅰ.
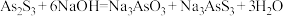
Ⅱ.
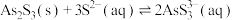
Ⅲ.砷酸(
 )在酸性条件下有强氧化性,能被
)在酸性条件下有强氧化性,能被 、氢碘酸等还原
、氢碘酸等还原(1)
 中砷元素的化合价为
中砷元素的化合价为(2)“沉砷”过程中FeS是否可以用过量的
 替换
替换(3)向滤液Ⅱ中通入氧气进行“氧化脱硫”,请写出脱硫的离子反应方程式
(4)用
 “还原”过程中,若需检验还原后溶液中是否仍存在砷酸。则还需要的实验试剂有
“还原”过程中,若需检验还原后溶液中是否仍存在砷酸。则还需要的实验试剂有(5)已知:常温下,pH>7.1时,吸附剂表面带负电,pH越大,吸附剂表面带的负电荷越多;pH<7.1时,吸附剂表面带正电,pH越小,吸附剂表面带的正电荷越多。

当溶液pH介于7~9,吸附剂对五价砷的平衡吸附量随pH的升高而下降,试分析其原因
(6)含砷废水也可采用另一种化学沉降法处理:向废水中先加入适量氧化剂,再加入生石灰调节pH,将砷元素转化为
 沉淀。若沉降后上层清液中
沉淀。若沉降后上层清液中 为
为 mol/L,则溶液中
mol/L,则溶液中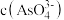 的浓度为
的浓度为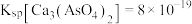 ,国家规定工业废水排放中砷元素含量<0.5mg/L)
,国家规定工业废水排放中砷元素含量<0.5mg/L)
您最近一年使用:0次
解题方法
10 . 水解反应可用于无机化合物的制备,如制备TiO2的反应:TiCl4+(x+2)H2O⇌TiO2·xH2O↓+4HCl。下列说法错误的是
A.含中子数为27的49Ti原子: | B.Cl-的结构示意图为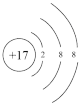 |
| C.H2O结构式为H—O—H | D.HCl电子式为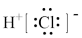 |
您最近一年使用:0次
2021-12-31更新
|
452次组卷
|
4卷引用:一轮巩固卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(北京专用)
(已下线)一轮巩固卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(北京专用)石家庄示范性高中2022届高三上学期调研考试化学试题河北省示范性高中2023届高三9月份考试化学试题云南省大理白族自治州实验中学2021-2022学年高一上学期期末考试化学试题



