名校
解题方法
1 . 下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用化学用语回答下列问题:
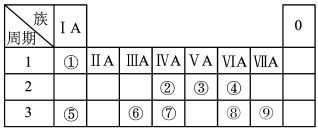
(1)画出元素⑦的原子结构示意图_____________ 。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是_______________ (填化学式)。
(3)①、④、⑤、⑨中的某些元素可形成既含离子键又含共价键的化合物,写出其中一种化合物的化学式:_______________ 。
(4)写出元素⑤形成的过氧化物的电子式__________________ ;
(5)由表中元素形成的常见物质 X、Y、Z、M、N 可发生以下反应:
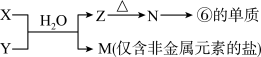
X 溶液与 Y 溶液反应的离子方程式为_____ 。

(1)画出元素⑦的原子结构示意图
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
(3)①、④、⑤、⑨中的某些元素可形成既含离子键又含共价键的化合物,写出其中一种化合物的化学式:
(4)写出元素⑤形成的过氧化物的电子式
(5)由表中元素形成的常见物质 X、Y、Z、M、N 可发生以下反应:

X 溶液与 Y 溶液反应的离子方程式为
您最近一年使用:0次
解题方法
2 . 二硫化钼(MoS2)被誉为“固体润滑剂之王”,利用低品质的辉钼矿(含MoS2、SiO2以及CuFeS2等杂质)制备高纯二硫化钼的一种生产工艺如图:
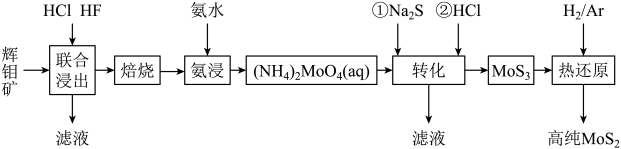
回答下列问题:
(1)(NH4)2MoO4中Mo的化合价为_____ 。
(2)“联合浸出”中HF除去的杂质化学式为_____ ,“焙烧”时MoS2转化为MoO3的化学方程式为_____ 。
(3)“转化”中加入Na2S后,(NH4)2MoO4转化为(NH4)2MoS4,写出(NH4)2MoS4与盐酸生成MoS3的离子方程式_____ 。
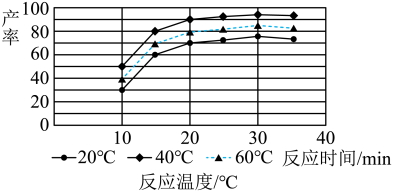
(4)由图分析产生MoS3沉淀的流程中应选择的最优温度和时间是_____ ,利用化学平衡原理分析低于或高于最优温度时,MoS3的产率均下降的原因_____ 。
(5)高纯MoS2中存在极微量非整比晶体杂质MoS2.8,则该杂质中Mo4+与Mo6+的物质的量之比为_____ 。
(6)已知Ksp(BaSO4)=1.1×10-10,Ksp(BaMoO4)=4.0×10-8,不纯的Na2MoO4溶液中若含少量可溶性硫酸盐杂质,可加入Ba(OH)2固体除去SO42-(溶液体积变化忽略),则当SO42-完全沉淀时,溶液中c(MoO42-)<_____ mol/L(保留2位有效数字)

回答下列问题:
(1)(NH4)2MoO4中Mo的化合价为
(2)“联合浸出”中HF除去的杂质化学式为
(3)“转化”中加入Na2S后,(NH4)2MoO4转化为(NH4)2MoS4,写出(NH4)2MoS4与盐酸生成MoS3的离子方程式
(4)由图分析产生MoS3沉淀的流程中应选择的最优温度和时间是

(5)高纯MoS2中存在极微量非整比晶体杂质MoS2.8,则该杂质中Mo4+与Mo6+的物质的量之比为
(6)已知Ksp(BaSO4)=1.1×10-10,Ksp(BaMoO4)=4.0×10-8,不纯的Na2MoO4溶液中若含少量可溶性硫酸盐杂质,可加入Ba(OH)2固体除去SO42-(溶液体积变化忽略),则当SO42-完全沉淀时,溶液中c(MoO42-)<
您最近一年使用:0次
名校
3 . 铍铜是广泛应用于制造高级弹性元件的良好合金。某科研小组从某旧铍铜元件(含25%BeO、71%CuS、少量FeS和SiO2)中回收铍和铜两种金属的工业流程如下:
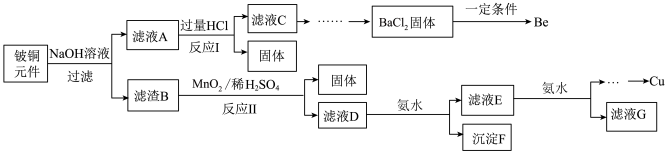
已知:i.铍、铝元素化学性质相似能形成BeO22-;ii.常温下部分难溶物的溶度积常数如下表:
(1)用NaOH溶液溶解铍铜元件步骤中提高溶解率的措施是_______ 。(至少写出两种)滤液A的主要成分除NaOH外,还有_____ (填化学式)。
(2)写出反应I中含铍化合物与过量盐酸反应的离子方程式_______ ,写出反应I中生成固体的化学方程式:________ 。
(3)滤液C中含NaCl、BeCl2和少量HCl。为提纯BeCl2,最合理的实验步骤顺序为____ (填字母)。
a.加入过量的氨水 b.通入过量的CO2 c.加入过量的NaOH
d.加入适量的HCl e.洗涤 f.过滤
(4)MnO2能将金属硫化物中的硫元素氧化为硫单质,写出反应Ⅱ中CuS发生反应的化学方程式:______ 。
(5)该小组从1kg该种旧铍铜元件中回收得到433g Cu,则该流程Cu的产率为_______ (保留三位有效数字)。

已知:i.铍、铝元素化学性质相似能形成BeO22-;ii.常温下部分难溶物的溶度积常数如下表:
| 难溶物 | Cu(OH)2 | Fe(OH)3 | Mn(OH)2 |
| 溶度积常数(Ksp) | 2.2×10-20 | 4.0×10-38 | 2.1×10-13 |
(1)用NaOH溶液溶解铍铜元件步骤中提高溶解率的措施是
(2)写出反应I中含铍化合物与过量盐酸反应的离子方程式
(3)滤液C中含NaCl、BeCl2和少量HCl。为提纯BeCl2,最合理的实验步骤顺序为
a.加入过量的氨水 b.通入过量的CO2 c.加入过量的NaOH
d.加入适量的HCl e.洗涤 f.过滤
(4)MnO2能将金属硫化物中的硫元素氧化为硫单质,写出反应Ⅱ中CuS发生反应的化学方程式:
(5)该小组从1kg该种旧铍铜元件中回收得到433g Cu,则该流程Cu的产率为
您最近一年使用:0次



