名校
解题方法
1 . 海冰是海水冻结而成的咸水冰。海水冻结时,部分来不及流走的盐分以卤汁的形式被包围在冰晶之间,形成“盐泡”(假设盐分以一个NaCl计),其大致结构如下图所示,若海冰的冰龄达到1年以上,融化后的水为淡水。下列叙述正确的是
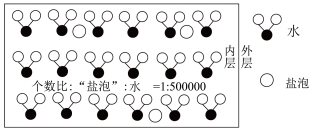

| A.海冰内层“盐泡”越多,密度越小 |
| B.海冰冰龄越长,内层的“盐泡”越少 |
| C.海冰内层“盐泡”内的盐分主要以NaCl分子的形式存在 |
| D.海冰内层NaCl的浓度约为10-4mol/L(设冰的密度为0.9g/cm3) |
您最近一年使用:0次
2020-08-20更新
|
1182次组卷
|
3卷引用:湖南省郴州市2021届高三上学期第一次质检化学试题
2 . 为测定CuSO4溶液的浓度,甲、乙两同学设计了两个方案。回答下列问题:
Ⅰ.甲方案
实验原理: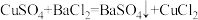
实验步骤:
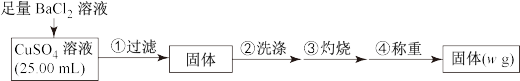
(1)判断 沉淀完全的操作为
沉淀完全的操作为____________ 。
(2)步骤②判断沉淀是否洗净所选用的试剂为_____________ 。
(3)步骤③灼烧时盛装样品的仪器名称为__________ 。
(4)固体质量为wg,则c(CuSO4)=________ mol‧L-1。
(5)若步骤①从烧杯中转移沉淀时未洗涤烧杯,则测得c(CuSO4)_________ (填“偏高”、“偏低”或“无影响”)。
Ⅱ.乙方案
实验原理: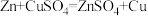 ,
,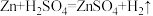
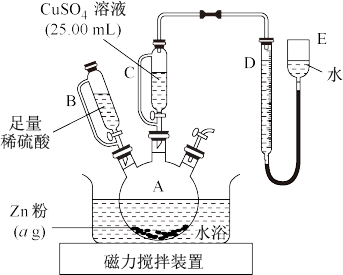
实验步骤:
①按右图安装装置(夹持仪器略去)
②……
③在仪器A、B、C、D、E…中加入图示的试剂
④调整D、E中两液面相平,使D中液面保持在0或略低于0刻度位置,读数并记录。
⑤将CuSO4溶液滴入A中搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生
⑥待体系恢复到室温,移动E管,保持D、E中两液面相平,读数并记录
⑦处理数据
(6)步骤②为___________ 。
(7)步骤⑥需保证体系恢复到室温的原因是________ (填序号)。
a.反应热受温度影响 b.气体密度受温度影响 c.反应速率受温度影响
(8)Zn粉质量为ag,若测得H2体积为bmL,已知实验条件下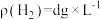 ,则c(CuSO4)
,则c(CuSO4)______ mol‧L-1(列出计算表达式)。
(9)若步骤⑥E管液面高于D管,未调液面即读数,则测得c(CuSO4)________ (填“偏高”、“偏低”或“无影响”)。
(10)是否能用同样的装置和方法测定MgSO4溶液的浓度:_________ (填“是”或“否”)。
Ⅰ.甲方案
实验原理:
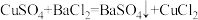
实验步骤:
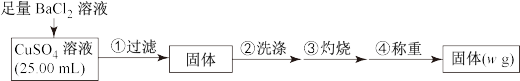
(1)判断
 沉淀完全的操作为
沉淀完全的操作为(2)步骤②判断沉淀是否洗净所选用的试剂为
(3)步骤③灼烧时盛装样品的仪器名称为
(4)固体质量为wg,则c(CuSO4)=
(5)若步骤①从烧杯中转移沉淀时未洗涤烧杯,则测得c(CuSO4)
Ⅱ.乙方案
实验原理:
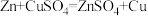 ,
,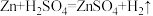

实验步骤:
①按右图安装装置(夹持仪器略去)
②……
③在仪器A、B、C、D、E…中加入图示的试剂
④调整D、E中两液面相平,使D中液面保持在0或略低于0刻度位置,读数并记录。
⑤将CuSO4溶液滴入A中搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生
⑥待体系恢复到室温,移动E管,保持D、E中两液面相平,读数并记录
⑦处理数据
(6)步骤②为
(7)步骤⑥需保证体系恢复到室温的原因是
a.反应热受温度影响 b.气体密度受温度影响 c.反应速率受温度影响
(8)Zn粉质量为ag,若测得H2体积为bmL,已知实验条件下
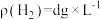 ,则c(CuSO4)
,则c(CuSO4)(9)若步骤⑥E管液面高于D管,未调液面即读数,则测得c(CuSO4)
(10)是否能用同样的装置和方法测定MgSO4溶液的浓度:
您最近一年使用:0次
2020-07-11更新
|
7828次组卷
|
28卷引用:2020年天津卷化学高考真题变式题13-16
(已下线)2020年天津卷化学高考真题变式题13-162020年天津卷化学高考试题(已下线)专题16 化学实验综合题-2020年高考真题和模拟题化学分项汇编(已下线)第29讲 化学实验方案的设计与评价-2021年高考化学一轮复习名师精讲练(已下线)专题讲座(九) 热点实验综合探究 (精讲)-2021年高考化学一轮复习讲练测(已下线)解密11 化学实验(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密11 化学实验(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)重点3 实验探究分析-2021年高考化学【热点·重点·难点】专练(新高考)(已下线)重点7 探究型实验综合题-2021年高考化学专练【热点·重点·难点】(已下线)考点31 物质的制备 定量分析-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点35 化学实验方案的设计与评价-备战2022年高考化学一轮复习考点帮(浙江专用)天津市塘沽一中2022届高三上学期毕业班开学调研考试化学试题河南省信阳高级中学2021-2022学年高一上学期12月月考化学试题(已下线)解密11 化学实验基础(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密11 化学实验(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题10 化学实验综合—2022年高考化学二轮复习讲练测(全国版)-练习四川省成都市石室中学2020-2021学年高一上学期10月阶段性测试化学试题(已下线)专题讲座(一) 化学计算的常用方法(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)考点53 化学实验方案设计与评价-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第十章 化学综合实验 第64讲 物质的检测综合实验探究(已下线)题型50 物质含量测定型综合实验(已下线)04 定量分析型综合实验 (解析)-备战2023年高考化学大题逐空突破系列(全国通用)(已下线)题型48 物质含量测定型综合实验(已下线)专题19 实验综合题(已下线)考点07 物质的量浓度(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)第17讲实验方案的设计与评价(已下线)微专题以物质含量或组成测定为主的综合实验天津市第八中学2023-2024学年高三上学期第一次大单元教学(9月月考)化学试题
名校
3 . 硫酸亚铁铵晶体[(NH4)2Fe(SO4)2·6H2O]易溶于水,在定量分析中常用来配制亚铁离子的标准溶液。某化学课外小组同学设计并完成下列实验。
I.(NH4)2Fe(SO4)2·6H2O的制取
实验步骤:
①称取4.2g碎铁屑于锥形瓶中,加入10mL30%的NaOH溶液,加热煮沸-段时间。倾去碱液,水洗至中性。
②向处理过的铁屑中加入25mL3mol/LH2SO4,水浴加热至反应完全,趁热过滤。
③向滤液中加入-定体积的饱和(NH4)2SO4溶液,加热浓缩,冷却,抽滤,洗涤,干燥得产品。
(1)步骤①中加入NaOH溶液的目的是___ 。
(2)步骤②趁热过滤的目的是___ 。
(3)步骤③加热浓缩溶液时,需要的仪器有酒精灯、___ 、___ (固定、夹持仪器除外)。
Ⅱ.(NH4)2Fe(SO4)2·6H2O和FeSO4·7H2O稳定性的对比研究
如图,在2支相同的注射器中分别装入等物质的量的两种晶体,调整2支注射器活塞使空气体积相等,用针头及胶塞封好注射器(气密性良好)。较长时间后,取出两种晶体,分别滴加2滴0.01mol/LKSCN溶液。整个过程中实验现象记录如下:

(4)判断a___ b(填“>”、“<”或“=”),出现此结果的原因可能是___ 。
(5)判断此条件下(NH4)2Fe(SO4)2·6H2O的稳定性___ (填“大于”或“小于”)FeSO4·7H2O。
Ⅲ.配制(NH4)2Fe(SO4)2溶液并标定浓度
配制(NH4)2Fe(SO4)2溶液100mL,准确量取20.00mL,置于锥形瓶中,加10mLH2SO4和邻二氮菲指示剂3~4滴,用cmol/LK2Cr2O7标准液滴定至溶液变成棕红色。消耗K2Cr2O7溶液的体积为VmL。
(6)计算(NH4)2Fe(SO4)2溶液的浓度为___ mol/L。
(7)下列操作会使所测溶液浓度偏大的是___ (填标号)。
A.锥形瓶用待测溶液润洗
B.滴定前滴定管尖嘴处有气泡,滴定后气泡消失
C.滴定过程中剧烈摇晃锥形瓶,溶液溅出
D.滴定前平视读数,滴定后俯视读数
I.(NH4)2Fe(SO4)2·6H2O的制取
实验步骤:
①称取4.2g碎铁屑于锥形瓶中,加入10mL30%的NaOH溶液,加热煮沸-段时间。倾去碱液,水洗至中性。
②向处理过的铁屑中加入25mL3mol/LH2SO4,水浴加热至反应完全,趁热过滤。
③向滤液中加入-定体积的饱和(NH4)2SO4溶液,加热浓缩,冷却,抽滤,洗涤,干燥得产品。
(1)步骤①中加入NaOH溶液的目的是
(2)步骤②趁热过滤的目的是
(3)步骤③加热浓缩溶液时,需要的仪器有酒精灯、
Ⅱ.(NH4)2Fe(SO4)2·6H2O和FeSO4·7H2O稳定性的对比研究
如图,在2支相同的注射器中分别装入等物质的量的两种晶体,调整2支注射器活塞使空气体积相等,用针头及胶塞封好注射器(气密性良好)。较长时间后,取出两种晶体,分别滴加2滴0.01mol/LKSCN溶液。整个过程中实验现象记录如下:

编号 | 活塞向右运动的距离(cm) | 滴加KSCN溶液后颜色变化 |
① | a | 较深的黄色 |
② | b | 淡淡的黄色 |
(5)判断此条件下(NH4)2Fe(SO4)2·6H2O的稳定性
Ⅲ.配制(NH4)2Fe(SO4)2溶液并标定浓度
配制(NH4)2Fe(SO4)2溶液100mL,准确量取20.00mL,置于锥形瓶中,加10mLH2SO4和邻二氮菲指示剂3~4滴,用cmol/LK2Cr2O7标准液滴定至溶液变成棕红色。消耗K2Cr2O7溶液的体积为VmL。
(6)计算(NH4)2Fe(SO4)2溶液的浓度为
(7)下列操作会使所测溶液浓度偏大的是
A.锥形瓶用待测溶液润洗
B.滴定前滴定管尖嘴处有气泡,滴定后气泡消失
C.滴定过程中剧烈摇晃锥形瓶,溶液溅出
D.滴定前平视读数,滴定后俯视读数
您最近一年使用:0次
2012·辽宁·一模
名校
4 . 已知14mol/L的H2SO4溶液的溶质质量分数为80%,那么7mol/L的H2SO4溶液的溶质质量分数将
| A.无法确定 | B.等于40% |
| C.小于40% | D.大于40% |
您最近一年使用:0次
2020-04-27更新
|
425次组卷
|
9卷引用:2013届辽宁省东北育才学校高三第一次模拟考试化学试卷
(已下线)2013届辽宁省东北育才学校高三第一次模拟考试化学试卷(已下线)2013届辽宁省东北育才学校高三第一次模拟考试化学试卷 (已下线)2013届山西省平遥中学高三上学期12月质检考试化学试卷(已下线)2015届吉林省公主岭市第一中学高三上学期第二次月考化学试卷辽宁省丹东市2017-2018学年高二下学期期末质量监测化学试题湖北省黄梅一中2019--2020学年高一下学期期中考试化学试题黑龙江省哈尔滨师范大学附属中学2022-2023学年高三9月月考化学试题辽宁省锦州市锦州中学2023届高三上学期9月月考化学试题山东省东营市胜利第一中学2023-2024学年高一下学期开学化学试题
2010·上海·二模
5 . 过碳酸钠是一种有多用途的新型氧系漂白剂,化学式可表示为aNa2CO3·bH2O2。现将一定质量的过碳酸钠粉末溶于水配成稀溶液,再向其中加入适量MnO2粉末,充分反应后生成672mL气体(标准状况)。反应后的混合物经过滤、洗涤后,将滤液和洗涤液混合并加水配成100mL溶液A。现向三份体积为10mL、浓度为c mol/L的稀硫酸中分别逐滴滴入溶液A,边滴边振荡,充分反应后,测得实验数据如下表所示:
(1)计算稀硫酸的物质的量浓度___ 。
(2)通过计算确定过碳酸钠的化学式___ 。
(3)工业上常以所含活性氧的质量分数[w(活性氧)= ×100%]来衡量过碳酸钠产品的优劣,13%以上者为优等品。现将0.2g某厂家生产的过碳酸钠样品(所含杂质不参与后面的氧化还原反应)溶于水配成溶液,加入15.0mL 1mol/L硫酸,再加入足量KI,摇匀后置于暗处,充分反应后,加入少量淀粉试液,用0.1mol/L Na2S2O3溶液滴定到蓝色恰好消失时,共消耗30.00mL,试计算判断该样品是否为优等品
×100%]来衡量过碳酸钠产品的优劣,13%以上者为优等品。现将0.2g某厂家生产的过碳酸钠样品(所含杂质不参与后面的氧化还原反应)溶于水配成溶液,加入15.0mL 1mol/L硫酸,再加入足量KI,摇匀后置于暗处,充分反应后,加入少量淀粉试液,用0.1mol/L Na2S2O3溶液滴定到蓝色恰好消失时,共消耗30.00mL,试计算判断该样品是否为优等品___ 。(已知:2Na2S2O3+I2→Na2S4O6+2NaI)
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 滴加溶液A的体积/mL | 10.0 | 20.0 | 30.0 |
| 生成气体的体积/mL(标准状况) | 89.6 | 179.2 | 224 |
(1)计算稀硫酸的物质的量浓度
(2)通过计算确定过碳酸钠的化学式
(3)工业上常以所含活性氧的质量分数[w(活性氧)=
 ×100%]来衡量过碳酸钠产品的优劣,13%以上者为优等品。现将0.2g某厂家生产的过碳酸钠样品(所含杂质不参与后面的氧化还原反应)溶于水配成溶液,加入15.0mL 1mol/L硫酸,再加入足量KI,摇匀后置于暗处,充分反应后,加入少量淀粉试液,用0.1mol/L Na2S2O3溶液滴定到蓝色恰好消失时,共消耗30.00mL,试计算判断该样品是否为优等品
×100%]来衡量过碳酸钠产品的优劣,13%以上者为优等品。现将0.2g某厂家生产的过碳酸钠样品(所含杂质不参与后面的氧化还原反应)溶于水配成溶液,加入15.0mL 1mol/L硫酸,再加入足量KI,摇匀后置于暗处,充分反应后,加入少量淀粉试液,用0.1mol/L Na2S2O3溶液滴定到蓝色恰好消失时,共消耗30.00mL,试计算判断该样品是否为优等品
您最近一年使用:0次
2010·上海宝山·二模
解题方法
6 . vmL密度为 g/cm3的某溶液中,含有相对分子质量为M的溶质m g,该溶液中溶质的质量分数为W%,物质的量浓度为cmol/L,那么下列关系式正确的是
g/cm3的某溶液中,含有相对分子质量为M的溶质m g,该溶液中溶质的质量分数为W%,物质的量浓度为cmol/L,那么下列关系式正确的是
 g/cm3的某溶液中,含有相对分子质量为M的溶质m g,该溶液中溶质的质量分数为W%,物质的量浓度为cmol/L,那么下列关系式正确的是
g/cm3的某溶液中,含有相对分子质量为M的溶质m g,该溶液中溶质的质量分数为W%,物质的量浓度为cmol/L,那么下列关系式正确的是A.c= | B.c=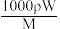 | C.W%=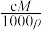 | D.m=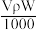 |
您最近一年使用:0次
2012·上海杨浦·二模
解题方法
7 . (1)某KClO3和KCl的混合物,钾的质量分数为43.09%,则氧的质量分数为_______ %(保留2位小数)。
(2)取KClO3和MnO2的混合物16.60g加热至恒重,将反应后的固体加15g水充分溶解,剩余固体6.55g (25℃),再加5 g水充分溶解,仍剩余固体4.80g(25℃)。
①若剩余的4.80g固体全是MnO2,则原混合物中KClO3的质量为_____ g(保留2位小数)。
②若剩余的4.80g固体是MnO2和KCl的混合物,则25℃时KCl的溶解度为__________ ;原混合物中KClO3的质量为__________ g;所得KCl溶液的密度为1.72g/cm3,则溶液的物质的量浓度为______ mol/L(保留2位小数)。
(3)可用以下反应制备KIO3和K2H3IO6(高碘酸氢二钾):
I2+2KClO3→2KIO3+Cl2 ① KIO3+Cl2+3KOH →K2H3IO6+2KCl ②
最终制得的KIO3和K2H3IO6 的物质的量之比x,若制得100molK2H3IO6, 共消耗ymol KClO3,试确定y与x的关系式_______________ 。
(4)取研细的KClO3、I2各0.02mol置于锥形瓶中,在不断摇动的情况下,慢慢加入浓盐酸,直到I2完全消失,没有黄绿色气体产生。将锥形瓶置于冰水中,有橙红色晶体A析出,剩余溶液中只检出K+和Cl-。取少量A放入试管中,发现A在常温下就会有升华现象。若将A水浴加热,产生红棕色液体B和黄绿色气体。
①试确定A的化学式。__________
②能否确定B的化学式?说明理由。__________
(2)取KClO3和MnO2的混合物16.60g加热至恒重,将反应后的固体加15g水充分溶解,剩余固体6.55g (25℃),再加5 g水充分溶解,仍剩余固体4.80g(25℃)。
①若剩余的4.80g固体全是MnO2,则原混合物中KClO3的质量为
②若剩余的4.80g固体是MnO2和KCl的混合物,则25℃时KCl的溶解度为
(3)可用以下反应制备KIO3和K2H3IO6(高碘酸氢二钾):
I2+2KClO3→2KIO3+Cl2 ① KIO3+Cl2+3KOH →K2H3IO6+2KCl ②
最终制得的KIO3和K2H3IO6 的物质的量之比x,若制得100molK2H3IO6, 共消耗ymol KClO3,试确定y与x的关系式
(4)取研细的KClO3、I2各0.02mol置于锥形瓶中,在不断摇动的情况下,慢慢加入浓盐酸,直到I2完全消失,没有黄绿色气体产生。将锥形瓶置于冰水中,有橙红色晶体A析出,剩余溶液中只检出K+和Cl-。取少量A放入试管中,发现A在常温下就会有升华现象。若将A水浴加热,产生红棕色液体B和黄绿色气体。
①试确定A的化学式。
②能否确定B的化学式?说明理由。
您最近一年使用:0次
解题方法
8 . 将5.1g镁铝合金溶于600mL0.5mol·L-1H2SO4溶液中,完全溶解后再加入1.0mol·L-1的NaOH溶液,得到沉淀的质量为13.6g,继续滴加NaOH溶液时则沉淀会减少。
(1)当加入__ mLNaOH溶液时,可使溶解在硫酸中的Mg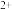 和Al
和Al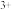 恰好完全沉淀。
恰好完全沉淀。
(2)计算合金溶于硫酸时所产生的氢气在标准状况下的体积。(列出算式)___
(1)当加入
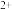 和Al
和Al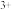 恰好完全沉淀。
恰好完全沉淀。(2)计算合金溶于硫酸时所产生的氢气在标准状况下的体积。(列出算式)
您最近一年使用:0次
名校
解题方法
9 . 相对分子质量为 M 的气态化合物 V L(标准状况),溶于 m g 水中,得到质量分数为 w、物质的量浓度为 c mol/L、密度为 ρg/mL 的溶液,下列说法正确的是
A.相对分子质量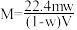 | B.物质的量浓度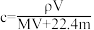 |
C.溶液的质量分数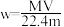 | D.溶液密度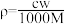 |
您最近一年使用:0次
2019-11-21更新
|
464次组卷
|
8卷引用:【校级联考】安徽省皖中名校联盟2019届高三上学期10月联考化学试题
名校
10 . 氯化亚铜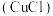 是一种白色粉末,微溶于水,不溶于乙醇、稀硝酸及稀硫酸;可溶于氯离子浓度较大的体系,形成
是一种白色粉末,微溶于水,不溶于乙醇、稀硝酸及稀硫酸;可溶于氯离子浓度较大的体系,形成 。在潮湿空气中迅速被氧化,见光则分解。右下图是实验室仿 工业制备氯化亚铜的流程进行的实验装置图。
。在潮湿空气中迅速被氧化,见光则分解。右下图是实验室仿 工业制备氯化亚铜的流程进行的实验装置图。
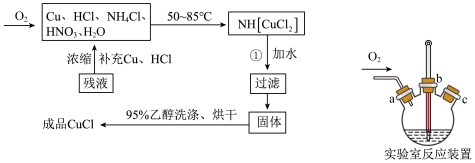
实验药品:铜丝 、氯化铵
、氯化铵 、65%硝酸
、65%硝酸 、20%盐酸
、20%盐酸 、水。
、水。
(1)质量分数为20%的盐酸密度为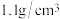 ,物质的量浓度为
,物质的量浓度为______ ;用浓盐酸配制20%盐酸需要的玻璃仪器有:______ 、烧杯、玻璃棒、胶头滴管。
(2)实验室制备 过程如下:
过程如下:
①检查装置气密性,向三颈瓶中加入铜丝、氢化铵、硝酸、盐酸,关闭 。实验开始时,温度计显示反应液温度低于室温,主要原因是
。实验开始时,温度计显示反应液温度低于室温,主要原因是______ ;
②加热至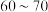 ℃,铜丝表面产生无色气泡,烧瓶上方气体颜色逐渐由无色为红棕色,气囊鼓起。打开
℃,铜丝表面产生无色气泡,烧瓶上方气体颜色逐渐由无色为红棕色,气囊鼓起。打开 ,通入氧气一段时间,将气囊变瘪,红棕色消失后关闭
,通入氧气一段时间,将气囊变瘪,红棕色消失后关闭 ,冷却至室温,制得
,冷却至室温,制得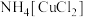 。通入氧气的目的为
。通入氧气的目的为______ ;
三颈瓶中生成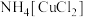 的总的离子方程为
的总的离子方程为______ ;
将液体转移至烧杯中用足量蒸馏水稀释,产生白色沉淀,过滤得氧化亚铜粗品和滤液。
③粗品用95%乙醇洗涤、烘干得氧化亚铜。
(3)便于观察和控制产生 的速率,制备氧气的装置最好运用
的速率,制备氧气的装置最好运用______ (填字母)。
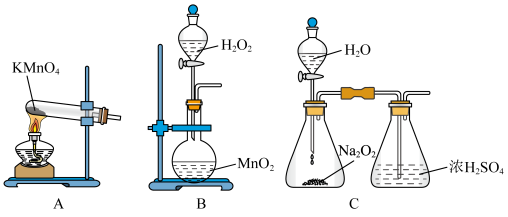
(4)下列说法不正确的是______
A.步骤Ⅰ中 可以省去,因为已经加入了
可以省去,因为已经加入了
B.步骤Ⅱ用去氧水稀释,目的是使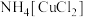 转化为
转化为 ,同时防止
,同时防止 被氧化
被氧化
C.当三颈烧瓶上方不出现红棕色气体时,可停止通入氧气
D.流程中可循环利用的物质只有氯化铵
(5)步骤Ⅲ用95%乙醇代替蒸馏水洗涤的主要目的是______ 、______ (答出两条)。
(6)氯化亚铜的定量分析:
①称取样品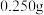 和
和 过量的
过量的 溶液于
溶液于 锥形瓶中,充分溶解;
锥形瓶中,充分溶解;
②用 硫酸[Ce(SO4)2]标准溶液测定。已知:
硫酸[Ce(SO4)2]标准溶液测定。已知:
已知:CuCl+FeCl3=CuCl2+FeCl2,Fe2++Ce4+=Fe3++Ce3+
三次平衡实验结果如下表(平衡实验结果相差不能超过1%):
则样品中 的纯度为
的纯度为______ (结果保留3位有效数字)。
误差分析:下列操作会使滴定结果偏高的是______ 。
A.锥形瓶中有少量蒸馏水 B.滴定终点读数时仰视滴定管刻度线
C.所取 溶液体积偏大 D.滴定前滴定管尖端有气泡,滴定后气泡消失
溶液体积偏大 D.滴定前滴定管尖端有气泡,滴定后气泡消失
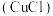 是一种白色粉末,微溶于水,不溶于乙醇、稀硝酸及稀硫酸;可溶于氯离子浓度较大的体系,形成
是一种白色粉末,微溶于水,不溶于乙醇、稀硝酸及稀硫酸;可溶于氯离子浓度较大的体系,形成 。在潮湿空气中迅速被氧化,见光则分解。右下图是实验室仿 工业制备氯化亚铜的流程进行的实验装置图。
。在潮湿空气中迅速被氧化,见光则分解。右下图是实验室仿 工业制备氯化亚铜的流程进行的实验装置图。
实验药品:铜丝
 、氯化铵
、氯化铵 、65%硝酸
、65%硝酸 、20%盐酸
、20%盐酸 、水。
、水。(1)质量分数为20%的盐酸密度为
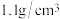 ,物质的量浓度为
,物质的量浓度为(2)实验室制备
 过程如下:
过程如下:①检查装置气密性,向三颈瓶中加入铜丝、氢化铵、硝酸、盐酸,关闭
 。实验开始时,温度计显示反应液温度低于室温,主要原因是
。实验开始时,温度计显示反应液温度低于室温,主要原因是②加热至
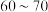 ℃,铜丝表面产生无色气泡,烧瓶上方气体颜色逐渐由无色为红棕色,气囊鼓起。打开
℃,铜丝表面产生无色气泡,烧瓶上方气体颜色逐渐由无色为红棕色,气囊鼓起。打开 ,通入氧气一段时间,将气囊变瘪,红棕色消失后关闭
,通入氧气一段时间,将气囊变瘪,红棕色消失后关闭 ,冷却至室温,制得
,冷却至室温,制得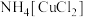 。通入氧气的目的为
。通入氧气的目的为三颈瓶中生成
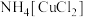 的总的离子方程为
的总的离子方程为将液体转移至烧杯中用足量蒸馏水稀释,产生白色沉淀,过滤得氧化亚铜粗品和滤液。
③粗品用95%乙醇洗涤、烘干得氧化亚铜。
(3)便于观察和控制产生
 的速率,制备氧气的装置最好运用
的速率,制备氧气的装置最好运用
(4)下列说法不正确的是
A.步骤Ⅰ中
 可以省去,因为已经加入了
可以省去,因为已经加入了
B.步骤Ⅱ用去氧水稀释,目的是使
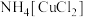 转化为
转化为 ,同时防止
,同时防止 被氧化
被氧化C.当三颈烧瓶上方不出现红棕色气体时,可停止通入氧气
D.流程中可循环利用的物质只有氯化铵
(5)步骤Ⅲ用95%乙醇代替蒸馏水洗涤的主要目的是
(6)氯化亚铜的定量分析:
①称取样品
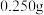 和
和 过量的
过量的 溶液于
溶液于 锥形瓶中,充分溶解;
锥形瓶中,充分溶解;②用
 硫酸[Ce(SO4)2]标准溶液测定。已知:
硫酸[Ce(SO4)2]标准溶液测定。已知:已知:CuCl+FeCl3=CuCl2+FeCl2,Fe2++Ce4+=Fe3++Ce3+
三次平衡实验结果如下表(平衡实验结果相差不能超过1%):
| 平衡实验次数 | 1 | 2 | 3 |
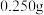 样品消耗硫酸锑标准溶液的体积 样品消耗硫酸锑标准溶液的体积 | 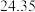 | 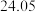 2 2 | 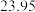 |
则样品中
 的纯度为
的纯度为误差分析:下列操作会使滴定结果偏高的是
A.锥形瓶中有少量蒸馏水 B.滴定终点读数时仰视滴定管刻度线
C.所取
 溶液体积偏大 D.滴定前滴定管尖端有气泡,滴定后气泡消失
溶液体积偏大 D.滴定前滴定管尖端有气泡,滴定后气泡消失
您最近一年使用:0次



