1 . NA代表阿伏伽德罗常数的值,下列叙述正确的是
| A.常温下1molCl2和足量氢氧化钠溶液充分反应,转移电子数目为2NA |
| B.12 g石墨烯(单层石墨)中含有六元环的个数为0.5NA |
| C.0.1molFe与稀硝酸恰好反应完后,溶液中NO3-的数目为0.3NA |
| D.l L pH=l的硫酸溶液中含有的H+数为0.2NA |
您最近一年使用:0次
2 . 为实现相关实验目的,选用的试剂、装置和操作均合理的是
| 实验目的 | 实验内容 | |
| A | 证明氨水中存在一水合氨的电离平衡 | 向含有酚酞的氨水中加入少量NaOH固体 |
| B | 配制100mL1.0 mol • L-1 NaOH 溶液 | 向100 mL容量瓶中加入4. 0 g NaOH固体,加水到刻度线 |
| C | 模拟利用牺牲阳极的阴极保护法保护铁 | 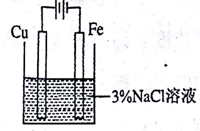 |
| D | 比较Cl-和I-的还原性 | 将少量Cl2通入滴有淀粉溶液的KI溶液中 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 硫酸高铈[Ce(SO4)2]是一种常用的强氧化剂。
(1)将Ce(SO4)2·4H2O(摩尔质量为404g/mol)在空气中加热,样品的固体残留率( )随温度的变化如图所示。
)随温度的变化如图所示。
当固体残留率为70.3%时,所得固体可能为______ (填字母)
A. Ce(SO4)2 B. Ce2(SO4)3 C. CeOSO4
(2)将一定质量的Ce(SO4)2·4H2O溶于50mL质量分数为60%、密度为1.47g/cm3的硫酸中,
再用水定容至l000mL,所得溶液中c(H+)=_______ mol/L
(3)利用Ce(SO4)2标准溶液测定FeC2O4·2H2O(摩尔质量为180g/mol)和Fe(C2O4)3·4H2O(摩尔质量为448g/mol)固体混合物中FeC2O4·2H2O含量的方法如下:
步骤l:称量1.1240g固体混合物,溶于硫酸,向溶液中加入100.00mL 0.2000mol/L的Ce(SO4)2溶液。物质转化关系如下: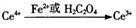
步骤2:将反应后的溶液加水稀释并定容至250.00mL,取25.00mL于锥形瓶中,滴加指示剂,用0.01000mol/LFeSO4标准溶液滴定过量的Ce4+,终点时消耗FeSO4标准溶液20.00mL。
计算固体混合物中FeC2O4·2H2O的质量分数,写出计算过程_______ 。
(1)将Ce(SO4)2·4H2O(摩尔质量为404g/mol)在空气中加热,样品的固体残留率(
 )随温度的变化如图所示。
)随温度的变化如图所示。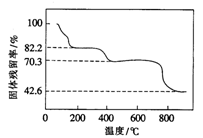
当固体残留率为70.3%时,所得固体可能为
A. Ce(SO4)2 B. Ce2(SO4)3 C. CeOSO4
(2)将一定质量的Ce(SO4)2·4H2O溶于50mL质量分数为60%、密度为1.47g/cm3的硫酸中,
再用水定容至l000mL,所得溶液中c(H+)=
(3)利用Ce(SO4)2标准溶液测定FeC2O4·2H2O(摩尔质量为180g/mol)和Fe(C2O4)3·4H2O(摩尔质量为448g/mol)固体混合物中FeC2O4·2H2O含量的方法如下:
步骤l:称量1.1240g固体混合物,溶于硫酸,向溶液中加入100.00mL 0.2000mol/L的Ce(SO4)2溶液。物质转化关系如下:
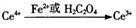
步骤2:将反应后的溶液加水稀释并定容至250.00mL,取25.00mL于锥形瓶中,滴加指示剂,用0.01000mol/LFeSO4标准溶液滴定过量的Ce4+,终点时消耗FeSO4标准溶液20.00mL。
计算固体混合物中FeC2O4·2H2O的质量分数,写出计算过程
您最近一年使用:0次
名校
4 . 碳及其化合物广泛存在于自然界中,试回答下列问题:
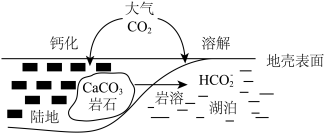
(1)某处碳循环如图所示,CaCO3转化为HCO3-的离子方程式为_____________ 。
(2)常温常压下,空气中的CO2溶于水,达到平衡时,无机碳在浓液中以4种形式存在,其转化关系如下:
①CO2(g)+H2O H2CO3 K=10-2.8
H2CO3 K=10-2.8
②H2CO3 H++HCO3- K1=10-3.5,
H++HCO3- K1=10-3.5,
③HCO3- H++CO32- K2=10-10.3,
H++CO32- K2=10-10.3,
若溶液中。c(CO2)=1.0×10-5mol/L,且忽略水的电离及H2CO3的第二级电离,则溶液pH=_____ 。
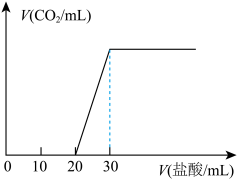
(3)某化学小组为了测量湖水中无机碳的含量,量取 100mL湖水,酸化后用N2吹出CO2,再用NaOH溶液吸收,将吸收液用0.10mol/L盐酸滴定,生成的V(CO2)随V (盐酸)变化关系如图所示,则吸收液中离子浓度由大到小的顺序为______________ (不用写出H+),湖水中无机碳的浓度为_______ mol/L。
(4)—定条件下,CO2和H2O可以转化为CO和H2,通过反应:CO(g)+2H2(g) CH3OH(g)制备甲醇,若起始时在密闭容器中按物质的量之比1:2充入CO和H2,测得平衡时CO转化率a (CO)随T、P的变化关系如图所示。
CH3OH(g)制备甲醇,若起始时在密闭容器中按物质的量之比1:2充入CO和H2,测得平衡时CO转化率a (CO)随T、P的变化关系如图所示。
①P1______ P2(填“大于”、“小于”或“等于”);
②该反应在195℃、P2条件下达到平衡后,c(H2)=0.5 mol/L ,则该反应的平衡常数为______ 。
③已知CH3OH和CO的燃烧热分别725.8kJ/mol、283.0 kJ/mol,1mol液态水变成气态水吸热44.0kJ,写出甲醇不完全燃烧生成一氧化碳和气态水的热化学方程式:_______ 。
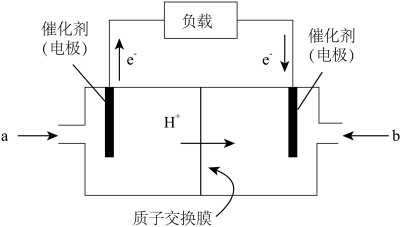
(5)用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图,则c电极的反应方程式为:__________ 。
(1)某处碳循环如图所示,CaCO3转化为HCO3-的离子方程式为
(2)常温常压下,空气中的CO2溶于水,达到平衡时,无机碳在浓液中以4种形式存在,其转化关系如下:
①CO2(g)+H2O
 H2CO3 K=10-2.8
H2CO3 K=10-2.8②H2CO3
 H++HCO3- K1=10-3.5,
H++HCO3- K1=10-3.5,③HCO3-
 H++CO32- K2=10-10.3,
H++CO32- K2=10-10.3,若溶液中。c(CO2)=1.0×10-5mol/L,且忽略水的电离及H2CO3的第二级电离,则溶液pH=
(3)某化学小组为了测量湖水中无机碳的含量,量取 100mL湖水,酸化后用N2吹出CO2,再用NaOH溶液吸收,将吸收液用0.10mol/L盐酸滴定,生成的V(CO2)随V (盐酸)变化关系如图所示,则吸收液中离子浓度由大到小的顺序为
(4)—定条件下,CO2和H2O可以转化为CO和H2,通过反应:CO(g)+2H2(g)
 CH3OH(g)制备甲醇,若起始时在密闭容器中按物质的量之比1:2充入CO和H2,测得平衡时CO转化率a (CO)随T、P的变化关系如图所示。
CH3OH(g)制备甲醇,若起始时在密闭容器中按物质的量之比1:2充入CO和H2,测得平衡时CO转化率a (CO)随T、P的变化关系如图所示。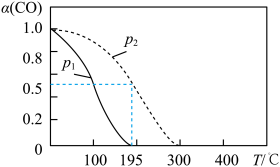
①P1
②该反应在195℃、P2条件下达到平衡后,c(H2)=0.5 mol/L ,则该反应的平衡常数为
③已知CH3OH和CO的燃烧热分别725.8kJ/mol、283.0 kJ/mol,1mol液态水变成气态水吸热44.0kJ,写出甲醇不完全燃烧生成一氧化碳和气态水的热化学方程式:
(5)用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图,则c电极的反应方程式为:
您最近一年使用:0次
2017-04-18更新
|
1023次组卷
|
3卷引用:2017届江西省宜春市高三第二次模拟考试化学试卷
解题方法
5 . 用11.92gNaClO配成100mL溶液,向其中加入0.01mol Na2Sx恰好完全反应,生成Na2SO4和NaCl。
(1)NaClO溶液的物质的量浓度_________ mol·L-1。
(2)化学式Na2Sx中的X=____________ 。
(1)NaClO溶液的物质的量浓度
(2)化学式Na2Sx中的X=
您最近一年使用:0次
2017-04-03更新
|
1572次组卷
|
7卷引用:2017届浙江省绍兴市高三3月教学质量调测考试化学试卷2
6 . 如图为实验室某浓盐酸试剂瓶标签上的有关数据,根据有关数据回答下列问题:
(1)该浓盐酸中HCl的物质的量浓度为_______ mol/L.
(2)取用任意体积的该盐酸溶液时,下列物理量不随所取体积多少而变化的_________ .
A、溶液中H+的物质的量浓度 B、溶液中HCl的质量
C、溶液中H+的数目 D、溶液的密度
(3)若现有1L 1mol/L的稀盐酸,欲使其浓度增大1倍,采取的措施最合理的是____________ .
A、通入标况下HCl气体22.4L
B、将溶液加热浓缩至0.5L
C、往原溶液加入5mol/L盐酸0.6L,再稀释至2L
D、往原溶液加入1L 3mol/L盐酸混合均匀.
| 盐酸 分子式:HCl 相对分子质量:36.5 密度:1.19g/cm3 质量分数:36.5% |
(1)该浓盐酸中HCl的物质的量浓度为
(2)取用任意体积的该盐酸溶液时,下列物理量不随所取体积多少而变化的
A、溶液中H+的物质的量浓度 B、溶液中HCl的质量
C、溶液中H+的数目 D、溶液的密度
(3)若现有1L 1mol/L的稀盐酸,欲使其浓度增大1倍,采取的措施最合理的是
A、通入标况下HCl气体22.4L
B、将溶液加热浓缩至0.5L
C、往原溶液加入5mol/L盐酸0.6L,再稀释至2L
D、往原溶液加入1L 3mol/L盐酸混合均匀.
您最近一年使用:0次
2017-03-20更新
|
848次组卷
|
2卷引用:2017届浙江省温州中学高三3月高考模拟化学试卷
7 . 左图是某同学在实验室中进行铝热反应(铝过量)的实验装置,实验中可观察到的现象之一为“纸漏斗的下部被烧穿,有熔融物落入沙中”。
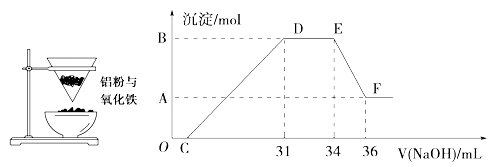
(1)试剂A的名称是___________________ 。
(2)探究铝热反应后固体的性质:将反应后容器中的残余固体置于烧杯中,加入100mL稀硝酸,固体完全溶解,(假设固体全部溶解后溶液体积不变),反应过程中无气体放出(活泼金属可把稀 HNO3还原为NH4NO3)。向反应后的溶液中缓慢滴加4 mol·L-1的NaOH溶液,产生沉淀的物质的量与加入 NaOH溶液 的体积的关系如上右图所示:
①写出DE段发生反应的离子方程式:___________________________
②求c(HNO3)=_________________ ③B与A的差值为_________________
(3)若铝和氧化铁能恰好完全反应。则该铝热剂与盐酸反应时转移电子与所耗H+的物质的量之比_______

(1)试剂A的名称是
(2)探究铝热反应后固体的性质:将反应后容器中的残余固体置于烧杯中,加入100mL稀硝酸,固体完全溶解,(假设固体全部溶解后溶液体积不变),反应过程中无气体放出(活泼金属可把稀 HNO3还原为NH4NO3)。向反应后的溶液中缓慢滴加4 mol·L-1的NaOH溶液,产生沉淀的物质的量与加入 NaOH溶液 的体积的关系如上右图所示:
①写出DE段发生反应的离子方程式:
②求c(HNO3)=
(3)若铝和氧化铁能恰好完全反应。则该铝热剂与盐酸反应时转移电子与所耗H+的物质的量之比
您最近一年使用:0次
2016-12-09更新
|
341次组卷
|
2卷引用:2016届江西省余江县第一中学高三上学期二次模拟化学试卷
解题方法
8 . 自然界中,金属硫化物矿床常因发生表生氧化及次生富集作用,产生辉铜矿(Cu2S)与铜蓝(CuS)。
已知:Cu2S、CuS是两种不溶于水的黑色固体,在一定条件下都能与稀HNO3反应:
①3CuS+8H++8NO3-→3Cu2++3SO42-+8NO↑+4H2O
②3Cu2S+16H++10NO3-→6Cu2++3SO42-+10NO↑+8H2O
现将四份质量不同的某Cu2S和CuS混合物样品分别与100mL 5mol/L的稀硝酸充分反应,样品质量与产生气体的体积(已折合成标准状况)如下表所示:
试回答下列问题(不考虑硝酸的挥发以及溶液体积变化):
53.用质量分数为0.63、密度为1.42g/cm3的浓硝酸配置100mL、5mol/L的稀硝酸,需浓硝酸的体积为_____________ 。(保留1位小数)
54.甲实验结束后,溶液中c(NO3-) =__________________ 。
55.混合物样品中Cu2S、CuS的物质的量之比是多少?_______ (写出计算过程)
56.乙实验结束后,溶液中氢离子的浓度是多少?________ (写出计算过程)
57.计算丙实验中产生气体的体积(V)。________ (写出计算过程)
已知:Cu2S、CuS是两种不溶于水的黑色固体,在一定条件下都能与稀HNO3反应:
①3CuS+8H++8NO3-→3Cu2++3SO42-+8NO↑+4H2O
②3Cu2S+16H++10NO3-→6Cu2++3SO42-+10NO↑+8H2O
现将四份质量不同的某Cu2S和CuS混合物样品分别与100mL 5mol/L的稀硝酸充分反应,样品质量与产生气体的体积(已折合成标准状况)如下表所示:
| 实验编号 | 甲 | 乙 | 丙 |
| 样品质量(g) | 9.6 | 12.8 | 64.0 |
| 气体体积(L) | 5.04 | 6.72 | V |
试回答下列问题(不考虑硝酸的挥发以及溶液体积变化):
53.用质量分数为0.63、密度为1.42g/cm3的浓硝酸配置100mL、5mol/L的稀硝酸,需浓硝酸的体积为
54.甲实验结束后,溶液中c(NO3-) =
55.混合物样品中Cu2S、CuS的物质的量之比是多少?
56.乙实验结束后,溶液中氢离子的浓度是多少?
57.计算丙实验中产生气体的体积(V)。
您最近一年使用:0次
2011·北京丰台·一模
9 . 高纯六水氯化锶(SrCl2·6H2O)可用于制造高档磁性材料、电解金属钠的助熔剂、高档颜料和液晶玻璃等,具有很高的经济价值。高纯六水氯化锶的制备过程如下:
Ⅰ.将纯水加入烧杯内,搅拌下加入适量工业碳酸锶粉末(含少量Ba、Fe的化合物),制成浆料。
Ⅱ.缓慢加入工业盐酸进行酸化,将固体物质溶解。
Ⅲ.然后喷淋加入适量的硫酸,再加入质量分数为30%的双氧水少许。
Ⅳ.调节pH至8~10, 加热至60~70℃,搅拌1h,过滤,除去残渣。
Ⅴ.滤液加热至沸,继续浓缩至氯化锶质量浓度(溶质质量与溶液体积之比)为 x g/L。
请回答:
(1)用电子式表示HCl的形成过程_____ 。
(2)已知Sr为第五周期第ⅡA族元素,则不符合Sr>Ca的是_____ (填序号)。
①原子半径 ②最外层电子数
③金属性 ④最高价氧化物对应的水化物的碱性
(3)写出步骤Ⅱ中加入盐酸时发生反应的离子方程式:_____ 。
(4)加入硫酸后会先生成硫酸锶沉淀,进而转化为硫酸钡沉淀,试分析原理_____ 。
(5)步骤Ⅲ中在酸性环境下加入双氧水是为将亚铁离子氧化成铁离子,写出该反应的离子方程式:_____ 。
(6)步骤Ⅳ中调节pH至8~10,最好选用的试剂为_____ 。
(7)已知某次实验得到浓缩后的氯化锶溶液中溶质为818g,溶剂为1000 g,经测定该溶液的密度为1.5 g/mL,则该溶液溶质的质量浓度x为_____ g/L(计算结果保留整数)。
Ⅰ.将纯水加入烧杯内,搅拌下加入适量工业碳酸锶粉末(含少量Ba、Fe的化合物),制成浆料。
Ⅱ.缓慢加入工业盐酸进行酸化,将固体物质溶解。
Ⅲ.然后喷淋加入适量的硫酸,再加入质量分数为30%的双氧水少许。
Ⅳ.调节pH至8~10, 加热至60~70℃,搅拌1h,过滤,除去残渣。
Ⅴ.滤液加热至沸,继续浓缩至氯化锶质量浓度(溶质质量与溶液体积之比)为 x g/L。
请回答:
(1)用电子式表示HCl的形成过程
(2)已知Sr为第五周期第ⅡA族元素,则不符合Sr>Ca的是
①原子半径 ②最外层电子数
③金属性 ④最高价氧化物对应的水化物的碱性
(3)写出步骤Ⅱ中加入盐酸时发生反应的离子方程式:
(4)加入硫酸后会先生成硫酸锶沉淀,进而转化为硫酸钡沉淀,试分析原理
(5)步骤Ⅲ中在酸性环境下加入双氧水是为将亚铁离子氧化成铁离子,写出该反应的离子方程式:
(6)步骤Ⅳ中调节pH至8~10,最好选用的试剂为
(7)已知某次实验得到浓缩后的氯化锶溶液中溶质为818g,溶剂为1000 g,经测定该溶液的密度为1.5 g/mL,则该溶液溶质的质量浓度x为
您最近一年使用:0次
10 . 标准状况下VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,质量分数为ω,物质浓度为c mol/L,则下列关系中不正确的是
A.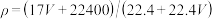 |
B.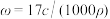 |
C.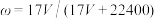 |
D. =1000Vρ/(17V+22400) =1000Vρ/(17V+22400) |
您最近一年使用:0次
2016-12-09更新
|
4951次组卷
|
131卷引用:江西省新余市第一中学2018届高三毕业年级第二次模拟考试化学试题
江西省新余市第一中学2018届高三毕业年级第二次模拟考试化学试题安徽省肥东县高级中学2019届高三上学期8月调研考试化学试题【全国百强校】甘肃省平凉市静宁县第一中学2019届高三上学期第三次模拟考试化学试题辽宁省沈阳市东北育才学校2020届高三上学期第一次模拟考试化学试题2010年普通高等学校招生全国统一考试理综化学部分(四川卷)2010年高考化学试题分项专题三 物质的量2010年高考化学试题分项专题十四 化学计算(已下线)2010年重庆一中高一下学期期末考试化学试题(已下线)2010年四川省成都七中高一上学期期中考试化学试卷(已下线)2010—2011学年黑龙江省哈六中高一上学期期末考试化学试卷(已下线)2010—2011学年辽宁省营口市高一上学期期末考试化学试卷(已下线)2011-2012学年浙江省嘉兴一中高一10月份月考化学试卷(已下线)2011-2012年辽宁省开原高中高一上学期第一次考试化学试卷(已下线)2011-2012学年浙江省嘉兴一中高二上学期期中考试化学试卷(已下线)2011-2012学年湖北省黄冈中学高一上学期期中考试化学试卷(已下线)2011-2012学年海南省琼海市嘉积中学高一上学期教学质量检测化学试卷(已下线)2011-2012学年甘肃省兰州市兰炼一中高一上学期期中考试化学试卷(已下线)2011-2012学年四川省成都市树德协进中学高一上学期期中考试化学试卷(已下线)2012-2013学年河北省石家庄市第二实验中学高一上学期期中考化学卷(已下线)2015届广西桂林市第十八中学高三上学期第一次月考化学试卷(已下线)2014-2015学年浙江嘉兴第一中学高一10月月考化学试卷2016届山东省枣庄市第二中学高三9月阶段性学情检测化学试题2016届广西桂林市第十八中学高三第一次月考化学试卷2015-2016学年山西大学附属中学高一上学期第一次月考化学试卷2015-2016学年广东省普宁一中高一上学期第三次月考化学试卷2015-2016学年四川省双流中学高一下入学考试化学试卷2015-2016学年广西桂林十八中高二下开学测化学试卷2015-2016学年河北省保定市高一上学期期末化学试卷2016-2017学年河北省邯郸一中高一上入学考试化学试卷2016-2017学年黑龙江牡丹江高级中学高一9月月考化学卷2017届湖北省大冶一中高三上学期8月月考化学试卷2017届福建省南安一中高三暑假阶段性考试化学试卷2016-2017学年宁夏育才中学高一上第一次月考化学试卷2016-2017学年河南省南阳一中高一上第一次月考化学卷2016-2017学年河北省定州二中高一上10月月考化学试卷2017届陕西省师范大学附属中学高三上学期第二次模考化学试卷山西省怀仁县第一中学(两校区)2016-2017学年高二下学期期末考试化学试题2018版化学(苏教版)高考总复习专题一对接高考精练--物质的量浓度及其溶液的配制山西省忻州市第一中学2016-2017学年高一必修一:第1章从实验学化学同步练习化学试题河南省南阳市第一中学2018届高三上学期第二次考试化学试题江西省崇义中学2017-2018学年高一上学期第一次月考化学试题湖南省长沙市实验中学2017-2018学年高一上学期第一次月考化学试题湖南省长沙市第一中学2017-2018学年高一上学期第一次阶段性检测化学试题黑龙江省哈尔滨市第三中学2017-2018学年高一上学期第一次验收考试化学试题新疆阿克苏市农一师中学2017-2018学年高一上学期第一次月考化学试题河南省周口市郸城县第一高级中学2017-2018学年高一10月月考化学试题河南省商丘市第一高级中学2017-2018学年高一上学期第一次月考化学试题天津市静海县第一中学2018届高三9月学生学业能力调研考试化学试题河南省中原名校(即豫南九校)2017-2018学年高一上学期期中联考化学试题安徽省定远重点中学2017-2018学年高一上学期期末考试化学试题陕西省西安市第一中学2017-2018学年高一上学期期末考试化学试题湖北省黄冈中学2017-2018学年高一上学期第一次月考化学试题【全国百强校】江西省新余市第一中学2017-2018学年高二下学期第三次段考化学试题【全国百强校】内蒙古集宁一中(东校区)2017-2018学年高二下学期期末考试化学试题黑龙江省青冈县一中2017-2018学年高二下学期期末考试化学试题(已下线)解密02 化学常用计量——备战2018年高考化学之高频考点解密(已下线)学科网2019年高考化学一轮复习讲练测1.2 物质的量浓度 测2018--2019高中化学《物质的量浓度》专项训练题【全国百强校】新疆维吾尔自治区乌鲁木齐市第一中学2019届高三上学期第一次月考(9月)化学试题湖南省岳阳县第一中学、汨罗市一中2018-2019学年高一上学期10月联考化学试题河南省豫西名校2018-2019学年高一上学期第一次联考化学试题湖南省长沙市周南梅溪湖中学2018-2019学年高一下学期一模检测化学试题河南省永城高中2018-2019学年高一上学期第一次月考化学试题【全国百强校】山西省太原市第五中学2018-2019学年高一上学期10月月考化学试题【全国百强校】山西省山西大学附属中学2018-2019学年高一上学期10月模块诊断化学试题【全国百强校】辽宁省实验中学2018-2019学年高一上学期期中考试化学试题安徽省阜阳市第三中学2018-2019学年高一上学期小期末考试(期末模拟)化学试题【全国百强校】内蒙古自治区乌兰察布市集宁区第一中学2018-2019学年高一上学期期末考试化学试题河北省大名县第一中学2018-2019学年高二(普通班)5月月考化学试题【全国百强校】吉林省延边第二中学2018-2019学年高二下学期第二次月考化学试题贵州省铜仁第一中学2018-2019学年高二下学期期末考试化学试题(已下线)专题1.2 物质的量浓度(讲)-《2020年高考一轮复习讲练测》吉林省乾安县七中2017-2018学年高一上学期期中考试化学试卷河北省秦皇岛一中2019-2020学年高一上学期第一次月考化学试题黑龙江省鹤岗市第一中学2019-2020学年高一第一次月考化学试题河南省林州市第一中学2019-2020学年高一10月月考化学试题安徽省六安市舒城中学2019-2020学年高一上学期第一次月考化学试题2020届高三化学一轮复习 基本概念物质的量(过关检测)山西运城市康杰中学2019-2020学年高一上学期期中考试化学试题四川省遂宁市第二中学2019-2020学年高一上学期期中考试化学试题宁夏回族自治区石嘴山市第三中学2019-2020学年高一上学期期中考试化学试题内蒙古翁牛特旗乌丹第一中学2019-2020学年高一上学期期中考试化学试题山西省朔州市怀仁县第一中学2018-2019学年高一上学期第三次月考化学试题2020届高三化学化学二轮复习——高考常考题:质量分数、物质的量浓度的相关计算【精编25题】广西壮族自治区来宾市金秀县民族中学2019-2020学年高一上学期期末考试化学试题内蒙古包钢第一中学2019-2020学年高一上学期10月月考化学试题广西壮族自治区来宾市忻城县民族中学2019-2020学年高一上学期期末考试化学试题黑龙江省哈尔滨市第一中学2019-2020 学年高二下学期期末考试化学试题(已下线)2.2.2化学反应的计算 练习(2)——《高中新教材同步备课》(苏教版 必修第一册)(已下线)第1单元 化学计量在实验中的应用(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷鲁科版(2019)高一必修第一册第1章 认识化学科学 总结检测高一必修第一册(鲁科2019)第1章第3节 化学中常用的物理量——物质的量广东省深圳市外国语学校2021届高三第一次月考化学试题陕西省渭南高级中学2019-2020学年高一上学期第一次月考化学试题山西大学附属中学2020-2021学年高上学期10月月考化学试题四川省成都外国语学校2020-2021学年高一上学期10月月考化学试题甘肃省天水市第一中学2020-2021学年高一上学期第一学段考试化学试题(已下线)【新东方】【2019】【高一上】【期中考】【JEZ】【化学】【栾子豪制作】(已下线)【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高二6月阶段性测试化学试题山西省太原市山西大学附属中学2020-2021学年高一上学期10月(总第一次)模块诊断化学试题四川省遂宁市射洪中学校2020-2021学年高一上学期第一次月考化学试题甘肃省临夏中学2020-2021学年高一上学期期中考试化学试题江西省上饶市横峰中学2020-2021学年高一上学期期中考试化学试题内蒙古自治区赤峰市第二实验中学2020-2021学年高一上学期10月月考化学试题四川省广元市川师大万达中学2020-2021学年高一上学期期中考试化学试题甘肃省天水市第三中学2020-2021学年高一上学期期中考试化学试题(已下线)【浙江新东方】绍兴qw72江西省南昌市八一中学、洪都中学等七校2020-2021学年高一上学期期末联考化学试题(已下线)专题03 溶液——备战2021年高考化学纠错笔记黑龙江省鹤岗市第一中学2020-2021学年高二下学期期中考试化学试题(已下线)专题02 物质的量在化学实验中的应用(热点讲义)-2022届高考化学一轮复习热点题型归纳与变式训练(已下线)课时12 物质的量浓度与溶液的配制-2022年高考化学一轮复习小题多维练(全国通用)四川省遂宁市射洪中学2021-2022学年高一上学期第一次月考化学试题山东省济南市商河县第三中学2022届高三10月月考化学试题广东省湛江市第二十一中学2022届高三9月第二次月考化学试题上海实验高中2021-2022学年高一上学期第一次测试化学试题辽宁省实验中学分校2017-2018学年高一上学期期中考试化学试题北京市第二十中学2021-2022学年高一上学期期中考试化学试题上海市黄浦区大同中学2021-2022学年高一上学期期中考试化学试题上海外国语大学附属外国语学校松江云间中学2021-2022学年高一上学期10月测试化学试题黑龙江省大庆中学2021-2022学年高一上学期期末考试化学试题北京市汇文中学2021-2022学年高一上学期期末考试化学试卷(已下线)第02讲 物质的量浓度与溶液的配制(练)-2023年高考化学一轮复习讲练测(全国通用)黑龙江省哈尔滨师范大学附属中学2021-2022学年高一下学期期末考试化学试题(已下线)2.2.2 物质的量浓度相关计算(好题帮)-备战2023年高考化学一轮复习考点帮(新教材新高考)黑龙江省齐齐哈尔市八校联合体2022-2023学年高三上学期期中考试化学试题黑龙江省实验中学2022-2023学年高一上学期期中测试化学试题上海市浦东新区上海中学东校2022-2023学年高一上学期第一次阶段性素质评估化学试题上海市实验学校2021-2022学年高一上学期第一次测试化学试题甘肃省兰州第一中学2023-2024学年高一上学期12月月考化学试题(已下线)第02讲 物质的量浓度(讲义)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)



