1 . 回答下列问题。
(1)等质量的CO和 ,物质的量之比为
,物质的量之比为___________ ;氧原子个数之比为___________ ;
(2) 个氨分子含
个氨分子含___________ 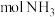 ,
,___________ g氮原子,___________ mol电子。
(3)含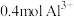 的
的 中所含的
中所含的 的质量是
的质量是___________ 。
(4)已知16g A和20g B恰好完全反应,生成0.04mol C和31.76g D,则C的摩尔质量为___________ 。
(1)等质量的CO和
 ,物质的量之比为
,物质的量之比为(2)
 个氨分子含
个氨分子含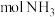 ,
,(3)含
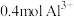 的
的 中所含的
中所含的 的质量是
的质量是(4)已知16g A和20g B恰好完全反应,生成0.04mol C和31.76g D,则C的摩尔质量为
您最近一年使用:0次
2 . 计算填空:
(1)标况下33.6L CO2中含________ mol碳原子________ 个氧原子(用NA表示阿伏加德罗常数的值),质量是________ g。
(2)有以下4种物质:①8g氢气②1.204×1024个氮气分子③22g二氧化碳④18ml水它们所含分子数最多的是____ ,原子数最多的是___ ,质量最大的是____ ,电子数最大的是____ 。
(1)标况下33.6L CO2中含
(2)有以下4种物质:①8g氢气②1.204×1024个氮气分子③22g二氧化碳④18ml水它们所含分子数最多的是
您最近一年使用:0次
3 . 倍半硅氧烷在液晶显示、塑料阻燃、生物医用等领域具有重要应用,氢基倍半硅氧烷的分子结构如图A所示,其加热分解产物中SiO2的晶胞结构如图B所示。回答下列问题:
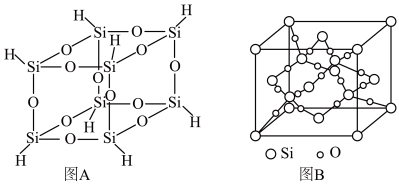
(1)基态Si原子的核外电子排布式为_______ ,其中每对成对电子之间的区别是_______ 。
(2)图A分子结构中,一个硅原子被3个_______ 元环共用,该分子的分子式为_______ 。
(3)图A分子结构中H元素的化合价为_______ ,O原子采用_______ 杂化,形成的极性共价键类型为(电子云重叠方式)_______ ;键的极性:Si-O键_______ Si-H键(填“>”“<”或“=”)。
(4)氢基倍半硅氧烷为_______ 晶体,SiO2为_______ 晶体。
(5)每个SiO2晶胞中含有O原子的个数为_______ ;已知SiO2晶体为面心立方结构,晶胞参数为anm,阿伏加德罗常数的值为NA,则SiO2晶体的密度为_______ g•cm-3。

(1)基态Si原子的核外电子排布式为
(2)图A分子结构中,一个硅原子被3个
(3)图A分子结构中H元素的化合价为
(4)氢基倍半硅氧烷为
(5)每个SiO2晶胞中含有O原子的个数为
您最近一年使用:0次
4 . 某同学设计实验确定CaC2O4•xH2O的结晶水数目。称取样品9.84g,经热分解测得气体产物中有CO、CO2、H2O,其中H2O的质量为2.16g;残留的固体产物是CaO和CaCO3的混合物,质量为5.34g。计算:
(1)x=____ (写出计算过程)。
(2)n(CO)=____ mol。
(1)x=
(2)n(CO)=
您最近一年使用:0次
名校
解题方法
5 . CO2的减排已经引起国际社会的广泛关注,近日我国科学家实现了CO2高选择性、高稳定性加氢合成甲醇(CH3OH)。回答下列问题:
(1)CH3OH的摩尔质量是__ g∙mol-1。
(2)2molH2O中所含原子的物质的量为__ mol。
(3)__ g的氢气中所含H原子的数目与1molCH3OH相同。
(4)含0.1NA个O的CO2中有__ 个电子,标况下该CO2的体积为__ L。
(1)CH3OH的摩尔质量是
(2)2molH2O中所含原子的物质的量为
(3)
(4)含0.1NA个O的CO2中有
您最近一年使用:0次
2020-03-14更新
|
198次组卷
|
4卷引用:福建省泉州市2019-2020学年高一上学期教学质量跟踪监测化学试题
名校
6 . (1)0.3molNH3分子中所含氢原子数与___ 个H2O分子中所含氢原子数相等。
(2)含0.4molAl3+的Al2(SO4)3中所含的SO42-的物质的量是___ 。
(3)2.3gNa中含___ mole-,在跟足量水反应中失去___ mole-。
(4)如果ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是(设NA为阿伏加 德罗常数)______ 。
(2)含0.4molAl3+的Al2(SO4)3中所含的SO42-的物质的量是
(3)2.3gNa中含
(4)如果ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是(设NA为阿伏加 德罗常数)
您最近一年使用:0次
名校
7 . (1)3.01×1023个氯气分子的物质的量是______ 。
(2)1.5 molNa2SO4·10H2O中所含的Na+的物质的量是_____ ,所含的SO42-的物质的量是_____ ,所含H2O的数目是_____ 。
(3)一定量的Na2CO3中,碳原子和氧原子的物质的量之比为______ 。
(4)0.5molNaOH中含有电子的物质的量是______ ,在____ molNa2CO3中所含Na+数目与上述0.5molNaOH所含Na+数目相等。
(2)1.5 molNa2SO4·10H2O中所含的Na+的物质的量是
(3)一定量的Na2CO3中,碳原子和氧原子的物质的量之比为
(4)0.5molNaOH中含有电子的物质的量是
您最近一年使用:0次
2019-05-20更新
|
975次组卷
|
4卷引用:步步为赢 高二化学暑假作业:作业一 化学常用计量 物质的分类和变化
步步为赢 高二化学暑假作业:作业一 化学常用计量 物质的分类和变化(已下线)1.2.1 物质的量(1)(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)第三节 物质的量 第1课时 物质的量的单位——摩尔云南省玉溪师范学院附属中学2022-2023学年高一下学期期末考试化学试题
8 . 水滑石材料在石油化学、塑料工业等方面均具有广泛用途,某活动小组同学进行如下实验制备某水滑石并测定其组成。
Ⅰ.水滑石的制备
(1)配制一定浓度的Mg(NO3)2与Al(NO3)3的混合溶液500mL,定容时,俯视刻度线,则所配溶液的浓度____________ (填“偏大”或“偏小”)。
(2)配制c(NaOH)=1.6mol/L和c(Na2CO3)=0.8mol/L的混合溶液500mL,配制时,若用托盘天平称取NaOH固体,则需称取NaOH的质量为____________ ;该混合溶液中c(Na+)=___________ mol/L。
(3)将(1)和(2)所配溶液混合后,过滤即得水滑石,过滤时玻璃棒的作用是____________ 。
Ⅱ.水滑石组成的测定
(4)设上述制得的水滑石组成为MgaAlb(OH)c(CO3)d。已知:a+b+c+d=25(a、b、c、d为正整数)。制得的样品含MgaAlb(OH)c(CO3)d0.1mol,用1mol/L的盐酸使其完全溶解,消耗盐酸的体积为1.8L;同时生成2.24L(标准状况)CO2,此时溶液中只含AlCl3和MgCl2两种溶质。通过计算确定该水滑石的化学式(请写出计算过程)____________ 。
Ⅰ.水滑石的制备
(1)配制一定浓度的Mg(NO3)2与Al(NO3)3的混合溶液500mL,定容时,俯视刻度线,则所配溶液的浓度
(2)配制c(NaOH)=1.6mol/L和c(Na2CO3)=0.8mol/L的混合溶液500mL,配制时,若用托盘天平称取NaOH固体,则需称取NaOH的质量为
(3)将(1)和(2)所配溶液混合后,过滤即得水滑石,过滤时玻璃棒的作用是
Ⅱ.水滑石组成的测定
(4)设上述制得的水滑石组成为MgaAlb(OH)c(CO3)d。已知:a+b+c+d=25(a、b、c、d为正整数)。制得的样品含MgaAlb(OH)c(CO3)d0.1mol,用1mol/L的盐酸使其完全溶解,消耗盐酸的体积为1.8L;同时生成2.24L(标准状况)CO2,此时溶液中只含AlCl3和MgCl2两种溶质。通过计算确定该水滑石的化学式(请写出计算过程)
您最近一年使用:0次
2016-12-09更新
|
189次组卷
|
2卷引用:2016届江苏省清江中学高三下学期2月月考化学试卷
2011·山西晋中·一模
9 . 含有相同原子个数的SO2和SO3,其质量比为______ ,摩尔质量比为______ ,物质的量比为______ ,其中所含氧原子个数比为______ ,硫原子个数比为______ .
您最近一年使用:0次



