名校
1 . 设 为表示阿伏加德罗常数的值,下列关于1mol HCl的说法不正确的是
为表示阿伏加德罗常数的值,下列关于1mol HCl的说法不正确的是
 为表示阿伏加德罗常数的值,下列关于1mol HCl的说法不正确的是
为表示阿伏加德罗常数的值,下列关于1mol HCl的说法不正确的是A.摩尔质量为36.5 |
B.含有的分子数为 |
| C.标准状况下,其体积约为22.4L |
D.溶于1L水中,所得溶液的物质的量浓度为1 |
您最近一年使用:0次
名校
2 . 物质的量是联系宏观和微观的桥梁:
(1) 个
个 气体分子的质量是
气体分子的质量是 ,则
,则 的摩尔质量是
的摩尔质量是_______ 。
(2) 氨气和
氨气和 二氧化碳,所含原子数
二氧化碳,所含原子数_______ (填“相等”或“不相等”)
(3)含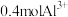 的
的 中所含的
中所含的 的个数是
的个数是_______ (用 表示),
表示), 的电离方程式是
的电离方程式是_______ 。
(4) 个
个 含
含_______ molO。
(1)
 个
个 气体分子的质量是
气体分子的质量是 ,则
,则 的摩尔质量是
的摩尔质量是(2)
 氨气和
氨气和 二氧化碳,所含原子数
二氧化碳,所含原子数(3)含
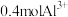 的
的 中所含的
中所含的 的个数是
的个数是 表示),
表示), 的电离方程式是
的电离方程式是(4)
 个
个 含
含
您最近一年使用:0次
名校
3 . NA是阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下22.4 L H2SO4中所含原子数为7NA |
| B.3 mol NO2与H2O完全反应时转移的电子数为2NA |
| C.11.2 LNO与11.2 LO2混合气体的分子数为NA |
| D.78 g Na2O2中含有的离子总数为3NA |
您最近一年使用:0次
2025高三·全国·专题练习
4 . 回答下列问题。
(1)某氯原子的质量是a g,12C原子的质量是b g,用NA表示阿伏加德罗常数的值。
①该氯原子的相对原子质量为___________ ;
②该氯原子的摩尔质量是___________ ;
③m g该氯原子的物质的量为___________ ;
④n g该氯原子所含的电子数为___________ 。
(2)12.4 g Na2R含Na+ 0.4 mol,则Na2R的摩尔质量为___________ ,R的相对原子质量为___________ 。含R的质量为1.6 g的Na2R,其物质的量为___________ 。
(1)某氯原子的质量是a g,12C原子的质量是b g,用NA表示阿伏加德罗常数的值。
①该氯原子的相对原子质量为
②该氯原子的摩尔质量是
③m g该氯原子的物质的量为
④n g该氯原子所含的电子数为
(2)12.4 g Na2R含Na+ 0.4 mol,则Na2R的摩尔质量为
您最近一年使用:0次
名校
5 . 设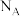 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
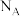 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是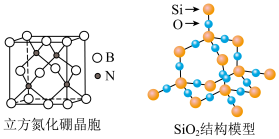
A.含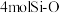 键的 键的 晶体中氧原子数目为 晶体中氧原子数目为 |
B.常温下, 的 的 溶液中 溶液中 数目为 数目为 |
C. 立方氮化硼晶体所含原子数目为 立方氮化硼晶体所含原子数目为 |
D.标准状况下,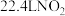 的分子数目为 的分子数目为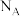 |
您最近一年使用:0次
6 . 设NA为阿伏加德罗常数的值。下列说法正确的是
| A.22.4LNO2含有的原子总数为3NA |
| B.常温下,将2.7g铝片投入浓硝酸中,转移的电子总数为0.3NA |
| C.5.6g铁粉与足量稀硫酸反应,转移的电子总数为0.3NA |
| D.11.2gN2含有的原子总数为0.8NA |
您最近一年使用:0次
7 . 回答下列问题。
(1)同温同压下,同体积的氨气和硫化氢(H2S)气体的质量之比为___________ ,密度之比为___________ 。
(2)同温同压下,同质量的氨气和硫化氢气体的体积之比为___________ ,其中含有的氢原子数目之比为___________ 。
(3)同温同压下,氨气和硫化氢气体含有的氢原子数相等,则氨气和硫化氢气体的体积之比为___________ ,电子数之比为___________ 。
(1)同温同压下,同体积的氨气和硫化氢(H2S)气体的质量之比为
(2)同温同压下,同质量的氨气和硫化氢气体的体积之比为
(3)同温同压下,氨气和硫化氢气体含有的氢原子数相等,则氨气和硫化氢气体的体积之比为
您最近一年使用:0次
名校
解题方法
8 . NA为阿伏加德罗常数的值,下列有关叙述正确的是
| A.标准状况下,11.2L氖气中所含电子数为0.5NA |
B.32g环状S8( )分子中含有的 )分子中含有的 键的数目为NA 键的数目为NA |
C.常温常压下,3.6gD2O与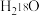 组成的体系中含有中子数2NA 组成的体系中含有中子数2NA |
D.某电池的总反应为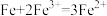 ,当有5.6gFe溶解时电路中有0.3NA电子通过 ,当有5.6gFe溶解时电路中有0.3NA电子通过 |
您最近一年使用:0次
解题方法
9 . 设 为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是
 为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是A.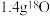 中含有的中子数目为 中含有的中子数目为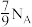 |
B.标准状况下, 溶于足量 溶于足量 溶液,所得溶液中 溶液,所得溶液中 的数目小于 的数目小于 |
C.含 的浓硫酸与足量铜共热,转移的电子数为 的浓硫酸与足量铜共热,转移的电子数为 |
D.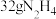 所含极性共价键的数目为 所含极性共价键的数目为 |
您最近一年使用:0次
10 . NA表示阿伏加德罗常数,下列说法正确的是
A.3molT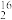 O分子中的分子总数为42NA O分子中的分子总数为42NA |
| B.氧原子总数为0.2NA的SO2和O2的混合气体,其体积为2.24L |
| C.0.1mol•L-1的Na2SO4溶液中含有Na+数目为0.2NA |
| D.7.8gNa2O2和Na2S的混合物中含有的阴离子数目为0.1NA |
您最近一年使用:0次



