名校
1 . 现有八种物质: ①铁粉 ②NH3 ③稀盐酸 ④熔融FeCl3 ⑤CH4 ⑥CaCO3固体 ⑦CuSO4溶液 ⑧Fe3O4。
(1)①-⑥属于电解质的是_______ 。
(2)写出③与⑧反应的离子方程式_______ 。将③与⑧反应后的溶液和⑦混合,再加入过量的①,反应结束后,一定没有的阳离子为_________ 。
(3)标准状况下,4.8g⑤中所含氢原子数与______ molH2O所含氢原子数相等。
(4)标准状况下,将22.4L②溶于83mL水中形成溶液的密度为0.88g/cm3,该氨水溶质的物质的量浓度为______ mol/L ,溶质的质量分数为_______ 。
(1)①-⑥属于电解质的是
(2)写出③与⑧反应的离子方程式
(3)标准状况下,4.8g⑤中所含氢原子数与
(4)标准状况下,将22.4L②溶于83mL水中形成溶液的密度为0.88g/cm3,该氨水溶质的物质的量浓度为
您最近一年使用:0次
名校
解题方法
2 . 根据要求进行计算:
(1)amolHClO4中含b个氧原子,则阿伏加德罗常数NA=_______ mol-1(用含a、b的代数式表示)。
(2)某含氯化合物X在标准状况下为气体,7.3gX在标准状况下的体积为4.48L,则X的摩尔质量是_______ 。
(3)1774年瑞典化学家舍勒发现软锰矿(主要成分是MnO2)和浓盐酸混合制氯气:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。现将92.8g含MnO2的质量分数为75%的软锰矿与足量10mol·L-1的浓盐酸完全反应(杂质不参加反应)。把反应后的溶液稀释成400mL(已知Mn的相对原子质量为55)。
MnCl2+Cl2↑+2H2O。现将92.8g含MnO2的质量分数为75%的软锰矿与足量10mol·L-1的浓盐酸完全反应(杂质不参加反应)。把反应后的溶液稀释成400mL(已知Mn的相对原子质量为55)。
①生成的氯气在标准状况下的体积是_______ 。
②稀释后溶液中MnCl2的物质的量浓度是_______ 。
(1)amolHClO4中含b个氧原子,则阿伏加德罗常数NA=
(2)某含氯化合物X在标准状况下为气体,7.3gX在标准状况下的体积为4.48L,则X的摩尔质量是
(3)1774年瑞典化学家舍勒发现软锰矿(主要成分是MnO2)和浓盐酸混合制氯气:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O。现将92.8g含MnO2的质量分数为75%的软锰矿与足量10mol·L-1的浓盐酸完全反应(杂质不参加反应)。把反应后的溶液稀释成400mL(已知Mn的相对原子质量为55)。
MnCl2+Cl2↑+2H2O。现将92.8g含MnO2的质量分数为75%的软锰矿与足量10mol·L-1的浓盐酸完全反应(杂质不参加反应)。把反应后的溶液稀释成400mL(已知Mn的相对原子质量为55)。①生成的氯气在标准状况下的体积是
②稀释后溶液中MnCl2的物质的量浓度是
您最近一年使用:0次
3 . 1774年,瑞典化学家舍勒发现软锰矿(主要成分是MnO2)和浓盐酸混合加热能制取氯气。现将23.2g含MnO2的质量分数为75%的软锰矿石与足量10mol·L-1浓盐酸完全反应(杂质不参加反应)。把反应后所得溶液稀释成200mL。
(1)参加反应的MnO2的质量为_______ 。
(2)生成的Cl2的体积(标准状况下)为_______ 。
(3)稀释后溶液中MnCl2的物质的量浓度为_______ 。
(1)参加反应的MnO2的质量为
(2)生成的Cl2的体积(标准状况下)为
(3)稀释后溶液中MnCl2的物质的量浓度为
您最近一年使用:0次
解题方法
4 . 一定质量的Na2O2投入到足量的水中,得到1L的溶液,同时生成的气体在标准状况时体积为2.24L。求:
(1)该反应转移的电子数目为_______ 。
(2)生成的NaOH物质的量浓度_______ 。
(3)参与该反应的物质Na2O2的质量_______ 。
(1)该反应转移的电子数目为
(2)生成的NaOH物质的量浓度
(3)参与该反应的物质Na2O2的质量
您最近一年使用:0次
5 . 碳酸氢钠受热易分解,某同学称取1.68g该固体充分加热,请计算:
(1)标准状况下生成气体的体积_____ 。
(2)将加热后得到的固体溶于水配成100mL溶液,求该溶液的物质的量浓度_____ 。
(1)标准状况下生成气体的体积
(2)将加热后得到的固体溶于水配成100mL溶液,求该溶液的物质的量浓度
您最近一年使用:0次
6 . 回答下列问题:
(1)氮原子的摩尔质量是_______ ;
 的质量是
的质量是_______ ,含有电子数是_______ 。
(2)标准状况下将
 气体溶于水中配成1L溶液,所得盐酸的物质的量浓度是
气体溶于水中配成1L溶液,所得盐酸的物质的量浓度是_______ 。
(3)
 分子中所含质子数与
分子中所含质子数与_______ 个 分子中所含质子数相等。
分子中所含质子数相等。
(4)有以下四种物质:①22g二氧化碳,②标准状况下,33.6L氢气,③ 个氮气分子,④4℃时18mL水。它们所含原子数最多的是
个氮气分子,④4℃时18mL水。它们所含原子数最多的是_______ (填序号),所含电子数最多的是_______ (填序号)。
(5)已知16gA和20gB恰好完全反应生成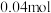 C和31.76gD,则C的摩尔质量为
C和31.76gD,则C的摩尔质量为_______ 。
(6)现有 、
、 、
、 三种物质,它们分别都含有
三种物质,它们分别都含有 氢原子,则三种物质的物质的量之比为
氢原子,则三种物质的物质的量之比为_______ 。
(1)氮原子的摩尔质量是

 的质量是
的质量是(2)标准状况下将

 气体溶于水中配成1L溶液,所得盐酸的物质的量浓度是
气体溶于水中配成1L溶液,所得盐酸的物质的量浓度是(3)

 分子中所含质子数与
分子中所含质子数与 分子中所含质子数相等。
分子中所含质子数相等。(4)有以下四种物质:①22g二氧化碳,②标准状况下,33.6L氢气,③
 个氮气分子,④4℃时18mL水。它们所含原子数最多的是
个氮气分子,④4℃时18mL水。它们所含原子数最多的是(5)已知16gA和20gB恰好完全反应生成
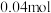 C和31.76gD,则C的摩尔质量为
C和31.76gD,则C的摩尔质量为(6)现有
 、
、 、
、 三种物质,它们分别都含有
三种物质,它们分别都含有 氢原子,则三种物质的物质的量之比为
氢原子,则三种物质的物质的量之比为
您最近一年使用:0次
7 . 2.7 g金属铝与100mL氢氧化钠溶液恰好完全反应,计算:
(1)生成标准状况下的气体体积___________ 。
(2)氢氧化钠溶液的物质的量浓度___________ 。
(1)生成标准状况下的气体体积
(2)氢氧化钠溶液的物质的量浓度
您最近一年使用:0次
解题方法
8 . 如图为某市所售盐酸试剂瓶标签上的部分数通过计算回答:

(1)该盐酸中HCl的物质的量浓度___ 。
(2)将6.5 g锌投入到足量的该盐酸中,充分反应后生成的H2在标准状况下的体积___ 。

(1)该盐酸中HCl的物质的量浓度
(2)将6.5 g锌投入到足量的该盐酸中,充分反应后生成的H2在标准状况下的体积
您最近一年使用:0次
9 . 把10.6g Na2CO3溶于水配成2L溶液,计算该溶液中Na2CO3的物质的量浓度。____
您最近一年使用:0次
名校
解题方法
10 . 请按要求完成下列各题。
(1)将2mol•L-1Al2(SO4)3和0.2mol•L-1H2SO4溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中c(SO42-)=___ mol•L-1.若用容量瓶以质量分数为98%、密度为1.84g/cm3的浓硫酸,配制480mL浓度成0.2mol•L-1稀硫酸,计算需要量取___ mL的浓硫酸。(读到小数点后一位)
(2)在标准状况下,由CO和CO2组成的混合气体6.72L,质量为12g。此混合物中CO和CO2分子数目之比是___ ,混合气体的平均摩尔质量是___ 。
(3)还原铁粉与高温水蒸气反应的化学方程式:___ 。
(4)除去Mg粉中的Al粉的试剂是___ ,反应的离子方程式为:___ 。
(1)将2mol•L-1Al2(SO4)3和0.2mol•L-1H2SO4溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中c(SO42-)=
(2)在标准状况下,由CO和CO2组成的混合气体6.72L,质量为12g。此混合物中CO和CO2分子数目之比是
(3)还原铁粉与高温水蒸气反应的化学方程式:
(4)除去Mg粉中的Al粉的试剂是
您最近一年使用:0次



