1 . Ⅰ.下表是生活生产中常见的物质,表中列出了它们的一种主要成分(其中加碘盐是氯化钠中添加适量的 ,其他成分未列出)
,其他成分未列出)
(1)请你对表中①~⑦的主要成分进行分类,是电解质的是______ ,是非电解质的是______ 。(填序号)
(2)写出④在水中的电离方程式____________ 。
(3)写出用④治疗胃酸(主要成分为盐酸)过多涉及的化学方程式:______________ 。
Ⅱ.铁的化学性质比较活泼,常温下铁可以与稀硝酸发生反应,反应的化学方程式为
(4)反应中氧化剂与还原剂的个数之比为______ ,其中 反应中显出来的性质是
反应中显出来的性质是______ 。
(5)该反应中的氧化产物为______ ,每生成11.2L(标准状况下)的NO,转移的电子个数为______ 。
 ,其他成分未列出)
,其他成分未列出)名称 | 天然气 | 白酒 | 醋酸 | 小苏打 |
主要成分 | ① | ② | ③ | ④ |
名称 | 熟石灰 | 铜线 | 加碘盐 | |
主要成分 | ⑤ | ⑥Cu | ⑦NaCl和 |
(2)写出④在水中的电离方程式
(3)写出用④治疗胃酸(主要成分为盐酸)过多涉及的化学方程式:
Ⅱ.铁的化学性质比较活泼,常温下铁可以与稀硝酸发生反应,反应的化学方程式为

(4)反应中氧化剂与还原剂的个数之比为
 反应中显出来的性质是
反应中显出来的性质是(5)该反应中的氧化产物为
您最近一年使用:0次
2 . 下列电离方程式中正确的是
A. | B. |
C.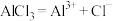 | D. |
您最近一年使用:0次
解题方法
3 . 甘肃马家窑遗址出土的青铜刀是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、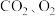 作用产生的,化学式为
作用产生的,化学式为 ,“铜绿”能跟酸反应生成铜盐、
,“铜绿”能跟酸反应生成铜盐、 和
和 。
。
(1) 属于
属于___________ (填“电解质”、“非电解质”)。
(2)从物质分类标准看,“铜绿”属于___________(填字母)。
(3)铜器表面有时会生成铜绿,这层铜绿可用化学方法除去。试写出用盐酸除去铜绿而不损伤器物的反应的离子方程式___________ 。
(4)古代人们高温灼烧孔雀石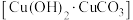 和木炭的混合物得到一种紫红色的金属铜,其化学反应式为
和木炭的混合物得到一种紫红色的金属铜,其化学反应式为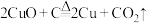 ,该反应属于___________(填序号)。
,该反应属于___________(填序号)。
(5)现代工业以黄铜矿为原料,在炼铜的过程中发生了多个反应,其中有如下两个反应: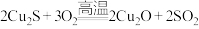 ;
; 。第一个反应中生成
。第一个反应中生成 时,转移的电子数是
时,转移的电子数是___________  ,第二个反应中氧化剂有
,第二个反应中氧化剂有___________ 。如把红色的 固体放入稀硫酸中,溶液显蓝色,反应的离子方程式为:
固体放入稀硫酸中,溶液显蓝色,反应的离子方程式为: 。请用双线桥表示该反应电子转移的方向和数目
。请用双线桥表示该反应电子转移的方向和数目___________ 。
(6)印刷电路板是电子元器件电气连接的提供者,制作印刷电路板主要原料是铜板。在制作过程中产生的铜粉,用稀硫酸和过氧化氢混合溶液溶解,可生成硫酸铜和水,其反应的离子方程式为___________ 。
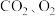 作用产生的,化学式为
作用产生的,化学式为 ,“铜绿”能跟酸反应生成铜盐、
,“铜绿”能跟酸反应生成铜盐、 和
和 。
。(1)
 属于
属于(2)从物质分类标准看,“铜绿”属于___________(填字母)。
| A.酸 | B.碱 | C.盐 | D.氧化物 |
(4)古代人们高温灼烧孔雀石
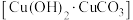 和木炭的混合物得到一种紫红色的金属铜,其化学反应式为
和木炭的混合物得到一种紫红色的金属铜,其化学反应式为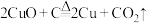 ,该反应属于___________(填序号)。
,该反应属于___________(填序号)。| A.化合反应 | B.置换反应 | C.氧化还原反应 | D.非氧化还原反应 |
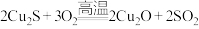 ;
; 。第一个反应中生成
。第一个反应中生成 时,转移的电子数是
时,转移的电子数是 ,第二个反应中氧化剂有
,第二个反应中氧化剂有 固体放入稀硫酸中,溶液显蓝色,反应的离子方程式为:
固体放入稀硫酸中,溶液显蓝色,反应的离子方程式为: 。请用双线桥表示该反应电子转移的方向和数目
。请用双线桥表示该反应电子转移的方向和数目(6)印刷电路板是电子元器件电气连接的提供者,制作印刷电路板主要原料是铜板。在制作过程中产生的铜粉,用稀硫酸和过氧化氢混合溶液溶解,可生成硫酸铜和水,其反应的离子方程式为
您最近一年使用:0次
解题方法
4 . 下列分类或归类正确的是
| A.液氯、氨水、干冰、碘化银均为纯净物 |
| B.明矾、水银、烧碱、碳酸钙均为电解质 |
| C.CaCl2、NaOH、HCl、IBr均为化合物 |
D.碱性氧化物: 、 、 、 、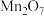 、 、 |
您最近一年使用:0次
解题方法
5 . 下列物质既不属于电解质也不属于非电解质的是
| A.烧碱 | B.食醋 | C.硫酸 | D.酒精 |
您最近一年使用:0次
名校
6 . 按要求回答下列问题:
(1)现有以下物质:①Cl2②CO2③Na2O④NaHSO4⑤漂白粉⑥NaOH溶液⑦Ba(OH)2,其中属于酸性氧化物的有
(2)某金属氯化物MClx的摩尔质量为133.5g/mol,取该金属氯化物26.7g配成水溶液,与足量AgNO3溶液完全反应,生成86.1g白色沉淀。则金属M的摩尔质量为
(3)下列是部分短周期中第二、第三周期元素的原子半径及主要化合价。
| 元素代号 | A | B | C | D | E | F | G |
原子半径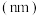 | 0.186 | 0.160 | 0.143 | 0.110 | 0.099 | 0.075 | 0.074 |
| 主要化合价 | +1 | +2 | +3 | +5、-3 | +7、-1 | +5、-3 | -2 |
①七种元素的最高价氧化物的水化物中,酸性最强的是
②B、E、G的离子半径由大到小的顺序是
③元素G的最简单氢化物的结构式
(4)200mL某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2充分反应后,得到Na2CO3和NaHCO3的混合溶液,向上述所得溶液中,逐滴加入2mol/L的盐酸,所得气体的体积与所加盐酸的体积关系如图所示(不考虑体积变化):
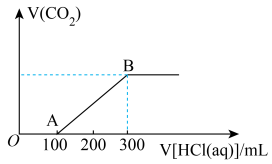
B点时,反应所得溶液中溶质的物质的量浓度是
(5)向浑浊的水中加入明矾(KAl(SO4)2·12H2O)后,水可得到净化。写出硫酸铝钾在水中的电离方程式:
您最近一年使用:0次
名校
7 . 下列叙述正确的有
①爆炸、变色、导电一定属于化学变化
② 都能溶于水生成碱,它们都属于碱性氧化物
都能溶于水生成碱,它们都属于碱性氧化物
③金刚石、石墨、 互为同位素
互为同位素
④ 均可通过化合反应制得
均可通过化合反应制得
⑤烧碱固体、纯醋酸、乙醇均不导电,所以它们都不是电解质
①爆炸、变色、导电一定属于化学变化
②
 都能溶于水生成碱,它们都属于碱性氧化物
都能溶于水生成碱,它们都属于碱性氧化物③金刚石、石墨、
 互为同位素
互为同位素④
 均可通过化合反应制得
均可通过化合反应制得⑤烧碱固体、纯醋酸、乙醇均不导电,所以它们都不是电解质
| A.1项 | B.2项 | C.3项 | D.4项 |
您最近一年使用:0次
8 . 现有以下物质:
①NaOH溶液;②熔融NaCl;③氯化氢;④熔融 ;⑤NaOH固体;⑥
;⑤NaOH固体;⑥ ;⑦硬铝;⑧饱和
;⑦硬铝;⑧饱和 溶液;⑨乙醇;⑩Cu。
溶液;⑨乙醇;⑩Cu。
回答下列问题:
(1)能导电的物质是___________ (填序号,下同),能导电的电解质是___________ ,属于合金的是___________ 。
(2)写出④的电离方程式:___________ 。
(3)写出 溶液和
溶液和 溶液反应的离子方程式:
溶液反应的离子方程式:___________ 。
(4)检验久置空气中的NaOH固体是否变质的方法是___________ 。
(5)向盐酸中逐滴滴加等浓度的氢氧化钠溶液,溶液的导电能力变化情况为___________ 。
①NaOH溶液;②熔融NaCl;③氯化氢;④熔融
 ;⑤NaOH固体;⑥
;⑤NaOH固体;⑥ ;⑦硬铝;⑧饱和
;⑦硬铝;⑧饱和 溶液;⑨乙醇;⑩Cu。
溶液;⑨乙醇;⑩Cu。回答下列问题:
(1)能导电的物质是
(2)写出④的电离方程式:
(3)写出
 溶液和
溶液和 溶液反应的离子方程式:
溶液反应的离子方程式:(4)检验久置空气中的NaOH固体是否变质的方法是
(5)向盐酸中逐滴滴加等浓度的氢氧化钠溶液,溶液的导电能力变化情况为
您最近一年使用:0次
9 . I.现有9种物质:①Na;②盐酸;③ ;④
;④ ;⑤空气;⑥
;⑤空气;⑥ ;⑦
;⑦ 胶体;⑧Na2O2;⑨CO
胶体;⑧Na2O2;⑨CO
(1)属于电解质的是_______ (用序号填空,下同);属于酸性氧化物的是_______ 。
(2)实验室中少量①通常保存在_____ 中;④在工业上大量用于_____ (写出一种用途即可)。
(3)⑧与⑥反应的化学方程式_______
(4)③是一种白色晶体,因受热易分解并产生气体适宜作膨松剂,请写出此物质受热分解的化学方程式_______ 。
Ⅱ.某种飞船以联氨 和
和 为动力源,发生反应:
为动力源,发生反应: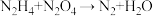 ,反应温度可高达
,反应温度可高达 ,回答下列问题。
,回答下列问题。
(5)①配平该方程式_______ 。
②该反应中,氧化产物与还原产物的质量之比为_______ 。
 ;④
;④ ;⑤空气;⑥
;⑤空气;⑥ ;⑦
;⑦ 胶体;⑧Na2O2;⑨CO
胶体;⑧Na2O2;⑨CO(1)属于电解质的是
(2)实验室中少量①通常保存在
(3)⑧与⑥反应的化学方程式
(4)③是一种白色晶体,因受热易分解并产生气体适宜作膨松剂,请写出此物质受热分解的化学方程式
Ⅱ.某种飞船以联氨
 和
和 为动力源,发生反应:
为动力源,发生反应: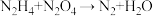 ,反应温度可高达
,反应温度可高达 ,回答下列问题。
,回答下列问题。(5)①配平该方程式
②该反应中,氧化产物与还原产物的质量之比为
您最近一年使用:0次
名校
10 . 下列叙述正确的是
A.碳酸钙难溶于水,放入水中溶液不导电,且碳酸钙在960℃时分解,不存在熔融状态导电的性质,故 是非电解质 是非电解质 |
| B.相同温度下,强电解质溶液的导电性比弱电解质溶液的导电性强 |
| C.AgCl难溶于水,但溶于水的那一部分能完全电离,故AgCl是强电解质 |
D. 晶体在熔融状态下不导电,但溶于水后其水溶液导电,故 晶体在熔融状态下不导电,但溶于水后其水溶液导电,故 是强电解质 是强电解质 |
您最近一年使用:0次








