解题方法
1 . 下列表示反应中相关微粒的化学用语正确的是
A.中子数为18的氯原子: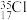 |
| B.HCl的电子式为:H:Cl |
C. 的原子结构示意图: 的原子结构示意图: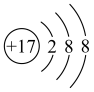 |
D.NaHCO3的电离方程式:NaHCO3 = Na+ + H+ + |
您最近一年使用:0次
2 . 某瓶装饮料中含有下列成分,其中不属于电解质的是
| A.小苏打 | B.葡萄糖 | C.氯化钾 | D.硫酸锌 |
您最近一年使用:0次
解题方法
3 . 科学家在研究化学物质常对其进行分类,以便对同类物质的性质进行深入研究,物质分类及转化思想贯穿整个化学学科学习的始终。
下列物质:①纯硫酸;②硝酸钾溶液;③铜;④Na2O固体;⑤Ba(OH)2固体;⑥K2CO3固体;⑦二氧化碳;⑧熔融KHSO4;⑨氨气;
(1)能导电的是___________ (填序号,下同),属于电解质的是___________ ,属于非电解质的是___________ 。
(2)写出⑧在水溶液中的电离方程式:___________ ,其中阴离子的检验方法:___________ 。
(3)从物质的组成看KNO3、K2CO3、KHSO4都属于钾盐,其分类标准依据是:___________ 。
(4)检验②中金属阳离子的实验方法是___________ (填实验操作的名称),确定该离子存在的现象是___________ 。
(5)向⑤的水溶液中通入过量的⑦反应的离子方程式:___________ 。
下列物质:①纯硫酸;②硝酸钾溶液;③铜;④Na2O固体;⑤Ba(OH)2固体;⑥K2CO3固体;⑦二氧化碳;⑧熔融KHSO4;⑨氨气;
(1)能导电的是
(2)写出⑧在水溶液中的电离方程式:
(3)从物质的组成看KNO3、K2CO3、KHSO4都属于钾盐,其分类标准依据是:
(4)检验②中金属阳离子的实验方法是
(5)向⑤的水溶液中通入过量的⑦反应的离子方程式:
您最近一年使用:0次
解题方法
4 . 下列化学用语表示错误的是
A.1,3-丁二烯的结构简式: |
B.顺—2—丁烯的分子结构模型: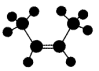 |
C. 的电离方程式: 的电离方程式: |
D.基态铜原子的价层电子轨道表示式: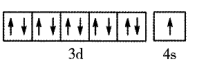 |
您最近一年使用:0次
5 . 完成下列问题。
(1)已知在25 ℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表所示。
①亚硫酸发生电离的方程式为______ 。
②碳酸和亚硫酸的第一步电离程度大于第二步电离程度的原因:______ 。
③在相同条件下,试比较H2CO3、 和
和 的酸性强弱:
的酸性强弱:____ >____ >____ 。
(2)在一定温度下,冰醋酸加水稀释的过程中,溶液的导电能力变化如图所示,请回答:____ 。
②a、b、c三点溶液的pH由大到小的顺序为____ ,电离程度最大的是____ 。
③若使c点溶液中c(CH3COO-)增大,在如下措施中可选择____ (填字母)。
A.加热 B.加很稀的NaOH溶液 C.加固体KOH
D.加水 E.加CH3COONa(s) F.加锌粉
(3)向氨水中加入醋酸溶液,其导电能力(I)与加入醋酸溶液的体积(V)关系正确的是______。
(1)已知在25 ℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表所示。
| 酸 | 电离平衡常数 |
| 醋酸 | Ka=1.75×10-5 |
| 碳酸 | Ka1=4.30×10-7 Ka2=5.61×10-11 |
| 亚硫酸 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
②碳酸和亚硫酸的第一步电离程度大于第二步电离程度的原因:
③在相同条件下,试比较H2CO3、
 和
和 的酸性强弱:
的酸性强弱:(2)在一定温度下,冰醋酸加水稀释的过程中,溶液的导电能力变化如图所示,请回答:
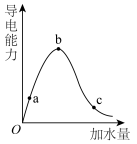
②a、b、c三点溶液的pH由大到小的顺序为
③若使c点溶液中c(CH3COO-)增大,在如下措施中可选择
A.加热 B.加很稀的NaOH溶液 C.加固体KOH
D.加水 E.加CH3COONa(s) F.加锌粉
(3)向氨水中加入醋酸溶液,其导电能力(I)与加入醋酸溶液的体积(V)关系正确的是______。
A.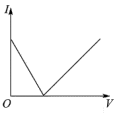 | B.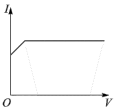 | C.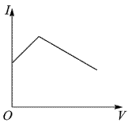 | D.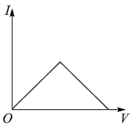 |
您最近一年使用:0次
解题方法
6 . 氯化铁是一种重要的盐,下列说法正确的是
A. FeCl3在水中的电离方程式: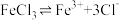 |
B.常温下,FeCl3溶液中水电离出的OH-浓度小于 |
C. FeCl3溶液呈酸性的原因: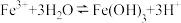 |
D.用FeCl3溶液脱除废气中的 |
您最近一年使用:0次
解题方法
7 . 下列物质既不属于电解质也不属于非电解质的是
| A.烧碱 | B.食醋 | C.硫酸 | D.酒精 |
您最近一年使用:0次
名校
8 . 新型冠状病毒肺炎爆发以来,各类杀菌消毒剂逐渐被人们所认识和使用。下列是我们常见的几种消毒剂:①“84”消毒液(有效成分 );②
);② (在水中一部分可以电离出阴、阳离子);③漂白粉;④
(在水中一部分可以电离出阴、阳离子);③漂白粉;④ ;⑤
;⑤ ;⑥碘酒;⑦
;⑥碘酒;⑦ 酒精;⑧过氧乙酸(
酒精;⑧过氧乙酸( );⑨高铁酸钠(
);⑨高铁酸钠( )。回答下列问题:
)。回答下列问题:
(1)上述杀菌消毒剂属于电解质的是___________ (填序号)。
(2)各类杀菌消毒剂使用时,必须严格按照使用说明。巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用导致游泳池藻类快速生长,池水变绿,写出该反应的化学方程式___________ 。
(3)实验室可用 溶液配制消毒液。
溶液配制消毒液。
①需要用托盘天平称量 固体的质量为
固体的质量为___________  ;在配制过程中,除托盘天平、烧杯、玻璃棒、胶头滴管外还必需的玻璃仪器有
;在配制过程中,除托盘天平、烧杯、玻璃棒、胶头滴管外还必需的玻璃仪器有___________ 。
②下列情况会导致所配制溶液浓度偏高的是___________ (填标号)。
a.称量时所用的砝码生锈
b.移液时,有少量液体浅出
c.定容时,俯视刻度线
(4)高铁酸钠 是一种新型净水剂。高铁酸钠在水中可以发生如下反应并生成胶体:
是一种新型净水剂。高铁酸钠在水中可以发生如下反应并生成胶体: 。当反应转移电子的数目是
。当反应转移电子的数目是 时,生成标准状况下
时,生成标准状况下 的体积约为
的体积约为___________ 。用 代替
代替 处理饮用水的优点是
处理饮用水的优点是___________ (只答一条即可)。
 );②
);② (在水中一部分可以电离出阴、阳离子);③漂白粉;④
(在水中一部分可以电离出阴、阳离子);③漂白粉;④ ;⑤
;⑤ ;⑥碘酒;⑦
;⑥碘酒;⑦ 酒精;⑧过氧乙酸(
酒精;⑧过氧乙酸( );⑨高铁酸钠(
);⑨高铁酸钠( )。回答下列问题:
)。回答下列问题:(1)上述杀菌消毒剂属于电解质的是
(2)各类杀菌消毒剂使用时,必须严格按照使用说明。巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用导致游泳池藻类快速生长,池水变绿,写出该反应的化学方程式
(3)实验室可用
 溶液配制消毒液。
溶液配制消毒液。①需要用托盘天平称量
 固体的质量为
固体的质量为 ;在配制过程中,除托盘天平、烧杯、玻璃棒、胶头滴管外还必需的玻璃仪器有
;在配制过程中,除托盘天平、烧杯、玻璃棒、胶头滴管外还必需的玻璃仪器有②下列情况会导致所配制溶液浓度偏高的是
a.称量时所用的砝码生锈
b.移液时,有少量液体浅出
c.定容时,俯视刻度线
(4)高铁酸钠
 是一种新型净水剂。高铁酸钠在水中可以发生如下反应并生成胶体:
是一种新型净水剂。高铁酸钠在水中可以发生如下反应并生成胶体: 。当反应转移电子的数目是
。当反应转移电子的数目是 时,生成标准状况下
时,生成标准状况下 的体积约为
的体积约为 代替
代替 处理饮用水的优点是
处理饮用水的优点是
您最近一年使用:0次
名校
解题方法
9 . Ⅰ.现有以下几种物质(或微粒):①液氯② ③
③ ④液态HCl⑤稀
④液态HCl⑤稀 ⑥熔融
⑥熔融 。回答下列问题:
。回答下列问题:
(1)②和③之间互为_____ 。
(2)以上物质中属于能导电的电解质是_____ 。(填代号)
(3)写出①在水中发生反应的离子方程式_____ 。
Ⅱ.实验室用固体NaOH配制0.5mol/L的NaOH溶液500mL,有以下仪器和用品有:①烧杯②100mL量筒③药匙④玻璃棒⑤托盘天平(带砝码)
(4)配制时,还缺少的仪器是_____ 。
(5)在配制的转移过程中某学生进行如图操作,请指出其中的错误:_____ 。
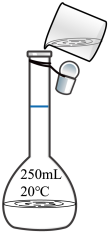
(6)下列操作会使配制的溶液浓度偏低的是_____(填字母)。
(7)实验中还需要2mol/L的NaOH溶液95mL,配制时应称取NaOH固体的质量是_____ g
 ③
③ ④液态HCl⑤稀
④液态HCl⑤稀 ⑥熔融
⑥熔融 。回答下列问题:
。回答下列问题:(1)②和③之间互为
(2)以上物质中属于能导电的电解质是
(3)写出①在水中发生反应的离子方程式
Ⅱ.实验室用固体NaOH配制0.5mol/L的NaOH溶液500mL,有以下仪器和用品有:①烧杯②100mL量筒③药匙④玻璃棒⑤托盘天平(带砝码)
(4)配制时,还缺少的仪器是
(5)在配制的转移过程中某学生进行如图操作,请指出其中的错误:

(6)下列操作会使配制的溶液浓度偏低的是_____(填字母)。
| A.没有将洗涤液转移到容量瓶 | B.转移过程中有少量溶液溅出 |
| C.容量瓶洗净后未干燥 | D.定容时俯视刻度线 |
(7)实验中还需要2mol/L的NaOH溶液95mL,配制时应称取NaOH固体的质量是
您最近一年使用:0次
名校
10 . 按要求回答下列问题:
(1)现有以下物质:①Cl2②CO2③Na2O④NaHSO4⑤漂白粉⑥NaOH溶液⑦Ba(OH)2,其中属于酸性氧化物的有
(2)某金属氯化物MClx的摩尔质量为133.5g/mol,取该金属氯化物26.7g配成水溶液,与足量AgNO3溶液完全反应,生成86.1g白色沉淀。则金属M的摩尔质量为
(3)下列是部分短周期中第二、第三周期元素的原子半径及主要化合价。
| 元素代号 | A | B | C | D | E | F | G |
原子半径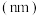 | 0.186 | 0.160 | 0.143 | 0.110 | 0.099 | 0.075 | 0.074 |
| 主要化合价 | +1 | +2 | +3 | +5、-3 | +7、-1 | +5、-3 | -2 |
①七种元素的最高价氧化物的水化物中,酸性最强的是
②B、E、G的离子半径由大到小的顺序是
③元素G的最简单氢化物的结构式
(4)200mL某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2充分反应后,得到Na2CO3和NaHCO3的混合溶液,向上述所得溶液中,逐滴加入2mol/L的盐酸,所得气体的体积与所加盐酸的体积关系如图所示(不考虑体积变化):
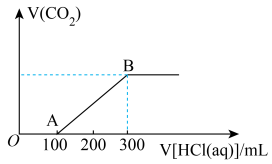
B点时,反应所得溶液中溶质的物质的量浓度是
(5)向浑浊的水中加入明矾(KAl(SO4)2·12H2O)后,水可得到净化。写出硫酸铝钾在水中的电离方程式:
您最近一年使用:0次



