名校
解题方法
1 . 过氧乙酸( )是一种常用的消毒剂,易溶于水、易挥发、见光或受热易分解,其制备愿理为:
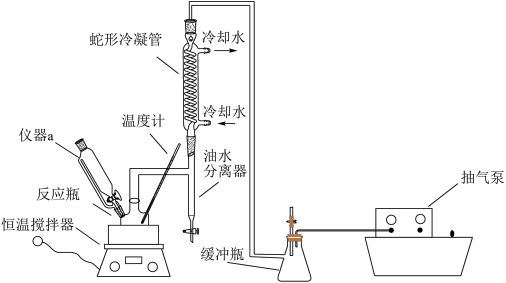
)是一种常用的消毒剂,易溶于水、易挥发、见光或受热易分解,其制备愿理为: ,同时利用乙酸丁酯与水形成共沸物(沸点90.7℃)及时分离出水,以提高产率,为减少反应瓶中乙丁酯的损耗,反应开始前,在油水分离器中加满乙酸丁酯,实验装置如下图。
,同时利用乙酸丁酯与水形成共沸物(沸点90.7℃)及时分离出水,以提高产率,为减少反应瓶中乙丁酯的损耗,反应开始前,在油水分离器中加满乙酸丁酯,实验装置如下图。
(1)过氧乙酸保存与使用时应注意____ (填标号)。
A.避光 B.低温 C.配制消毒液时应带上橡胶手套 D.储存于密闭的金属容器
(2)仪器a的名称是___ ,在本实验中与使用普通分液漏斗相比的优点是__ ,其中盛放的试剂为__ (填“乙酸”或“双氧水”)
(3)反应体系采用减压的目的是___ 。
(4)过氧乙酸(含有少量 杂质)的含量测定流程如下图。
杂质)的含量测定流程如下图。

①判断 恰好除尽的实验现象是
恰好除尽的实验现象是____ 。
②过氧乙酸被 还原,还原产物之一为乙酸,其离子方程式为
还原,还原产物之一为乙酸,其离子方程式为_____ 。
③若样品体积为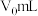 ,加入
,加入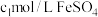 溶液
溶液 ,消耗
,消耗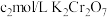 溶液
溶液 ,则过氧乙酸含量为
,则过氧乙酸含量为_____  。
。
(5)判断下列情况对过氧乙酸含量测定结果的影响(填“偏高”、“偏低”或“无影响”)。
①若滴定前无气泡,滴定终点时出现气泡,会使测定结果_____ 。
②若 标准液部分变质,会使测定结果
标准液部分变质,会使测定结果_______ 。
 )是一种常用的消毒剂,易溶于水、易挥发、见光或受热易分解,其制备愿理为:
)是一种常用的消毒剂,易溶于水、易挥发、见光或受热易分解,其制备愿理为: ,同时利用乙酸丁酯与水形成共沸物(沸点90.7℃)及时分离出水,以提高产率,为减少反应瓶中乙丁酯的损耗,反应开始前,在油水分离器中加满乙酸丁酯,实验装置如下图。
,同时利用乙酸丁酯与水形成共沸物(沸点90.7℃)及时分离出水,以提高产率,为减少反应瓶中乙丁酯的损耗,反应开始前,在油水分离器中加满乙酸丁酯,实验装置如下图。
(1)过氧乙酸保存与使用时应注意
A.避光 B.低温 C.配制消毒液时应带上橡胶手套 D.储存于密闭的金属容器
(2)仪器a的名称是
(3)反应体系采用减压的目的是
(4)过氧乙酸(含有少量
 杂质)的含量测定流程如下图。
杂质)的含量测定流程如下图。
①判断
 恰好除尽的实验现象是
恰好除尽的实验现象是②过氧乙酸被
 还原,还原产物之一为乙酸,其离子方程式为
还原,还原产物之一为乙酸,其离子方程式为③若样品体积为
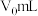 ,加入
,加入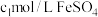 溶液
溶液 ,消耗
,消耗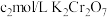 溶液
溶液 ,则过氧乙酸含量为
,则过氧乙酸含量为 。
。(5)判断下列情况对过氧乙酸含量测定结果的影响(填“偏高”、“偏低”或“无影响”)。
①若滴定前无气泡,滴定终点时出现气泡,会使测定结果
②若
 标准液部分变质,会使测定结果
标准液部分变质,会使测定结果
您最近一年使用:0次
解题方法
2 . 某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,得到含70%Cu、25%Al、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
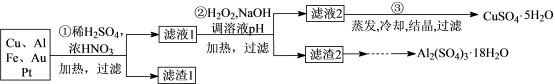
请回答下列问题:
(1)第①步Cu与酸反应的离子方程式为_______________________________________ ;得到滤渣1的主要成分为_________________________________________________ 。
(2)第②步加H2O2的作用是______________________ ,使用H2O2的优点是_____________ 。
(3)用第③步所得CuSO4·5H2O制备无水CuSO4的方法是________________________ 。
(4)由滤渣2制取Al2(SO4)3·18H2O,探究小组设计了三种方案:

上述三种方案中,_________________ 方案不可行,原因是____________________ ,从原子利用率角度考虑,___________ 方案更合理。

请回答下列问题:
(1)第①步Cu与酸反应的离子方程式为
(2)第②步加H2O2的作用是
(3)用第③步所得CuSO4·5H2O制备无水CuSO4的方法是
(4)由滤渣2制取Al2(SO4)3·18H2O,探究小组设计了三种方案:

上述三种方案中,
您最近一年使用:0次
解题方法
3 . 铝是应用广泛的金属,以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料制备铝的一种工艺流程如下:

注:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)A1的原子结构示意图为_______________ ;A1与NaOH溶液反应的离子方程式为______________________________________ 。
(2) “碱溶”时生成偏铝酸钠的离子方程式为_______________________________ 。
(3)向” 过滤Ⅰ所得滤液中加入NaHCO3溶液,溶液的pH_________ (填“增大”、“ 不变”或“减小”)。
(4) “电解Ⅰ”是电解熔融Al2O3,电解过程中作阳极的石墨易消耗,原因是__________________ 。
(5)”电解Ⅱ原理如图所示。

①试写出A、B、C、D物质的化学式:A_______ ,B_______ ,C_______ ,D_______ 。
②阳极的电极反应式为______________________________ 。
(6)铝粉在1000℃时可与N2反应制备AlN。在铝粉中添加少量NH4Cl固体并充分混合,有利于AlN的制备,其主要原因是________________________________ 。

注:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)A1的原子结构示意图为
(2) “碱溶”时生成偏铝酸钠的离子方程式为
(3)向” 过滤Ⅰ所得滤液中加入NaHCO3溶液,溶液的pH
(4) “电解Ⅰ”是电解熔融Al2O3,电解过程中作阳极的石墨易消耗,原因是
(5)”电解Ⅱ原理如图所示。

①试写出A、B、C、D物质的化学式:A
②阳极的电极反应式为
(6)铝粉在1000℃时可与N2反应制备AlN。在铝粉中添加少量NH4Cl固体并充分混合,有利于AlN的制备,其主要原因是
您最近一年使用:0次
10-11高一上·云南红河·期中
名校
解题方法
4 . 在溶液中能大量共存,加入OH-有沉淀产生,加入H+有气体放出的是( )
A.Na+、Cu2+、Cl-、 |
B.Fe3+、K+、 、 、 |
C.Na+、 、OH-、 、OH-、 |
D.Na+、Ca2+、Cl-、 |
您最近一年使用:0次
2017-10-28更新
|
1250次组卷
|
20卷引用:2010年云南省个旧一中高一上学期期中检测化学卷
(已下线)2010年云南省个旧一中高一上学期期中检测化学卷(已下线)2011-2012学年云南省昆明一中高一上学期期中考试化学试卷(已下线)2012-2013学年河北省石家庄市第一中学高一上学期期中考试化学试卷(已下线)2013届广东省揭阳第三中学高一下学期第二次阶段考试文科化学试卷2015-2016学年湖南省娄底市湘中名校高一上期末考试化学试卷江西省临川实验学校2017-2018学年高一(普通班)上学期第一次月考化学试题黑龙江省哈尔滨市第六中学2017-2018学年高一上学期期中考试化学试题内蒙古翁牛特旗乌丹第二中学、呼和浩特市第二十一中学2017-2018学年高一上学期期末联考化学试题河北省保定市蠡县中学2018-2019学年高一上学期9月月考化学试题甘肃省兰州市第一中学2020届高三上学期9月月考化学试题广东省深圳外国语学校2019-2020学年度高一上学期期中考试化学试题(已下线)【浙江新东方】15安徽省舒城中学2020-2021学年高一上学期第一次统考化学试题河南省鹤壁市高级中学2020-2021学年高一上学期第一次段考化学试题天津市五十五中学2022-2023学年高一上学期期中学期调研化学试题甘肃省靖远县二中2021-2022学年高一上学期第一次月考化学试题山西省运城市芮城中学2021-2022学年高一下学期开学摸底考试化学试题陕西省咸阳市兴平南郊高级中学2022-2023学年高一上学期期中考试化学试题安徽省淮北市实验高级中学2022-2023学年高一上学期期末考试化学试题(已下线)专题02 离子反应-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)



