名校
解题方法
1 .  四种易溶于水的化合物只由表中的八种离子组成,且四种化合物中阴、阳离子各不相同。
四种易溶于水的化合物只由表中的八种离子组成,且四种化合物中阴、阳离子各不相同。
已知:A溶液呈强酸性,且A溶液与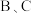 溶液混合均产生白色沉淀,
溶液混合均产生白色沉淀, 的焰色反应呈黄色。
的焰色反应呈黄色。
回答下列问题:
(1)写出C的化学式:_____________ , 的电子式:
的电子式:_____________ 。
(2)写出A溶液与 溶液反应的离子方程式:
溶液反应的离子方程式:_____________ 。
(3)A中阴离子的检验操作_____________________________________ 。
(4)请选出适合存放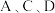 溶液的试剂瓶的序号:(每空1分)
溶液的试剂瓶的序号:(每空1分)
 四种易溶于水的化合物只由表中的八种离子组成,且四种化合物中阴、阳离子各不相同。
四种易溶于水的化合物只由表中的八种离子组成,且四种化合物中阴、阳离子各不相同。| 阴离子 | 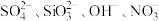 |
| 阳离子 | 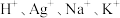 |
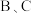 溶液混合均产生白色沉淀,
溶液混合均产生白色沉淀, 的焰色反应呈黄色。
的焰色反应呈黄色。回答下列问题:
(1)写出C的化学式:
 的电子式:
的电子式:(2)写出A溶液与
 溶液反应的离子方程式:
溶液反应的离子方程式:(3)A中阴离子的检验操作
(4)请选出适合存放
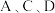 溶液的试剂瓶的序号:(每空1分)
溶液的试剂瓶的序号:(每空1分)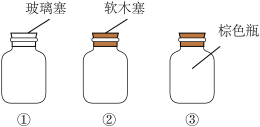
溶液 | A | C |
|
试剂瓶序号 |
您最近一年使用:0次
解题方法
2 . 化学是一门以实验为基础的学科,化学实验是开展化学研究的重要手段.
(1)检验物质的常用方法有显色法、沉淀法、气体法等。下列物质检验的方法中,不合理的是______ 。
(2)下列物质的分离与提纯的方法中,与物质的溶解度无关的是______ 。
(3)不能用于鉴别Na2CO3和KCl溶液的试剂或方法是______ 。
(4)下列各组溶液中,不用其他试剂就可鉴别的是______ 。
(5)下列检验某无色溶液样品中所含离子的实验,正确的是______ 。
(6)下列关于从碘水中萃取碘的实验中,说法正确的是______ 。
(7)某溶液中存在SO 和Cl-两种负离子,使用以下操作进行检验:①滴加足量的BaCl2溶液;②滴加足量的Ba(NO3)2溶液;③过滤;④加足量的盐酸:⑤滴加AgNO3溶液。正确的操作及顺序是
和Cl-两种负离子,使用以下操作进行检验:①滴加足量的BaCl2溶液;②滴加足量的Ba(NO3)2溶液;③过滤;④加足量的盐酸:⑤滴加AgNO3溶液。正确的操作及顺序是______ 。
(8)某化学兴趣小组在课外活动中,对某溶液进行了多次检测,其中三次检测结果如表所示,回答:
①三次检测结果中第______ 次检测结果肯定不正确。
②在检测时,为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子:
第一步:向溶液中滴加过量的______ 溶液(填化学式),其目的是检验CO 并将其除去。
并将其除去。
第二步:加入______ 溶液(填化学式),其目的是______ 。
第三步:过滤,再向滤液中加入______ 溶液(填化学式),其目的是______ 。
(1)检验物质的常用方法有显色法、沉淀法、气体法等。下列物质检验的方法中,不合理的是
| A.酸性溶液:显色法 | B.I2:显色法 |
| C.Cl-:沉淀法 | D.Ca2+:气体法 |
| A.过滤 | B.萃取 | C.结晶 | D.蒸馏 |
| A.盐酸 | B.BaCl2溶液 | C.AgNO3溶液 | D.焰色反应 |
| A.HCl、CuCl2、NaNO3、Na2SO4 |
| B.Na2CO3、Na2SO4、HCl、H2SO4 |
| C.FeCl3、Na2SO4、NaCl、NaOH |
| D.BaCl2、Na2CO3、HCl、NaNO3 |
| A.加AgNO3溶液,生成白色沉淀,可确定有Cl-存在 |
B.加足量稀盐酸,产生无色的气体,可确定有CO 存在 存在 |
C.加足量稀盐酸,无明显现象,再加BaCl2溶液,生成白色沉淀,可确定有SO 存在 存在 |
| D.用洁净的铂丝蘸取溶液,在火焰上灼烧焰色为黄色,可确定含Na+,不含K+ |
| A.萃取剂不能溶于水,且比水更容易使碘溶解 |
| B.注入碘水和萃取剂,倒转分液漏斗反复用力振荡后即可分液 |
| C.萃取时,选用萃取剂的密度必须比水大 |
| D.若没有四氯化碳,可用酒精代替 |
 和Cl-两种负离子,使用以下操作进行检验:①滴加足量的BaCl2溶液;②滴加足量的Ba(NO3)2溶液;③过滤;④加足量的盐酸:⑤滴加AgNO3溶液。正确的操作及顺序是
和Cl-两种负离子,使用以下操作进行检验:①滴加足量的BaCl2溶液;②滴加足量的Ba(NO3)2溶液;③过滤;④加足量的盐酸:⑤滴加AgNO3溶液。正确的操作及顺序是| A.①③⑤ | B.②④③⑤ | C.②③⑤ | D.⑤③① |
| 检测次数 | 溶液中检测出的物质 |
| 第一次 | KCl、K2SO4、Na2CO3、NaCl |
| 第二次 | KCl、BaCl2、Na2SO4、K2CO3 |
| 第三次 | Na2SO4、KCl、K2CO3、NaCl |
②在检测时,为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子:
第一步:向溶液中滴加过量的
 并将其除去。
并将其除去。第二步:加入
第三步:过滤,再向滤液中加入
您最近一年使用:0次
3 . A、B、C三种可溶性化合物,它们的阳离子可能是Na+、Mg2+、Ag+,阴离子可能是 、OH-、Cl-,分别取相同质量的三种化合物,溶解于水,配制相同体积的溶液,其物质的量的浓度由大到小的顺序是A、B、C,则三种化合物化学式分别是:A
、OH-、Cl-,分别取相同质量的三种化合物,溶解于水,配制相同体积的溶液,其物质的量的浓度由大到小的顺序是A、B、C,则三种化合物化学式分别是:A___________ 、B___________ 、C___________ 。
 、OH-、Cl-,分别取相同质量的三种化合物,溶解于水,配制相同体积的溶液,其物质的量的浓度由大到小的顺序是A、B、C,则三种化合物化学式分别是:A
、OH-、Cl-,分别取相同质量的三种化合物,溶解于水,配制相同体积的溶液,其物质的量的浓度由大到小的顺序是A、B、C,则三种化合物化学式分别是:A
您最近一年使用:0次
解题方法
4 . Ⅰ.FeCl3是黑棕色晶体,主要用于金属蚀刻,污水处理。回答下列问题。
(1)按照物质的分类方法,FeCl3应属于_______ (填序号)。
①酸 ②氯化物 ③混合物 ④盐 ⑤电解质
(2)将饱和FeCl3溶液逐滴加入沸水中,继续煮沸可制取氢氧化铁胶体,氢氧化铁胶体可处理污水,该反应的化学方程式为_____________________ 。
(3)某河道两旁甲、乙两厂,它们排放的工业废水中,共含K+、Ag+、Fe3+、Cl-、OH-、 六种离子。甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子是
六种离子。甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子是_________ 。
(4)已知:H3PO2+NaOH(过量)=NaH2PO2+H2O。据此H3PO2属于______ (选填“一”、“二”或“三”)元酸。NaH2PO2属于_____ (选填“正盐”或“酸式盐”)。
(1)按照物质的分类方法,FeCl3应属于
①酸 ②氯化物 ③混合物 ④盐 ⑤电解质
(2)将饱和FeCl3溶液逐滴加入沸水中,继续煮沸可制取氢氧化铁胶体,氢氧化铁胶体可处理污水,该反应的化学方程式为
(3)某河道两旁甲、乙两厂,它们排放的工业废水中,共含K+、Ag+、Fe3+、Cl-、OH-、
 六种离子。甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子是
六种离子。甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子是(4)已知:H3PO2+NaOH(过量)=NaH2PO2+H2O。据此H3PO2属于
您最近一年使用:0次
名校
5 . 现有一混合溶液可能含有下列离子中的若干种: 、
、 、
、 、
、 、
、 、
、 、
、 、
、 ,为确定溶液的成分,进行如下实验:
,为确定溶液的成分,进行如下实验:
①取200mL该混合溶液,分为二等份,分别置于两支试管中;
②向第一份溶液中加入足量NaOH溶液并加热,无沉淀产生,收集到的气体(设气体全部逸出)在标准状况下的体积为224mL;
③向第二份溶液中加入足量氯化钡溶液后得到8.6g沉淀,经足量盐酸洗涤、干燥后,沉淀质量为4.66g。
已知: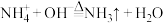 。根据实验完成下列问题;
。根据实验完成下列问题;
(1)由第一份溶液中进行的实验可知,原溶液中含有
___________ 。
(2)由第二份溶液中进行的实验可知,8.6g沉淀的成分为___________ (填化学式),原混合液中,形成该沉淀对应的阴离子的物质的量浓度为___________ 。
(3)综合上述实验结果,该混合物中是否一定含有 ?
?___________ (填“是”或“否”),可能存在的离子有___________ (填离子符号,下同),一定不存在的离子有___________ 。
(4)请写出第二份溶液中用盐酸洗涤沉淀时发生反应的离子方程式___________ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 ,为确定溶液的成分,进行如下实验:
,为确定溶液的成分,进行如下实验:①取200mL该混合溶液,分为二等份,分别置于两支试管中;
②向第一份溶液中加入足量NaOH溶液并加热,无沉淀产生,收集到的气体(设气体全部逸出)在标准状况下的体积为224mL;
③向第二份溶液中加入足量氯化钡溶液后得到8.6g沉淀,经足量盐酸洗涤、干燥后,沉淀质量为4.66g。
已知:
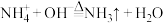 。根据实验完成下列问题;
。根据实验完成下列问题;(1)由第一份溶液中进行的实验可知,原溶液中含有

(2)由第二份溶液中进行的实验可知,8.6g沉淀的成分为
(3)综合上述实验结果,该混合物中是否一定含有
 ?
?(4)请写出第二份溶液中用盐酸洗涤沉淀时发生反应的离子方程式
您最近一年使用:0次
名校
6 . 在化学研究中,往往可以通过观察现象认识物质变化的情况。请分析以下一组有现象变化的化学反应。
(1)实验Ⅰ的现象为______ 。
(2)实验Ⅱ的现象中能证明 发生反应而Cu2+不发生反应的实验现象是
发生反应而Cu2+不发生反应的实验现象是______ 。
(3)实验Ⅲ的离子方程式为______ 。
(4)实验Ⅳ中Cu4(OH)xSO4中x=______ ,已知最终得到的溶液中Cu元素仅存在Cu(OH) 一种形式,若分离出蓝色沉淀并称量其质量为ag,则溶液中Cu(OH)
一种形式,若分离出蓝色沉淀并称量其质量为ag,则溶液中Cu(OH) 的物质的量浓度为
的物质的量浓度为______ (列出计算式)。
| 实验 | 试剂及操作 | 现象 | |
 1.0mL | 试管 | 滴管 | |
| 0.1mol·L−1H2SO4溶液 | 先滴加酚酞溶液,再滴加1.5mL0.2mol·L−1NaOH溶液 | Ⅰ.______ | |
| 0.1mol·L−1CuSO4溶液 | 滴加2mL0.1mol·L−1BaCl2溶液 | Ⅱ.______ | |
| 0.1mol·L−1FeCl2溶液 | 滴加5-6滴饱和NaHCO3溶液 | Ⅲ.产生绿色沉淀,并产生气泡 | |
| 0.1mol·L−1CuSO4溶液 | 持续滴加1.0mLNaOH溶液 | Ⅳ.先产生蓝色沉淀[主要成分Cu4(OH)xSO4],后沉淀部分溶解 | |
(1)实验Ⅰ的现象为
(2)实验Ⅱ的现象中能证明
 发生反应而Cu2+不发生反应的实验现象是
发生反应而Cu2+不发生反应的实验现象是(3)实验Ⅲ的离子方程式为
(4)实验Ⅳ中Cu4(OH)xSO4中x=
 一种形式,若分离出蓝色沉淀并称量其质量为ag,则溶液中Cu(OH)
一种形式,若分离出蓝色沉淀并称量其质量为ag,则溶液中Cu(OH) 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
名校
7 . 某无色透明溶液中可能大量存在Ag+、Ca2+、Cu2+、Fe3+、Na+中的几种。请填写下列空白。
(1)不做任何实验就可以肯定原溶液中不存在的离子是___________ 。
(2)取少量原溶液,加入过量稀盐酸、有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是___________ 。
(3)取(2)中的滤液,加入过量的碳酸钠溶液,出现白色沉淀,说明原溶液中肯定有___________ ,该过程产生白色沉淀的离子方程式为___________ 。
(4)原溶液可能大量共存的阴离子是___________(选填字母编号)。
(5)写出NaHSO4在水溶液中的电离方程式___________ 。12gNaHSO4中含有___________ 个O原子,将其溶于水配成500mL溶液,则溶液的物质的量浓度为___________ mol/L,从中取出l00mL可以消耗1mol/L的NaOH溶液___________ mL。
(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸、有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是
(3)取(2)中的滤液,加入过量的碳酸钠溶液,出现白色沉淀,说明原溶液中肯定有
(4)原溶液可能大量共存的阴离子是___________(选填字母编号)。
| A.OH- | B. | C. | D.Cl- |
您最近一年使用:0次
名校
8 . 某无色溶液可能含有 、
、 、
、 、
、 、
、 、
、 中的一种或几种离子。
中的一种或几种离子。
①向此溶液中滴加稀盐酸无明显现象。
②取少量①的溶液加入少量的Na2SO4溶液,有白色沉淀产生。
③取②的上层清液并加入过量的NaOH溶液,无明显现象。
(1)原溶液中一定含有的离子是_______ ,一定不含有的离子是_____ ,不能确定是否含有的离子是_______ ,可以用______ 检验此离子。
(2)②中反应的离子方程式为__________ 。
 、
、 、
、 、
、 、
、 、
、 中的一种或几种离子。
中的一种或几种离子。①向此溶液中滴加稀盐酸无明显现象。
②取少量①的溶液加入少量的Na2SO4溶液,有白色沉淀产生。
③取②的上层清液并加入过量的NaOH溶液,无明显现象。
(1)原溶液中一定含有的离子是
(2)②中反应的离子方程式为
您最近一年使用:0次
解题方法
9 . 在溶液中进行的化学反应通常是比较快的。所以在实验室或化工生产中,溶液的应用非常广泛。回答下列问题:
(1)实验室配制250mL NaOH溶液时应使用托盘天平称量NaOH固体的质量为
NaOH溶液时应使用托盘天平称量NaOH固体的质量为___________ g。下列配制过程中出现的情况,会使所配溶液浓度偏高的是___________ (填字母)。
A.溶解时,有少量溶液溅出 B.未恢复至室温就转移定容
C.定容时,俯视刻度线 D.未干燥容量瓶
现有一混合溶液,可能含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的若干种,取两份各100mL该混合溶液进行如下实验。
中的若干种,取两份各100mL该混合溶液进行如下实验。
实验I:向第一份混合溶液中滴加上述配制的 的NaOH溶液,溶液中沉淀的质量与NaOH溶液的体积关系如图所示:
的NaOH溶液,溶液中沉淀的质量与NaOH溶液的体积关系如图所示:

实验II:先向第二份混合溶液中加入足量 溶液,无明显现象;再加入足量的
溶液,无明显现象;再加入足量的 溶液,产生白色沉淀。
溶液,产生白色沉淀。
已知: ,
, 。
。
(2)由实验I推断该混合溶液中一定存在___________ (填离子符号,下同),一定不存在___________ 。
(3)实验I图像ab段发生反应的离子方程式为___________ ;bc段参与反应的离子的物质的量为___________ 。
(4)某同学由实验II推断该混合溶液中一定存在 ,你是否同意该说法,说明理由:
,你是否同意该说法,说明理由:_____ 。
(5)若原混合溶液中不含 ,则原溶液中含有的阴离子为
,则原溶液中含有的阴离子为___________ ,其物质的量浓度为___________ 。
(1)实验室配制250mL
 NaOH溶液时应使用托盘天平称量NaOH固体的质量为
NaOH溶液时应使用托盘天平称量NaOH固体的质量为A.溶解时,有少量溶液溅出 B.未恢复至室温就转移定容
C.定容时,俯视刻度线 D.未干燥容量瓶
现有一混合溶液,可能含有
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的若干种,取两份各100mL该混合溶液进行如下实验。
中的若干种,取两份各100mL该混合溶液进行如下实验。实验I:向第一份混合溶液中滴加上述配制的
 的NaOH溶液,溶液中沉淀的质量与NaOH溶液的体积关系如图所示:
的NaOH溶液,溶液中沉淀的质量与NaOH溶液的体积关系如图所示:
实验II:先向第二份混合溶液中加入足量
 溶液,无明显现象;再加入足量的
溶液,无明显现象;再加入足量的 溶液,产生白色沉淀。
溶液,产生白色沉淀。已知:
 ,
, 。
。(2)由实验I推断该混合溶液中一定存在
(3)实验I图像ab段发生反应的离子方程式为
(4)某同学由实验II推断该混合溶液中一定存在
 ,你是否同意该说法,说明理由:
,你是否同意该说法,说明理由:(5)若原混合溶液中不含
 ,则原溶液中含有的阴离子为
,则原溶液中含有的阴离子为
您最近一年使用:0次
名校
10 . Ⅰ.X、Y、Z三种可溶性盐,其阳离子分别是 、
、 、
、 中的某一种,阴离子分别是
中的某一种,阴离子分别是 、
、 、
、 ,中的某一种。现进行以下实验:
,中的某一种。现进行以下实验:
①将三种盐各取少量,分别溶于盛有5mL蒸馏水的三支试管中,只有X盐溶液呈蓝色。
②分别向三支试管中加入2mL稀盐酸,发现Y盐溶液中产生白色沉淀,Z盐溶液无明显现象。
回答下列问题:
(1)根据上述事实,推断这三种盐的化学式:X_______ ,Y_______ ,Z_______ 。
(2)写出下列反应的离子方程式。
X与氢氧化钡溶液反应:_______ 。
Y与盐酸反应:_______ 。
Ⅱ.有关物质的量的计算
(3) 和
和 一定条件下可以发生反应
一定条件下可以发生反应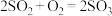 ,若有a mol
,若有a mol  与b mol
与b mol  充分反应,则反应后硫原子与氧原子的个数比为
充分反应,则反应后硫原子与氧原子的个数比为_______ (用含a、b的代数式表示)。
(4)36g CO与 的混合气体与足量
的混合气体与足量 充分反应后,将所得气体通入过量的澄清石灰水中,生成白色沉淀的质量为100g,则36g CO与
充分反应后,将所得气体通入过量的澄清石灰水中,生成白色沉淀的质量为100g,则36g CO与 的混合气体的总物质的量为
的混合气体的总物质的量为_______ mol,其中的CO在标准状况下的体积为_______ L。
(5)用质量分数为98%,密度为1.84g/mL的浓硫酸配制1mol/L的稀硫酸500mL,则需用量筒量取浓硫酸的体积为_______ 。
 、
、 、
、 中的某一种,阴离子分别是
中的某一种,阴离子分别是 、
、 、
、 ,中的某一种。现进行以下实验:
,中的某一种。现进行以下实验:①将三种盐各取少量,分别溶于盛有5mL蒸馏水的三支试管中,只有X盐溶液呈蓝色。
②分别向三支试管中加入2mL稀盐酸,发现Y盐溶液中产生白色沉淀,Z盐溶液无明显现象。
回答下列问题:
(1)根据上述事实,推断这三种盐的化学式:X
(2)写出下列反应的离子方程式。
X与氢氧化钡溶液反应:
Y与盐酸反应:
Ⅱ.有关物质的量的计算
(3)
 和
和 一定条件下可以发生反应
一定条件下可以发生反应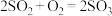 ,若有a mol
,若有a mol  与b mol
与b mol  充分反应,则反应后硫原子与氧原子的个数比为
充分反应,则反应后硫原子与氧原子的个数比为(4)36g CO与
 的混合气体与足量
的混合气体与足量 充分反应后,将所得气体通入过量的澄清石灰水中,生成白色沉淀的质量为100g,则36g CO与
充分反应后,将所得气体通入过量的澄清石灰水中,生成白色沉淀的质量为100g,则36g CO与 的混合气体的总物质的量为
的混合气体的总物质的量为(5)用质量分数为98%,密度为1.84g/mL的浓硫酸配制1mol/L的稀硫酸500mL,则需用量筒量取浓硫酸的体积为
您最近一年使用:0次



