1 . 下列变化中,不涉及氧化还原反应的是
| A.金属的冶炼 | B.钢铁的锈蚀 |
| C.食物的腐败 | D.水变成水蒸气 |
您最近一年使用:0次
2 . 下列表示氧化还原反应中电子转移的方向和数目正确的是
A.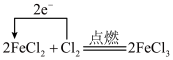 | B.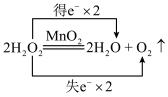 |
C. | D.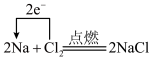 |
您最近一年使用:0次
3 . 下列反应中,不属于四种基本反应类型,但属于氧化还原反应的是
| A.2F2+2H2O=4HF+O2 | B.CH4+2O2=CO2+2H2O |
| C.2KClO3=2KCl+3O2↑ | D.Ca(ClO)2+2HCl=CaCl2+2HClO |
您最近一年使用:0次
4 . 有A、B、C、D、E、F六种化合物,它们之间的反应关系如下所示:
①A+B→C+E,②C+NaOH→蓝色沉淀D+F,③D A+E,④
A+E,④ →白色沉淀
→白色沉淀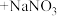 。
。
请回答下列问题。
(1)写出化学式:B___________ ,D___________ ,F___________ 。
(2)写出①④反应的离子方程式:
①___________ 。
④___________ 。
(3)根据西汉《淮南万毕术》记载,C溶液与F的反应是现代湿法冶金的基础。写出该反应的化学方程式,并用单线桥标出电子转移的方向和数目。___________ 。
①A+B→C+E,②C+NaOH→蓝色沉淀D+F,③D
 A+E,④
A+E,④ →白色沉淀
→白色沉淀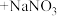 。
。请回答下列问题。
(1)写出化学式:B
(2)写出①④反应的离子方程式:
①
④
(3)根据西汉《淮南万毕术》记载,C溶液与F的反应是现代湿法冶金的基础。写出该反应的化学方程式,并用单线桥标出电子转移的方向和数目。
您最近一年使用:0次
解题方法
5 . 甲烷在空气中燃烧,甲烷发生了___ 反应。
您最近一年使用:0次
6 . 氧化还原反应在工农业生产、日常生活中具有广泛用途,贯穿古今。
(1)工业盐的主要成分是 ,以前有许多起因误食
,以前有许多起因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力,这说明
结合的能力,这说明 具有
具有_______ (填“氧化”或“还原”,下同)。工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有________ 性。
(2) 常用于焊接,在焊接铜器时可用
常用于焊接,在焊接铜器时可用 除去铜器表面的氧化铜,便于焊接,其反应如下:
除去铜器表面的氧化铜,便于焊接,其反应如下: 。
。
①配平上述氧化还原反应方程式___________ 。
②该反应中,氧化剂是___________ (填化学式),被氧化的元素是___________ (填元素名称)。
(3)二氧化氯是一种高效消毒剂。工业上制备 的反应为:
的反应为: 。
。
①该反应中的还原产物是___________ (写化学式),反应中每生成1mol 分子,被氧化的HCl的物质的量为
分子,被氧化的HCl的物质的量为___________ ,转移电子的数目为___________ 。
②用“单线桥”标出反应中电子转移的方向与数目___________ 。
③ 在杀菌消毒的过程中会生成副产物亚氯酸盐(
在杀菌消毒的过程中会生成副产物亚氯酸盐( ),要将其转化为
),要将其转化为 除去,下列试剂能实现其转化过程的是
除去,下列试剂能实现其转化过程的是___________ (填字母)。
a. b.
b. c.
c. d.
d.
(4)双氯水是公认的绿色氧化剂。已知氯化性强弱顺序为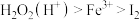 ,向
,向 溶液中加入足量硫酸酸化的双氧水,发生反应的离子方程式为
溶液中加入足量硫酸酸化的双氧水,发生反应的离子方程式为___________ 。
(1)工业盐的主要成分是
 ,以前有许多起因误食
,以前有许多起因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力,这说明
结合的能力,这说明 具有
具有(2)
 常用于焊接,在焊接铜器时可用
常用于焊接,在焊接铜器时可用 除去铜器表面的氧化铜,便于焊接,其反应如下:
除去铜器表面的氧化铜,便于焊接,其反应如下: 。
。①配平上述氧化还原反应方程式
②该反应中,氧化剂是
(3)二氧化氯是一种高效消毒剂。工业上制备
 的反应为:
的反应为: 。
。①该反应中的还原产物是
 分子,被氧化的HCl的物质的量为
分子,被氧化的HCl的物质的量为②用“单线桥”标出反应中电子转移的方向与数目
③
 在杀菌消毒的过程中会生成副产物亚氯酸盐(
在杀菌消毒的过程中会生成副产物亚氯酸盐( ),要将其转化为
),要将其转化为 除去,下列试剂能实现其转化过程的是
除去,下列试剂能实现其转化过程的是a.
 b.
b. c.
c. d.
d.
(4)双氯水是公认的绿色氧化剂。已知氯化性强弱顺序为
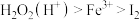 ,向
,向 溶液中加入足量硫酸酸化的双氧水,发生反应的离子方程式为
溶液中加入足量硫酸酸化的双氧水,发生反应的离子方程式为
您最近一年使用:0次
7 . 填空
(1)过氧化钠与水反应的化学方程式__________ 。
(2)铁在氯气中燃烧反应的化学方程式__________ 。
(3)氯气和水反应的化学方程式__________ 。
(4)钠与氯气反应的反应方程式为__________ ,钠最外层有__________ 电子,氯最外层有__________ 电子,在反应中钠元素的化合价__________ ,氯元素的化合价__________ ,在氧化还原反应中得到电子和失去电子分别是__________ ,钠元素的原子结构示意图为__________ 。
(5)在水溶液里或__________ 状态下能够__________ 的化合物叫电解质。
(6)Na保存在__________ 或石蜡油中若着火了用__________ 灭火。
(1)过氧化钠与水反应的化学方程式
(2)铁在氯气中燃烧反应的化学方程式
(3)氯气和水反应的化学方程式
(4)钠与氯气反应的反应方程式为
(5)在水溶液里或
(6)Na保存在
您最近一年使用:0次
名校
解题方法
8 . 回答下列问题:
(1)氧化亚铜( )是一种鲜红色粉末状固体,几乎不溶于水,可在酸性溶液中发生反应与硫酸、硝酸的反应如下:
)是一种鲜红色粉末状固体,几乎不溶于水,可在酸性溶液中发生反应与硫酸、硝酸的反应如下:
ⅰ.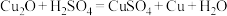
ⅱ.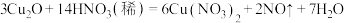
①反应ⅰ中还原剂为_______ (填化学式,下同),ⅱ的还原产物为_______ 。
②用单线桥标出反应ⅱ中电子转移的方向和数目:_______ 。
(2)高铁酸钠( )有强氧化性,可以有效杀灭水中的细菌和病毒。已知湿法制备高铁酸钠的反应体系有六种微粒:
)有强氧化性,可以有效杀灭水中的细菌和病毒。已知湿法制备高铁酸钠的反应体系有六种微粒: 、
、 、
、 、
、 、
、 、
、 。写出并配平湿法制备高铁酸钠的离子方程式:
。写出并配平湿法制备高铁酸钠的离子方程式:_______ 。
(3) 和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为:_______
和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为:_______ _______
_______ _______
_______ _______
_______ _______
_______ _______
_______ 。请配平上述化学方程式:
。请配平上述化学方程式:_______ 。
(4)产生1个 ,转移的电子的个数为
,转移的电子的个数为_______ 个。
(5)酸性高锰酸钾用_______ (填酸的化学式)酸酸化。
(1)氧化亚铜(
 )是一种鲜红色粉末状固体,几乎不溶于水,可在酸性溶液中发生反应与硫酸、硝酸的反应如下:
)是一种鲜红色粉末状固体,几乎不溶于水,可在酸性溶液中发生反应与硫酸、硝酸的反应如下:ⅰ.
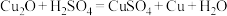
ⅱ.
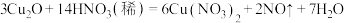
①反应ⅰ中还原剂为
②用单线桥标出反应ⅱ中电子转移的方向和数目:
(2)高铁酸钠(
 )有强氧化性,可以有效杀灭水中的细菌和病毒。已知湿法制备高铁酸钠的反应体系有六种微粒:
)有强氧化性,可以有效杀灭水中的细菌和病毒。已知湿法制备高铁酸钠的反应体系有六种微粒: 、
、 、
、 、
、 、
、 、
、 。写出并配平湿法制备高铁酸钠的离子方程式:
。写出并配平湿法制备高铁酸钠的离子方程式:(3)
 和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为:_______
和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为:_______ _______
_______ _______
_______ _______
_______ _______
_______ _______
_______ 。请配平上述化学方程式:
。请配平上述化学方程式:(4)产生1个
 ,转移的电子的个数为
,转移的电子的个数为(5)酸性高锰酸钾用
您最近一年使用:0次
名校
解题方法
9 . 运用分类的方法,可以发现物质及其变化的规律,预测物质的性质及可能发生的变化。下图是依据一定的分类标准,对某些物质与水反应进行分类的情况。
已知: 。
。
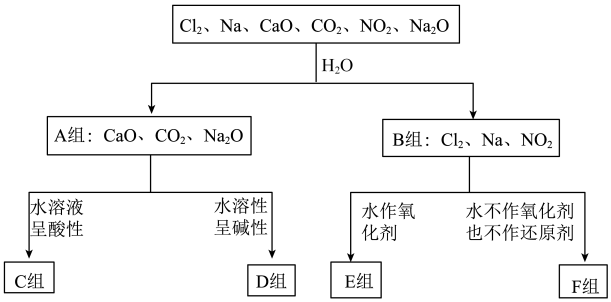
回答下列问题:
(1)第一级分类标准(分成A、B组的依据)是___________ 。
(2)A组物质中属于电解质的是___________ (填化学式)。
(3)从物质类别角度分析, 属于酸性氧化物,类似于
属于酸性氧化物,类似于 ,从而认为
,从而认为 可以归于C组。预测
可以归于C组。预测 和足量
和足量 溶液反应的离子方程式为
溶液反应的离子方程式为___________ 。
(4)若将 与水的反应依据图中标准分类,应属于
与水的反应依据图中标准分类,应属于___________ (填标号)。
a.C组 b.D组 c.E组 d.F组
(5)写出E组发生反应的化学方程式并用双线桥法标出电子转移的方向和数目___________ 。
(6)实验室常用F组中的一种物质与NaOH溶液反应来制备“84”消毒液,此反应的化学方程式为___________ 。
已知:
 。
。
回答下列问题:
(1)第一级分类标准(分成A、B组的依据)是
(2)A组物质中属于电解质的是
(3)从物质类别角度分析,
 属于酸性氧化物,类似于
属于酸性氧化物,类似于 ,从而认为
,从而认为 可以归于C组。预测
可以归于C组。预测 和足量
和足量 溶液反应的离子方程式为
溶液反应的离子方程式为(4)若将
 与水的反应依据图中标准分类,应属于
与水的反应依据图中标准分类,应属于a.C组 b.D组 c.E组 d.F组
(5)写出E组发生反应的化学方程式并用双线桥法标出电子转移的方向和数目
(6)实验室常用F组中的一种物质与NaOH溶液反应来制备“84”消毒液,此反应的化学方程式为
您最近一年使用:0次
2024-01-10更新
|
76次组卷
|
2卷引用:新疆乌鲁木齐市第十一中学2023-2024学年高一上学期1月期末化学试题
名校
解题方法
10 . 印刷电路板是由塑料和铜箔复合而成,刻制印刷电路时要用FeCl3溶液作为“腐蚀液”生成CuCl2和FeCl2,其反应的化学方程式如下:Cu+2FeCl3=CuCl2+2FeCl2。
(1)请在上式中标出电子转移的方向和数目:________ 。
(2)上述反应中被氧化的元素是___________ 。
(3)写出FeCl3的电离方程式:___________ 。
(4)使用过的腐蚀液会失效,但还可以回收利用,其中有一步需要将Fe2+转化为Fe3+,下列试剂能实现上述变化的是______(填序号)。
(5)若要由反应后的废液回收金属铜和得到较纯净的FeCl2溶液,你选择加入的物质是_______ 。
(1)请在上式中标出电子转移的方向和数目:
(2)上述反应中被氧化的元素是
(3)写出FeCl3的电离方程式:
(4)使用过的腐蚀液会失效,但还可以回收利用,其中有一步需要将Fe2+转化为Fe3+,下列试剂能实现上述变化的是______(填序号)。
| A.氯气 | B.铁 | C.双氧水 | D.稀硫酸 |
您最近一年使用:0次



