名校
1 . 下列“解释或结论”与“实验操作及现象”不对应的是
| 选项 | 实验操作及现象 | 解释或结论 |
| A | 向某钠盐溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的气体 | 该盐一定是 |
| B | 将氯气通入淀粉碘化钾溶液中,溶液有无色变为蓝色 | 氯气的氧化性强于碘单质 |
| C | 向某溶液中加入稀盐酸无明显现象,再加入 溶液,有白色沉淀生成 溶液,有白色沉淀生成 | 该溶液中一定含有 |
| D | 将点燃的氢气放入盛有氯气的集气瓶中,火焰呈苍白色,且有大量白雾产生 | 燃烧不一定需要 参与 参与 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . “曾青得铁则化为铜”涉及反应的离子方程式为: ,这是现代湿法冶金的基础。下列关于该反应的叙述正确的是
,这是现代湿法冶金的基础。下列关于该反应的叙述正确的是
 ,这是现代湿法冶金的基础。下列关于该反应的叙述正确的是
,这是现代湿法冶金的基础。下列关于该反应的叙述正确的是A.该反应中 被氧化 被氧化 |
| B.该反应属于有离子参加的置换反应 |
| C.该反应说明Fe的金属活动性比Cu的弱 |
| D.该反应说明金属单质都能与盐发生反应 |
您最近一年使用:0次
解题方法
3 . 按F2、Cl2、Br2、I2顺序,下列说法错误的是
| A.颜色由深变浅 | B.氧化性逐渐减弱 |
| C.与氢气化合由易变难 | D.密度逐渐增大 |
您最近一年使用:0次
名校
解题方法
4 . 反应 可用于制备金属钼(Mo)。下列关于该反应的说法不正确的是
可用于制备金属钼(Mo)。下列关于该反应的说法不正确的是
 可用于制备金属钼(Mo)。下列关于该反应的说法不正确的是
可用于制备金属钼(Mo)。下列关于该反应的说法不正确的是| A.Al的还原性比Mo强 | B.Mo为还原产物 |
| C.Al得到电子 | D. 发生还原反应 发生还原反应 |
您最近一年使用:0次
2022-12-27更新
|
480次组卷
|
5卷引用:江苏省2022-2023学年高二上学期学业水平合格性模拟预测(一)化学试题
江苏省2022-2023学年高二上学期学业水平合格性模拟预测(一)化学试题江苏省涟水县第一中学2022-2023学年高二上学期学业水平合格性考试化学试题(已下线)专题七 氧化还原反应(已下线)合格考汇编3氧化还原反应广东省湛江市第二十一中学2023-2024学年高一下学期第一次月考化学(学考)试题
解题方法
5 . 下列关于钠的叙述中,不正确 的是
| A.钠具有很强的还原性 | B.钠燃烧时发出黄色的火焰 |
| C.钠原子的最外层只有1个电子 | D.钠离子具有很强的氧化性 |
您最近一年使用:0次
解题方法
6 . 某化学课外小组用海带为原料制取少量单质,实验流程如下:

请回答下列问题:
(1)①实验步骤Ⅰ会用到下列仪器中的_______ (填字母);
a.酒精灯 b.漏斗 c.坩埚 d.泥三角
②步骤Ⅲ所采用的分离方法是_______ (填“过滤”或“蒸馏”);
③步骤Ⅳ说明氧化性:Cl2_______ (填“>”或“<”)I2。
(2)一定条件下,工业上可利用H2和I2反应生成HI,反应的化学方程式为H2(g)+I2(g) 2HI(g)。将1mol I2(g)和1mol H2置于1L的密闭容器中,10min后测得I2(g)为0.3 mol。则:
2HI(g)。将1mol I2(g)和1mol H2置于1L的密闭容器中,10min后测得I2(g)为0.3 mol。则:
①用I2(g)表示该反应的速率为_______ mol·L-1·min-1;
②其他条件不变时,再通入1mol H2,该反应的速率将_______ (填“增大”“不变”或“减小”)。

请回答下列问题:
(1)①实验步骤Ⅰ会用到下列仪器中的
a.酒精灯 b.漏斗 c.坩埚 d.泥三角
②步骤Ⅲ所采用的分离方法是
③步骤Ⅳ说明氧化性:Cl2
(2)一定条件下,工业上可利用H2和I2反应生成HI,反应的化学方程式为H2(g)+I2(g)
 2HI(g)。将1mol I2(g)和1mol H2置于1L的密闭容器中,10min后测得I2(g)为0.3 mol。则:
2HI(g)。将1mol I2(g)和1mol H2置于1L的密闭容器中,10min后测得I2(g)为0.3 mol。则:①用I2(g)表示该反应的速率为
②其他条件不变时,再通入1mol H2,该反应的速率将
您最近一年使用:0次
7 . 某实验小组欲通过加热蒸发KNO3溶液的方法获得KNO3固体。已知KNO3固体在一定温度下能够发生反应:2KNO3 2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。
2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。
【查阅资料】
ⅰ.AgNO2是微溶于水的白色(略带黄色)固体
ⅱ.KNO2能在酸性条件下与KI反应,生成I2
【实验过程】
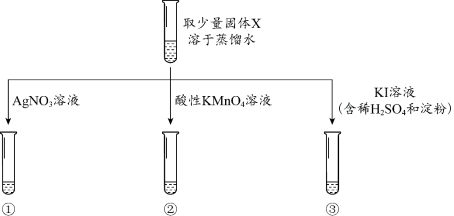
【分析解释】
(1)实验①中,观察到有少量白色沉淀生成,该白色沉淀是_______ 。
(2)实验②中,观察到酸性KMnO4溶液紫红色褪去,利用对比实验排除了稀释对溶液颜色变化的影响。补全该反应的离子方程式:2MnO + 5NO
+ 5NO + 6H+ = 2Mn2+ +
+ 6H+ = 2Mn2+ +_______ + 3H2O
(3)实验③中,观察到溶液变为蓝色。实验③中选择KI溶液的依据是_______ (填字母)。
a.KNO2具有氧化性,KI具有还原性
b.KNO2具有还原性,KI具有氧化性
【反思评价】
(4)综合上述实验,甲同学认为,实验①、②、③均可以证明固体X中含有KNO2;乙同学认为,通过实验③不能证明固体X中含有KNO2。乙同学的理由是_______ 。
 2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。
2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。【查阅资料】
ⅰ.AgNO2是微溶于水的白色(略带黄色)固体
ⅱ.KNO2能在酸性条件下与KI反应,生成I2
【实验过程】

【分析解释】
(1)实验①中,观察到有少量白色沉淀生成,该白色沉淀是
(2)实验②中,观察到酸性KMnO4溶液紫红色褪去,利用对比实验排除了稀释对溶液颜色变化的影响。补全该反应的离子方程式:2MnO
 + 5NO
+ 5NO + 6H+ = 2Mn2+ +
+ 6H+ = 2Mn2+ +(3)实验③中,观察到溶液变为蓝色。实验③中选择KI溶液的依据是
a.KNO2具有氧化性,KI具有还原性
b.KNO2具有还原性,KI具有氧化性
【反思评价】
(4)综合上述实验,甲同学认为,实验①、②、③均可以证明固体X中含有KNO2;乙同学认为,通过实验③不能证明固体X中含有KNO2。乙同学的理由是
您最近一年使用:0次
2022-04-15更新
|
283次组卷
|
2卷引用:北京市2021-2022学年高三年级下学期合格考(第一次)化学试题
8 . 海水是一个巨大的化学资源宝库。实验室模拟从海水中提取溴,设计实验流程如下:
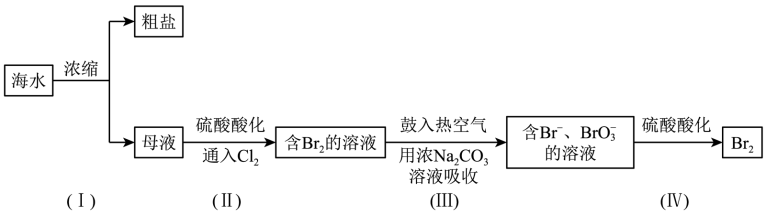
(1)海水中的溴元素存在形式是___________ (填“游离态”或“化合态”)。
(2)步骤(Ⅰ)中分离粗盐和母液的操作名称是___________ ,该操作使用的玻璃仪器有烧杯、玻璃棒和___________ 。
(3)写出步骤(Ⅱ)中 和
和 反应的离子方程式:
反应的离子方程式:___________ ,可推断氧化性:
___________  (填“>”或“<”)。
(填“>”或“<”)。
(4)步骤(Ⅲ)中鼓入热空气可将溴单质分离出来,是利用溴单质的___________ 性。
(5)步骤(Ⅳ)中主要反应的离子方程式为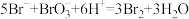 ,该反应的还原剂是
,该反应的还原剂是___________ 。

(1)海水中的溴元素存在形式是
(2)步骤(Ⅰ)中分离粗盐和母液的操作名称是
(3)写出步骤(Ⅱ)中
 和
和 反应的离子方程式:
反应的离子方程式:
 (填“>”或“<”)。
(填“>”或“<”)。(4)步骤(Ⅲ)中鼓入热空气可将溴单质分离出来,是利用溴单质的
(5)步骤(Ⅳ)中主要反应的离子方程式为
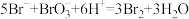 ,该反应的还原剂是
,该反应的还原剂是
您最近一年使用:0次
2022-01-01更新
|
543次组卷
|
3卷引用:2021年6月福建省普通高中学业水平合格性考试化学试题
解题方法
9 . 将氯水分别滴加到盛有等浓度的KI溶液、NaBr溶液的试管中,对比观察。通过此实验能够观察到的现象或得出的结论正确的是( )
| A.两支试管中溶液均呈紫色 |
| B.可证明还原性强弱:I->Br- |
| C.可证明氧化性强弱:Cl2>Br2>I2 |
| D.可证明Cl2的氧化性强于Br2和I2 |
您最近一年使用:0次
2020-07-11更新
|
742次组卷
|
6卷引用:天津市南开区2020届高中学业水平合格性考试模拟试卷化学试题
天津市南开区2020届高中学业水平合格性考试模拟试卷化学试题(已下线)第二章 海水中的重要元素——钠和氯(能力提升)-2020-2021学年高一化学单元测试定心卷(人教版2019必修第一册)(已下线)2.2.1氯气的性质(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)天津市东丽区2020-2021学年高一下学期期末考试化学试题(已下线)易错专题16 氯水的成分及性质-【突破易错·冲刺满分】2021-2022学年高一上学期化学期中期末易错专题(人教版2019)(已下线)专题七 氧化还原反应
名校
解题方法
10 . 已知Pb3O4与HNO3溶液发生反应I:Pb3O4+4H+ =PbO2+2Pb2++2H2O;PbO2与酸化的MnSO4溶液发生反应II:5PbO2+2Mn2++4H++5 =2
=2 +5PbSO4+2H2O。下列推断正确的是
+5PbSO4+2H2O。下列推断正确的是
 =2
=2 +5PbSO4+2H2O。下列推断正确的是
+5PbSO4+2H2O。下列推断正确的是| A.由反应I可知,Pb3O4中Pb(II)和Pb(IV)含量之比为2:1 |
B.由反应I、II可知,氧化性:HNO3>PbO2>MnO |
| C.Pb可与稀硝酸发生反应:3Pb+16HNO3=3Pb(NO3)4+4NO↑+8H2O |
| D.Pb3O4可与盐酸发生反应:Pb3O4+8HCl=3PbCl2+4H2O+Cl2↑ |
您最近一年使用:0次
2020-10-10更新
|
642次组卷
|
7卷引用:山东省2020年普通高中学业水平等级考试模拟试题



