1 . 某红色固体粉末样品可能含有Fe2O3和Cu2O中的一种或两种,某校化学自主探究实验小组拟对其组成进行探究。
查阅资料:Cu2O在酸性溶液中会发生反应:Cu2O+2H+=Cu+Cu2++H2O
探究一:用下图所示装置进行实验,回答下列问题:

(1)仪器组装完成后,夹好止水夹,___________ 。则说明装置A的气密性良好。
(2)装置A是氢气的发生装置,可以选用的药品是___________(填选项)
(3)从下列实验步骤中,选择正确的操作顺序:①___________ ③(填序号)
① 打开止水夹
② 熄灭C处的酒精喷灯
③ C处冷却至室温后,关闭止水夹
④ 点燃C处的酒精喷灯
⑤ 收集氢气并验纯
⑥ 通入气体一段时间,排尽装置内的空气
(4)收集氢气验纯时,最好采用___________ 方法收集氢气。
探究二:
(5)取少量样品于试管中,加入适量的稀硫酸,若无红色物质生成,则说明样品中不含Cu2O;此观点是否正确___________ 。(填“是”或“否”)若填“否”,则原因是___________ (用离子方程式说明);另取少量样品于试管中,加入适量的浓硝酸,产生红棕色的气体。
证明样品中一定含有___________ ,取少量反应后的溶液,加适量蒸馏水稀释后,滴加___________ (填试剂和实验现象),则可证明另一成分存在,反之,说明样品中不含该成分。
探究三:
(6)取一定量样品于烧杯中,加入足量的稀硫酸,若反应后经过滤得到固体3.2g,滤液中Fe2+有1.0mol,则样品中n(Cu2O)=___________ mol。
查阅资料:Cu2O在酸性溶液中会发生反应:Cu2O+2H+=Cu+Cu2++H2O
探究一:用下图所示装置进行实验,回答下列问题:

(1)仪器组装完成后,夹好止水夹,
(2)装置A是氢气的发生装置,可以选用的药品是___________(填选项)
| A.稀硫酸和锌片 | B.稀硝酸和铁片 | C.氢氧化钠溶液和铝片D.浓硫酸和镁片 |
① 打开止水夹
② 熄灭C处的酒精喷灯
③ C处冷却至室温后,关闭止水夹
④ 点燃C处的酒精喷灯
⑤ 收集氢气并验纯
⑥ 通入气体一段时间,排尽装置内的空气
(4)收集氢气验纯时,最好采用
探究二:
(5)取少量样品于试管中,加入适量的稀硫酸,若无红色物质生成,则说明样品中不含Cu2O;此观点是否正确
证明样品中一定含有
探究三:
(6)取一定量样品于烧杯中,加入足量的稀硫酸,若反应后经过滤得到固体3.2g,滤液中Fe2+有1.0mol,则样品中n(Cu2O)=
您最近一年使用:0次
解题方法
2 . 向 由铁粉和铜粉组成的混合物中,加入某浓度的稀硝酸,充分反应后测得生成
由铁粉和铜粉组成的混合物中,加入某浓度的稀硝酸,充分反应后测得生成 的体积
的体积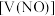 (已换算成标准状况下)、m(固体剩余质量)随加入的稀硝酸的体积的变化如图所示(设硝酸的还原产物只有
(已换算成标准状况下)、m(固体剩余质量)随加入的稀硝酸的体积的变化如图所示(设硝酸的还原产物只有 )。下列说法中正确的是
)。下列说法中正确的是
 由铁粉和铜粉组成的混合物中,加入某浓度的稀硝酸,充分反应后测得生成
由铁粉和铜粉组成的混合物中,加入某浓度的稀硝酸,充分反应后测得生成 的体积
的体积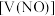 (已换算成标准状况下)、m(固体剩余质量)随加入的稀硝酸的体积的变化如图所示(设硝酸的还原产物只有
(已换算成标准状况下)、m(固体剩余质量)随加入的稀硝酸的体积的变化如图所示(设硝酸的还原产物只有 )。下列说法中正确的是
)。下列说法中正确的是
A.a点时, 稀硝酸中溶解了 稀硝酸中溶解了 粉 粉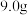 |
B.稀硝酸的浓度为 |
C.加入稀硝酸的体积从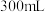 至 至 ,期间收集到 ,期间收集到 的体积约为 的体积约为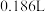 |
D.b点对应的溶液中可能含有的金属阳离子为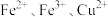 |
您最近一年使用:0次
3 . 向 和
和 的混合溶液中不断通入
的混合溶液中不断通入 ,溶液中n(含碘的某微粒)和n(含铁的某微粒)随
,溶液中n(含碘的某微粒)和n(含铁的某微粒)随 的变化曲线如图所示。(已知:①
的变化曲线如图所示。(已知:① 可将
可将 氧化成
氧化成 ;②
;②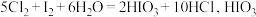 为强酸)下列说法中错误的是
为强酸)下列说法中错误的是

 和
和 的混合溶液中不断通入
的混合溶液中不断通入 ,溶液中n(含碘的某微粒)和n(含铁的某微粒)随
,溶液中n(含碘的某微粒)和n(含铁的某微粒)随 的变化曲线如图所示。(已知:①
的变化曲线如图所示。(已知:① 可将
可将 氧化成
氧化成 ;②
;②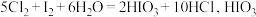 为强酸)下列说法中错误的是
为强酸)下列说法中错误的是
A.还原性: |
B.b点溶液中 |
C.a点时已通入标准状况下氯气的总体积为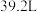 |
D.c点溶液中阴离子的个数为 |
您最近一年使用:0次
2023-12-01更新
|
902次组卷
|
4卷引用:广东省深圳市七校2023-2024学年高一上学期期中联考化学试题
名校
4 . 将 铜镁合金完全溶解于
铜镁合金完全溶解于 某浓度的硝酸中,得到标准状况下
某浓度的硝酸中,得到标准状况下 和
和 的混合气体,向反应后的溶液中加入
的混合气体,向反应后的溶液中加入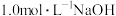 溶液
溶液 ,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为
,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为 。下列说法错误的是
。下列说法错误的是
 铜镁合金完全溶解于
铜镁合金完全溶解于 某浓度的硝酸中,得到标准状况下
某浓度的硝酸中,得到标准状况下 和
和 的混合气体,向反应后的溶液中加入
的混合气体,向反应后的溶液中加入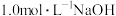 溶液
溶液 ,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为
,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为 。下列说法错误的是
。下列说法错误的是A.该硝酸的物质的量浓度为 |
B.合金中铜与镁的物质的量之比为 |
C.混合气体中 和 和 的体积之比为 的体积之比为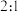 |
D.铜镁合金溶解后,溶液中剩余 的物质的量为 的物质的量为 |
您最近一年使用:0次
2024-01-30更新
|
402次组卷
|
2卷引用:山东省烟台市2023-2024学年高一上学期期末考试化学试题
名校
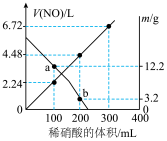
5 . 向mg由铁粉和铜粉组成的混合物中,加入某浓度的稀硝酸,充分反应后测得生成NO的体积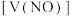 (已换算成标准状况下)、m(固体剩余质量)随加入的稀硝酸的体积的变化如图所示(设硝酸的还原产物只有NO)。下列说法中正确的是
(已换算成标准状况下)、m(固体剩余质量)随加入的稀硝酸的体积的变化如图所示(设硝酸的还原产物只有NO)。下列说法中正确的是
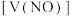 (已换算成标准状况下)、m(固体剩余质量)随加入的稀硝酸的体积的变化如图所示(设硝酸的还原产物只有NO)。下列说法中正确的是
(已换算成标准状况下)、m(固体剩余质量)随加入的稀硝酸的体积的变化如图所示(设硝酸的还原产物只有NO)。下列说法中正确的是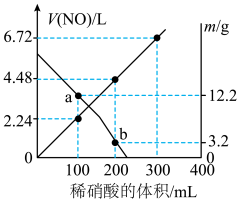
| A.a点时,100mL稀硝酸中溶解了Fe粉5.6g |
B.稀硝酸的浓度为 |
| C.加入稀硝酸的体积从300mL至400mL,期间收集产生的NO物质的量约为0.0083mol |
D.b点对应的溶液中可能含有的金属阳离子为 、 、 和 和 |
您最近一年使用:0次
名校
解题方法
6 . 取某铁铝铜合金9.34g,溶于足量的稀硝酸中,金属无剩余,收集到的一种气体是唯一还原产物。向溶液中加过量的氢氧化钠溶液,小心收集沉淀洗涤干净称重11.23g,加热分解至衡重,得固体质量为8.80g。则下列说法不正确的是
| A.参加反应的氢氧化钠不一定比参加反应的硝酸的物质的量多 |
| B.合金中铁铝的物质的量之比为1:2 |
| C.收集到的气体在标准状况下为4.256L |
| D.与铁铝铜合金反应的硝酸的物质的量是0.57mol |
您最近一年使用:0次
解题方法
7 . 将一定量铁粉和铜粉混合均匀后分为四等份,分别加入同浓度的稀硝酸,充分反应,在标准状况下生成 的体积和剩余金属的质量如表所示(设
的体积和剩余金属的质量如表所示(设 的还原产物只有
的还原产物只有 ):
):
下列说法错误的是
 的体积和剩余金属的质量如表所示(设
的体积和剩余金属的质量如表所示(设 的还原产物只有
的还原产物只有 ):
):| 实验序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
稀硝酸的体积/ | 50 | 100 | 150 | 175 |
| 剩余金属的质量/g | 9.0 | 4.8 | 0 | 0 |
 的体积(标准状况)/ 的体积(标准状况)/ | 1120 | 2240 | 3360 | V |
A.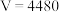 |
B.每等份混合物的质量为 |
C.稀硝酸的物质的量的浓度为 |
D.实验Ⅰ中发生反应的化学方程式为 |
您最近一年使用:0次
2023-04-27更新
|
745次组卷
|
2卷引用:河北省邢台市2022-2023学年高一下学期期中考试化学试题
名校
解题方法
8 . 将1.52 g铜镁合金完全溶解于50 mL密度为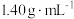 、质量分数为63%的浓硝酸中,得到
、质量分数为63%的浓硝酸中,得到 和
和 的混合气体0.05 mol,向反应后的溶液中加入
的混合气体0.05 mol,向反应后的溶液中加入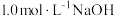 溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法不正确的是
溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法不正确的是
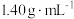 、质量分数为63%的浓硝酸中,得到
、质量分数为63%的浓硝酸中,得到 和
和 的混合气体0.05 mol,向反应后的溶液中加入
的混合气体0.05 mol,向反应后的溶液中加入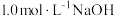 溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法不正确的是
溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法不正确的是| A.该合金中铜与镁的物质的量之比是2:1 |
B.该浓硝酸中 的物质的量浓度是 的物质的量浓度是 |
C. 和 和 的混合气体中, 的混合气体中, 的体积分数是20% 的体积分数是20% |
| D.得到2.54 g沉淀时,加入NaOH溶液的体积是660 mL |
您最近一年使用:0次
名校
解题方法
9 . 1.52g铜镁合金完全溶解于50mL14mol/L的浓硝酸中,得到NO2和NO的混合气体896mL(标准状况),向反应后的溶液中加入1.0mol·L-1NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀。下列说法不正确的是
| A.该合金中铜与镁的物质的量之比是2∶1 |
| B.固体溶解后的溶液中硝酸的物质的量为0.6mol |
| C.得到2.54g沉淀时,加入NaOH溶液的体积至少为600mL |
| D.反应过程中转移的电子数是0.06NA(NA代表阿伏加德罗常数的值) |
您最近一年使用:0次
名校
解题方法
10 . 如图所示,实验室中利用洁净的铜片(0.3 mol)和浓硫酸进行反应,实验中无气体生成,Y型管左侧得到Cu2S和白色固体a,倾斜Y型管使左侧的物质全部转移到右侧稀硝酸中,反应生成固体单质b、a的溶液和NO。下列说法错误的是
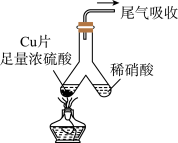

| A.白色固体为CuSO4 |
| B.NO为还原产物,b为氧化产物 |
| C.NO与b的物质的量之和可能为0.2 mol |
| D.参加反应的浓硫酸中,表现氧化性的占25% |
您最近一年使用:0次
2023-05-16更新
|
1221次组卷
|
3卷引用:山东省烟台市2022-2023学年高一上学期期末考试化学试题



