1 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.质量均为13g的 和 和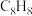 中含有的C原子数均为 中含有的C原子数均为 |
B. 的苯甲酸钠溶液中含有苯甲酸根离子的数目小于 的苯甲酸钠溶液中含有苯甲酸根离子的数目小于 |
C. 是正四面体网状结构,则 是正四面体网状结构,则 中含有的Si-O键数为 中含有的Si-O键数为 |
D.当氧化产物为 时,每生成22.4L(标准状况) 时,每生成22.4L(标准状况) 转移的电子数为 转移的电子数为 |
您最近一年使用:0次
解题方法
2 . 设NA为阿伏加德罗常数的值。下列说法正确的是
| A.5.6gFe与硫完全反应时失电子总数为0.8NA |
| B.电解精炼粗铜时,当阴极增重6.4g时,电解质溶液中Cu2+增加0.1NA |
| C.100g46%的乙醇溶液中含有氧原子总数为3NA |
| D.14g乙烯和21g丙烯的混合气体中含有C-H共价键的数目为5NA |
您最近一年使用:0次
名校
3 . 我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑。下列说法错误的是
| A.氧化剂是KNO3和S |
| B.木炭被氧化 |
| C.每生成1mol的CO2转移8NA个电子 |
| D.KNO3的氧化性强于CO2 |
您最近一年使用:0次
2024-03-12更新
|
82次组卷
|
2卷引用:青海省西宁市海湖中学2023-2024学年高一下学期开学考试化学试卷
4 . 实验室用白磷和浓硝酸反应制备磷酸并探究产物的性质,装置如图所示。回答下列问题:
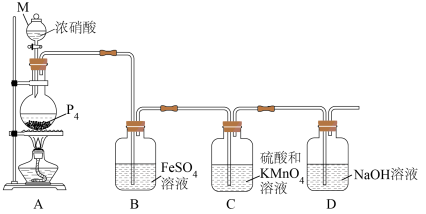
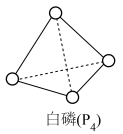
(1)白磷呈正四面体形结构(如图), 含
含_____  共价键;实验室中少量
共价键;实验室中少量 保存在
保存在________ 。
(2)仪器 的名称是
的名称是_________ ,仪器 在使用前应该先
在使用前应该先_________ 。
(3)已知 和浓硝酸反应生成
和浓硝酸反应生成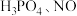 和
和 ,经检测产物中
,经检测产物中 和
和 的物质的量之比为
的物质的量之比为 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
(4) 装置中溶液褪色,氧化产物的阴离子为
装置中溶液褪色,氧化产物的阴离子为 ,写出
,写出 装置中发生反应的离子方程式:
装置中发生反应的离子方程式:________ 。
(5) 不能与
不能与 溶液反应,利用
溶液反应,利用 装置吸收尾气中的
装置吸收尾气中的 时,需要同时通入某种模拟空气
时,需要同时通入某种模拟空气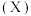 。若
。若 恰好完全被吸收,且氧化产物只有
恰好完全被吸收,且氧化产物只有 ,则同温同压下,
,则同温同压下,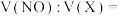
______ 。(设该模拟空气中氧气的体积分数为 )
)
(6)探究 装置中溶液呈棕黄色的原因,一课题小组提出如下猜想:
装置中溶液呈棕黄色的原因,一课题小组提出如下猜想:
猜想1:存在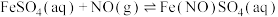 (棕黄色);
(棕黄色);
猜想2:生成了 。
。
针对猜想2设计实验:_________ (写出步骤、现象),猜想2成立。

(1)白磷呈正四面体形结构(如图),
 含
含 共价键;实验室中少量
共价键;实验室中少量 保存在
保存在
(2)仪器
 的名称是
的名称是 在使用前应该先
在使用前应该先(3)已知
 和浓硝酸反应生成
和浓硝酸反应生成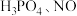 和
和 ,经检测产物中
,经检测产物中 和
和 的物质的量之比为
的物质的量之比为 ,该反应的化学方程式为
,该反应的化学方程式为(4)
 装置中溶液褪色,氧化产物的阴离子为
装置中溶液褪色,氧化产物的阴离子为 ,写出
,写出 装置中发生反应的离子方程式:
装置中发生反应的离子方程式:(5)
 不能与
不能与 溶液反应,利用
溶液反应,利用 装置吸收尾气中的
装置吸收尾气中的 时,需要同时通入某种模拟空气
时,需要同时通入某种模拟空气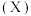 。若
。若 恰好完全被吸收,且氧化产物只有
恰好完全被吸收,且氧化产物只有 ,则同温同压下,
,则同温同压下,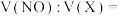
 )
)(6)探究
 装置中溶液呈棕黄色的原因,一课题小组提出如下猜想:
装置中溶液呈棕黄色的原因,一课题小组提出如下猜想:猜想1:存在
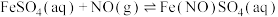 (棕黄色);
(棕黄色);猜想2:生成了
 。
。针对猜想2设计实验:
您最近一年使用:0次
名校
5 . 铁及其化合物在生产,生活中有着重要作用。按要求回答下列问题
(1)铁及其化合物的价类分布及转化关系如图所示:
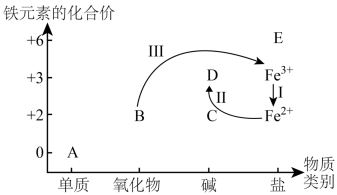
①氯化铁溶液常用于蚀刻铜制电路板,实现了反应Ⅰ的转化,写出反应的离子方程式:_____
②往氯化亚铁溶液中滴加氢氧化钠溶液的过程可实现E→C→D的转化,可观察到的现象为_____
③为实现反应Ⅲ的转化,可选择的试剂为稀硝酸,被还原的N和未被还原的N的物质的量之比为_____ 。
(2)探究某铁盐X的组成与性质(忽略过程中氧气的参与):
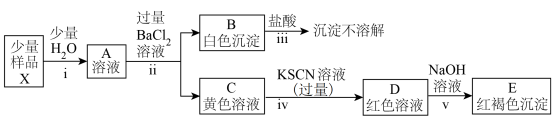
①由步骤ⅱ、ⅲ及其现象可推知该铁盐X中含有的阴离子为_____ (填离子符号)。
②根据步骤ⅳ、ⅴ及其现象分析,体系中与 结合能力最强的离子是
结合能力最强的离子是_____ (填“ ”或“
”或“ ”)。
”)。
(3)高铁酸钾( )是一种新型污水处理剂。可以次氯酸钠和氯化铁为原料,在碱性溶液中反应生成高铁酸钠,然后加入氢氧化钾,将高铁酸钠转化成高铁酸钾。
)是一种新型污水处理剂。可以次氯酸钠和氯化铁为原料,在碱性溶液中反应生成高铁酸钠,然后加入氢氧化钾,将高铁酸钠转化成高铁酸钾。
①写出生成高铁酸钠的反应的离子方程式:_____
②若反应过程中转移了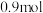 电子,则还原产物的物质的量为
电子,则还原产物的物质的量为_____ mol。
③低温下,向高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾( ),由此可说明溶解度:
),由此可说明溶解度:
_____ (填“>”“<”或“=”) 。
。
(1)铁及其化合物的价类分布及转化关系如图所示:

①氯化铁溶液常用于蚀刻铜制电路板,实现了反应Ⅰ的转化,写出反应的离子方程式:
②往氯化亚铁溶液中滴加氢氧化钠溶液的过程可实现E→C→D的转化,可观察到的现象为
③为实现反应Ⅲ的转化,可选择的试剂为稀硝酸,被还原的N和未被还原的N的物质的量之比为
(2)探究某铁盐X的组成与性质(忽略过程中氧气的参与):

①由步骤ⅱ、ⅲ及其现象可推知该铁盐X中含有的阴离子为
②根据步骤ⅳ、ⅴ及其现象分析,体系中与
 结合能力最强的离子是
结合能力最强的离子是 ”或“
”或“ ”)。
”)。(3)高铁酸钾(
 )是一种新型污水处理剂。可以次氯酸钠和氯化铁为原料,在碱性溶液中反应生成高铁酸钠,然后加入氢氧化钾,将高铁酸钠转化成高铁酸钾。
)是一种新型污水处理剂。可以次氯酸钠和氯化铁为原料,在碱性溶液中反应生成高铁酸钠,然后加入氢氧化钾,将高铁酸钠转化成高铁酸钾。①写出生成高铁酸钠的反应的离子方程式:
②若反应过程中转移了
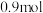 电子,则还原产物的物质的量为
电子,则还原产物的物质的量为③低温下,向高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(
 ),由此可说明溶解度:
),由此可说明溶解度:
 。
。
您最近一年使用:0次
2023-12-29更新
|
226次组卷
|
3卷引用:2024届青海省协作联考高三上学期一模理综试题
名校
6 . 锡是大名鼎鼎的“五金”——金、银、铜、铁、锡之一。早在远古时代,人们便发现并使用锡了。在我国的一些古墓中,便常发掘到一些锡壶、锡烛台之类锡器。

工业上冶炼锡的第一步反应原理为2SnO2+3C=2Sn+aM↑+CO2↑,则下列说法中错误的是( )

工业上冶炼锡的第一步反应原理为2SnO2+3C=2Sn+aM↑+CO2↑,则下列说法中错误的是( )
| A.反应中SnO2被还原 | B.每生成1个CO2,转移8个电子 |
| C.反应后元素化合价升高的物质有两种 | D.a的值为3 |
您最近一年使用:0次
2020-10-15更新
|
123次组卷
|
6卷引用:青海省西宁市海湖中学2023-2024学年高一下学期开学考试化学试卷
青海省西宁市海湖中学2023-2024学年高一下学期开学考试化学试卷山东省济宁市曲阜市第一中学2020-2021学年高一上学期10月月考化学试题云南省临沧市凤庆县第一中学2021-2022学年高一下学期3月份考试化学试题(已下线)第11讲 氧化还原反应的配平及应用-【暑假自学课】2023年新高一化学暑假精品课(鲁科版2019必修第一册)广西贵港市名校2023-2024学年高一上学期入学联考化学试题甘肃省武威市民勤县第一中学2023-2024学年高一上学期入学考试化学试题



