名校
1 . 滴定是一种重要的定量实验方法。现拟用KMnO4溶液去测定市场上售卖的草酸的纯度,步骤如下:(已知:M(H2C2O4)=90g·mol-1)
①称取1.260g草酸样品,将其制成100mL水溶液为待测液;
②取25.00mL待测液放入锥形瓶中,再加入适的稀H2SO4;
③用浓度为0.05000mol·L-1的KMnO4标准溶液进行滴定。
(1)请写出与滴定有关反应的离子方程式___________ 。
(2)滴定时盛装KMnO4标准溶液所用仪器为___________ 。
(3)由如图可知消耗KMnO4溶液体积为___________ mL。

(4)滴定终点的现象为___________ 。
(5)通过上述数据,求得草酸的纯度为___________ 。(精确度保留到0.1)
(6)误差分析:
①以标准KMnO4溶液滴定样品溶液的浓度时,未用标准KMnO4溶液润洗滴定管,引起实验结果___________ (偏大、偏小或无影响,下同);
②用酸式滴定管量取待测液时,未用待测液润洗滴定管,引起实验结果___________ ;
③滴定前有气泡,滴定后气泡消失,引起实验结果___________ ;
④滴定前正确读数,滴定后俯视,引起实验结果___________ 。
①称取1.260g草酸样品,将其制成100mL水溶液为待测液;
②取25.00mL待测液放入锥形瓶中,再加入适的稀H2SO4;
③用浓度为0.05000mol·L-1的KMnO4标准溶液进行滴定。
(1)请写出与滴定有关反应的离子方程式
(2)滴定时盛装KMnO4标准溶液所用仪器为
(3)由如图可知消耗KMnO4溶液体积为

(4)滴定终点的现象为
(5)通过上述数据,求得草酸的纯度为
(6)误差分析:
①以标准KMnO4溶液滴定样品溶液的浓度时,未用标准KMnO4溶液润洗滴定管,引起实验结果
②用酸式滴定管量取待测液时,未用待测液润洗滴定管,引起实验结果
③滴定前有气泡,滴定后气泡消失,引起实验结果
④滴定前正确读数,滴定后俯视,引起实验结果
您最近一年使用:0次
名校
2 . 已知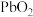 在盐酸溶液中易生成
在盐酸溶液中易生成 ,且
,且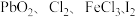 的氧化性依次减弱,下列叙述中,正确的是
的氧化性依次减弱,下列叙述中,正确的是
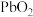 在盐酸溶液中易生成
在盐酸溶液中易生成 ,且
,且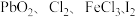 的氧化性依次减弱,下列叙述中,正确的是
的氧化性依次减弱,下列叙述中,正确的是A. 通入 通入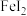 溶液中,可存在反应: 溶液中,可存在反应: |
B.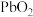 可能与浓盐酸反应生成 可能与浓盐酸反应生成 |
C. 溶液能将 溶液能将 溶液中的 溶液中的 还原成 还原成 |
D. 可能将 可能将 氧化成 氧化成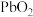 |
您最近一年使用:0次
3 . 氧化还原反应实际上包含氧化反应和还原反应两个过程,一个还原反应过程的离子方程式为NO3-+4H++3e-=NO↑+2H2O。下列四种物质:KMnO4、Na2CO3、KI、Fe2(SO4)3中的一种物质甲,滴加少量稀硝酸,能使上述反应过程发生。
(1)被还原的元素是_____ ,还原剂是_____ ;
(2)写出并配平该氧化还原反应方程式___________________ ;
(3)反应生成0.3mol H2O,则转移电子的数目为___________________ ;
(4)若反应后,氧化产物的化合价升高,而其他物质保持不变,则反应中氧化剂与还原剂的物质的量之比将___________________ (填“增大”“不变”“减小”或“不能确定”)。
(1)被还原的元素是
(2)写出并配平该氧化还原反应方程式
(3)反应生成0.3mol H2O,则转移电子的数目为
(4)若反应后,氧化产物的化合价升高,而其他物质保持不变,则反应中氧化剂与还原剂的物质的量之比将
您最近一年使用:0次
2020-10-26更新
|
484次组卷
|
2卷引用:陕西省渭南市临渭区尚德中学2021届高三第一次月考化学试题
名校
4 . FeCl3为黑棕色固体,无水氯化铁在300℃以上升华,遇潮湿空气极易潮解。
(1)甲组同学拟用下列装置制取纯净干燥的氯气。
①装置B的作用是_________
②装置A中发生反应时消耗的氧化剂和还原剂的物质的量之比为__________
(2)乙组同学选用甲组实验中的装置ABC和下列装置制取FeCl3

①乙组同学的实验装置中,依次连接的合理顺序为:a→_____ →_____ →_____ →_____ →_____ →_____
②连好装置,检查装置的气密性,先打开装置A中___________ (填仪器的名称)的活塞,直到______ 再点燃装置F处的酒精灯,目的是_______
③装置D的作用有_______
(3)实验结束后,取少量F中的固体加水溶解,欲对所得产物FeCl3中是否含有FeCl2进行检测,所需试剂是_______
a.KSCN b.H2O2 c.K3[Fe(CN)6] d. .K4[Fe(CN)6]
经检测发现溶液中含有Fe2+,丙同学认为所得产物FeCl3中一定含有FeCl2,丁同学认为不一定,理由是_____
(1)甲组同学拟用下列装置制取纯净干燥的氯气。
①装置B的作用是
②装置A中发生反应时消耗的氧化剂和还原剂的物质的量之比为
(2)乙组同学选用甲组实验中的装置ABC和下列装置制取FeCl3

①乙组同学的实验装置中,依次连接的合理顺序为:a→
②连好装置,检查装置的气密性,先打开装置A中
③装置D的作用有
(3)实验结束后,取少量F中的固体加水溶解,欲对所得产物FeCl3中是否含有FeCl2进行检测,所需试剂是
a.KSCN b.H2O2 c.K3[Fe(CN)6] d. .K4[Fe(CN)6]
经检测发现溶液中含有Fe2+,丙同学认为所得产物FeCl3中一定含有FeCl2,丁同学认为不一定,理由是
您最近一年使用:0次



