名校
解题方法
1 . 下列对应离子方程式的书写正确的是
A.将 (少量)通入 (少量)通入 溶液中: 溶液中: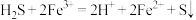 |
B.向 溶液中滴加稀氨水: 溶液中滴加稀氨水: |
C.向 溶液中滴加少量稀盐酸: 溶液中滴加少量稀盐酸: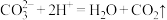 |
D.向 溶液中滴加少量澄清石灰水: 溶液中滴加少量澄清石灰水: |
您最近半年使用:0次
2024-03-08更新
|
137次组卷
|
4卷引用:2024届陕西省西安市浐灞第二中学高三下学期理科综合模拟试卷-高中化学
名校
2 . 滴定是一种重要的定量实验方法。现拟用KMnO4溶液去测定市场上售卖的草酸的纯度,步骤如下:(已知:M(H2C2O4)=90g·mol-1)
①称取1.260g草酸样品,将其制成100mL水溶液为待测液;
②取25.00mL待测液放入锥形瓶中,再加入适的稀H2SO4;
③用浓度为0.05000mol·L-1的KMnO4标准溶液进行滴定。
(1)请写出与滴定有关反应的离子方程式___________ 。
(2)滴定时盛装KMnO4标准溶液所用仪器为___________ 。
(3)由如图可知消耗KMnO4溶液体积为___________ mL。

(4)滴定终点的现象为___________ 。
(5)通过上述数据,求得草酸的纯度为___________ 。(精确度保留到0.1)
(6)误差分析:
①以标准KMnO4溶液滴定样品溶液的浓度时,未用标准KMnO4溶液润洗滴定管,引起实验结果___________ (偏大、偏小或无影响,下同);
②用酸式滴定管量取待测液时,未用待测液润洗滴定管,引起实验结果___________ ;
③滴定前有气泡,滴定后气泡消失,引起实验结果___________ ;
④滴定前正确读数,滴定后俯视,引起实验结果___________ 。
①称取1.260g草酸样品,将其制成100mL水溶液为待测液;
②取25.00mL待测液放入锥形瓶中,再加入适的稀H2SO4;
③用浓度为0.05000mol·L-1的KMnO4标准溶液进行滴定。
(1)请写出与滴定有关反应的离子方程式
(2)滴定时盛装KMnO4标准溶液所用仪器为
(3)由如图可知消耗KMnO4溶液体积为

(4)滴定终点的现象为
(5)通过上述数据,求得草酸的纯度为
(6)误差分析:
①以标准KMnO4溶液滴定样品溶液的浓度时,未用标准KMnO4溶液润洗滴定管,引起实验结果
②用酸式滴定管量取待测液时,未用待测液润洗滴定管,引起实验结果
③滴定前有气泡,滴定后气泡消失,引起实验结果
④滴定前正确读数,滴定后俯视,引起实验结果
您最近半年使用:0次
3 . 化学与人类生产、生活密切相关,按要求回答下列问题。
(1)工业上制造光导纤维的基本原料是_______ (填化学式)。
(2)钠的化合物中,可用作潜水艇中供氧剂的是_______ ,其与 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
(3)饮用水质量是关系人类健康的重要问题。暴雨过后,井水混浊无法饮用。为了能让井水变澄清,可向井水中投入_______(填字母)。
(4)工业上以氯气和石灰乳为原料制造漂白粉,漂白粉的有效成分是_______ (填化学式)。
(5)新型陶瓷氮化铝可用氧化铝高温还原法制备: (未配平),配平该化学反应方程式并用单线桥法标出电子转移的方向和数目
(未配平),配平该化学反应方程式并用单线桥法标出电子转移的方向和数目_______ 。若反应中共转移 个电子,则产生
个电子,则产生 气体的体积为
气体的体积为_______ L(标准状况下)。
(1)工业上制造光导纤维的基本原料是
(2)钠的化合物中,可用作潜水艇中供氧剂的是
 发生反应的化学方程式为
发生反应的化学方程式为(3)饮用水质量是关系人类健康的重要问题。暴雨过后,井水混浊无法饮用。为了能让井水变澄清,可向井水中投入_______(填字母)。
A. | B. | C. | D. |
(5)新型陶瓷氮化铝可用氧化铝高温还原法制备:
 (未配平),配平该化学反应方程式并用单线桥法标出电子转移的方向和数目
(未配平),配平该化学反应方程式并用单线桥法标出电子转移的方向和数目 个电子,则产生
个电子,则产生 气体的体积为
气体的体积为
您最近半年使用:0次
2023-07-31更新
|
357次组卷
|
4卷引用:陕西省汉中市2020-2021学年高一上学期期末考试化学试题
陕西省汉中市2020-2021学年高一上学期期末考试化学试题(已下线)结构与性质(已下线)期末测试卷02-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册) 2023-2024学年高一上学期化学人教版(2019)必修第一册 期末综合测试题(一)
解题方法
4 . 消毒剂在生活中应用广泛, 、
、 、
、 、
、 、
、 是生活中不同领域的消毒剂。根据下列反应回答问题:
是生活中不同领域的消毒剂。根据下列反应回答问题:
①
②
③ (未配平)
(未配平)
④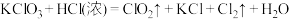 (未配平)
(未配平)
(1)储存过氧化氢的试剂瓶上最适合贴上的标签是_____(填字母)。
(2)反应①中,氧化剂与还原剂的物质的量之比为_____ 。
(3)反应②中,当有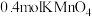 参加反应时,做酸性介质的
参加反应时,做酸性介质的 的物质的量为
的物质的量为_____  。
。
(4)配平并用双线桥法表示反应③中电子转移的方向和数目_____ 。
(5)若反应④中有 (标准状况下)氯气生成,则转移的电子数为
(标准状况下)氯气生成,则转移的电子数为_____
(6)某强酸反应体系中会发生氧化还原反应,反应物和生成物共六种微粒: 、
、 、
、 、
、 、
、 、
、 ,已知该反应中
,已知该反应中 只发生过程
只发生过程 。
。
i.该反应体系选择的酸是_____ (填字母)。
A盐酸 B.稀硫酸 C.醋酸
ii.该反应的离子方程式为_____ 。
 、
、 、
、 、
、 、
、 是生活中不同领域的消毒剂。根据下列反应回答问题:
是生活中不同领域的消毒剂。根据下列反应回答问题:①

②

③
 (未配平)
(未配平)④
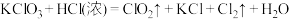 (未配平)
(未配平)(1)储存过氧化氢的试剂瓶上最适合贴上的标签是_____(填字母)。
A. | B. |
C. | D. |
(3)反应②中,当有
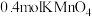 参加反应时,做酸性介质的
参加反应时,做酸性介质的 的物质的量为
的物质的量为 。
。(4)配平并用双线桥法表示反应③中电子转移的方向和数目
(5)若反应④中有
 (标准状况下)氯气生成,则转移的电子数为
(标准状况下)氯气生成,则转移的电子数为(6)某强酸反应体系中会发生氧化还原反应,反应物和生成物共六种微粒:
 、
、 、
、 、
、 、
、 、
、 ,已知该反应中
,已知该反应中 只发生过程
只发生过程 。
。i.该反应体系选择的酸是
A盐酸 B.稀硫酸 C.醋酸
ii.该反应的离子方程式为
您最近半年使用:0次
名校
5 . 已知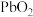 在盐酸溶液中易生成
在盐酸溶液中易生成 ,且
,且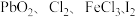 的氧化性依次减弱,下列叙述中,正确的是
的氧化性依次减弱,下列叙述中,正确的是
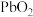 在盐酸溶液中易生成
在盐酸溶液中易生成 ,且
,且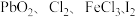 的氧化性依次减弱,下列叙述中,正确的是
的氧化性依次减弱,下列叙述中,正确的是A. 通入 通入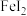 溶液中,可存在反应: 溶液中,可存在反应: |
B.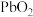 可能与浓盐酸反应生成 可能与浓盐酸反应生成 |
C. 溶液能将 溶液能将 溶液中的 溶液中的 还原成 还原成 |
D. 可能将 可能将 氧化成 氧化成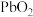 |
您最近半年使用:0次
6 . 氧化还原反应实际上包含氧化反应和还原反应两个过程,一个还原反应过程的离子方程式为NO3-+4H++3e-=NO↑+2H2O。下列四种物质:KMnO4、Na2CO3、KI、Fe2(SO4)3中的一种物质甲,滴加少量稀硝酸,能使上述反应过程发生。
(1)被还原的元素是_____ ,还原剂是_____ ;
(2)写出并配平该氧化还原反应方程式___________________ ;
(3)反应生成0.3mol H2O,则转移电子的数目为___________________ ;
(4)若反应后,氧化产物的化合价升高,而其他物质保持不变,则反应中氧化剂与还原剂的物质的量之比将___________________ (填“增大”“不变”“减小”或“不能确定”)。
(1)被还原的元素是
(2)写出并配平该氧化还原反应方程式
(3)反应生成0.3mol H2O,则转移电子的数目为
(4)若反应后,氧化产物的化合价升高,而其他物质保持不变,则反应中氧化剂与还原剂的物质的量之比将
您最近半年使用:0次
2020-10-26更新
|
483次组卷
|
2卷引用:陕西省渭南市临渭区尚德中学2021届高三第一次月考化学试题
名校
解题方法
7 . 利用铝热反应原理可以制取金属锰,化学方程式为3MnO2+4Al 3Mn+2Al2O3,该反应的氧化剂是( )
3Mn+2Al2O3,该反应的氧化剂是( )
 3Mn+2Al2O3,该反应的氧化剂是( )
3Mn+2Al2O3,该反应的氧化剂是( )| A.MnO2 | B.Al | C.Mn | D.Al2O3 |
您最近半年使用:0次
2020-03-09更新
|
483次组卷
|
10卷引用:陕西省吴起高级中学2019-2020学年高一上学期期中考试化学(能力卷)试题
陕西省吴起高级中学2019-2020学年高一上学期期中考试化学(能力卷)试题湖南省普通高中2016-2017学年高二学业水平考试模拟化学试题云南省云天化中学2019-2020学年高一9月月考化学试题湖南省邵东县创新实验学校2019-2020学年高二上学期期中考试化学(文)试题湖南省永州市双牌县第二中学2019-2020学年高二上学期期中考试化学试题(学考)广东省潮州市潮安区龙溪中学2019-2020学年上学期普通高中学业水平测试合格考化学试题2015年湖南省普通高中学业水平考试化学试题湖南省益阳市箴言中学2019-2020学年高二上学期期末学业水平考试化学试题河北省衡水市武强中学2020-2021学年高一上学期第三次月考化学试题湖南省2020-2021学年普通高中学业水平合格性考试模拟化学试题
名校
8 . FeCl3为黑棕色固体,无水氯化铁在300℃以上升华,遇潮湿空气极易潮解。
(1)甲组同学拟用下列装置制取纯净干燥的氯气。
①装置B的作用是_________
②装置A中发生反应时消耗的氧化剂和还原剂的物质的量之比为__________
(2)乙组同学选用甲组实验中的装置ABC和下列装置制取FeCl3

①乙组同学的实验装置中,依次连接的合理顺序为:a→_____ →_____ →_____ →_____ →_____ →_____
②连好装置,检查装置的气密性,先打开装置A中___________ (填仪器的名称)的活塞,直到______ 再点燃装置F处的酒精灯,目的是_______
③装置D的作用有_______
(3)实验结束后,取少量F中的固体加水溶解,欲对所得产物FeCl3中是否含有FeCl2进行检测,所需试剂是_______
a.KSCN b.H2O2 c.K3[Fe(CN)6] d. .K4[Fe(CN)6]
经检测发现溶液中含有Fe2+,丙同学认为所得产物FeCl3中一定含有FeCl2,丁同学认为不一定,理由是_____
(1)甲组同学拟用下列装置制取纯净干燥的氯气。
①装置B的作用是
②装置A中发生反应时消耗的氧化剂和还原剂的物质的量之比为
(2)乙组同学选用甲组实验中的装置ABC和下列装置制取FeCl3

①乙组同学的实验装置中,依次连接的合理顺序为:a→
②连好装置,检查装置的气密性,先打开装置A中
③装置D的作用有
(3)实验结束后,取少量F中的固体加水溶解,欲对所得产物FeCl3中是否含有FeCl2进行检测,所需试剂是
a.KSCN b.H2O2 c.K3[Fe(CN)6] d. .K4[Fe(CN)6]
经检测发现溶液中含有Fe2+,丙同学认为所得产物FeCl3中一定含有FeCl2,丁同学认为不一定,理由是
您最近半年使用:0次
12-13高一上·陕西·期末
9 . 在 2Na2O2+2CO2=2Na2CO3+O2反应中,
(1)请在此方程上用双线桥法标出电子转移的方向和数目____ 。
(2)________ 是还原剂,________ 是氧化剂。
(3)若转移3mol电子,则所产生的O2在标准状况下的体积为____ 。
(1)请在此方程上用双线桥法标出电子转移的方向和数目
(2)
(3)若转移3mol电子,则所产生的O2在标准状况下的体积为
您最近半年使用:0次



