解题方法
1 . 在催化剂作用下,肼蒸气受热可分解生成N2和一种能使湿润红色石蕊试纸变蓝的气体。写出该反应的化学方程式:_____________ 。
您最近半年使用:0次
解题方法
2 . Fe/Fe3O4复合物是一种高密度磁记录材料,磁记录材料有记录和存储信息的功能。制备该材料的一种流程如下:
Ⅰ、相关反应原理:
①Fe2++2OH-=Fe(OH)2
②3Fe(OH)2=Fe+2Fe(OH)3
③Fe(OH)2+2Fe(OH)3=Fe3O4+4H2O
Ⅱ、25℃时Fe(OH)2的Ksp=8.0×10-16
1.用FeCl2溶液和KOH溶液制备Fe/Fe3O4反应的离子方程式为_____ 。该“反应”中通入氩气的原因_____ 。
2.取少量反应后溶液于试管中,选择试剂_____,可证明FeCl2溶液已反应完全。
3.已知参加反应的FeCl2溶液浓度为lmol·L−1。由题给信息分析,25℃时,当pH<2时,Fe/Fe3O4产率极低的原因_____ 。
下图1为回流时间与Fe/Fe3O4产率的关系图,图2为回流1h所得产品的X射线衍射图。_____ 。
通过Fe3O4和FeO的热化学循环可以利用太阳能,其转化关系如图所示。
6.从绿色化学角度评价该循环过程(说一点)。_____

Ⅰ、相关反应原理:
①Fe2++2OH-=Fe(OH)2
②3Fe(OH)2=Fe+2Fe(OH)3
③Fe(OH)2+2Fe(OH)3=Fe3O4+4H2O
Ⅱ、25℃时Fe(OH)2的Ksp=8.0×10-16
1.用FeCl2溶液和KOH溶液制备Fe/Fe3O4反应的离子方程式为
2.取少量反应后溶液于试管中,选择试剂_____,可证明FeCl2溶液已反应完全。
| A.SO2 | B.铁粉 |
| C.KSCN溶液 | D.KSCN溶液新制氯水 |
下图1为回流时间与Fe/Fe3O4产率的关系图,图2为回流1h所得产品的X射线衍射图。

通过Fe3O4和FeO的热化学循环可以利用太阳能,其转化关系如图所示。
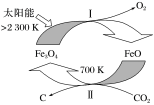
| A.反应物 | B.中间产物 | C.催化剂 | D.产物 |
您最近半年使用:0次
名校
解题方法
3 . 已知离子方程式: (已配平,且系数之比为最简整数比),则系数错误的是
(已配平,且系数之比为最简整数比),则系数错误的是
 (已配平,且系数之比为最简整数比),则系数错误的是
(已配平,且系数之比为最简整数比),则系数错误的是| A.m=2 | B.p=4 | C.x=3 | D.y=3 |
您最近半年使用:0次
2023-01-17更新
|
244次组卷
|
2卷引用:上海市进才中学2022-2023学年高一上学期期末考试化学试题
名校
4 . Ⅰ.某地出现硫酸型酸雨,现采集了一份雨水样品,其pH随时间变化如下:
(1)用化学方程式表示雨水样品pH变化的原因_______ 。
(2)如将刚采集到的雨水样品与自来水混合(自来水含氯气),pH将_______ (选填“变大”、“变小”、“不变”)。发生反应的化学方程式为_______ 。
(3)为了防治酸雨,降低煤燃烧时产生的SO2,工业上将生石灰(CaO)与含硫煤混合使用制取石膏,请写出燃烧时,有关“固硫”的方程式:_______ 。
Ⅱ.如图是土壤中发生的氮循环示意图,回答下列问题:
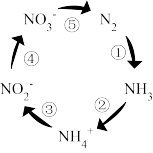
(4)固氮过程的序号是_______ 。人工固氮的反应方程式为_______ 。在细菌微生物的作用下可实现反硝化作用,实现转化的序号为_______ 。为了消除NOx对大气的污染,工业上通常利用NH3还原的方法实现无害化处理,配平NO2与NH3反应的化学方程式:_______ 。
(5)现有NO2和NO的混合气体3L,可用相同状况下3.5L的NH3恰好使其完全转化为N2,则混合气体中NO2和NO体积之比为_______ 。
| 测试时间/h | 0 | 2 | 4 | 6 |
| pH | 4.73 | 4.55 | 4.42 | 4.41 |
(1)用化学方程式表示雨水样品pH变化的原因
(2)如将刚采集到的雨水样品与自来水混合(自来水含氯气),pH将
(3)为了防治酸雨,降低煤燃烧时产生的SO2,工业上将生石灰(CaO)与含硫煤混合使用制取石膏,请写出燃烧时,有关“固硫”的方程式:
Ⅱ.如图是土壤中发生的氮循环示意图,回答下列问题:

(4)固氮过程的序号是
(5)现有NO2和NO的混合气体3L,可用相同状况下3.5L的NH3恰好使其完全转化为N2,则混合气体中NO2和NO体积之比为
您最近半年使用:0次
5 . 目前从海水提溴(Br2)大致有以下步骤。
(1)向浓缩的海水中通入某种气体,将海水中的Br﹣氧化为Br2,该气体是___ 。
(2)用热空气将Br2从上述溶液中吹出,并由浓Na2CO3溶液吸收,转变为NaBr、NaBrO3、1molBr2需消耗Na2CO3___ mol。
(3)再将所得混合溶液用稀硫酸酸化,得到浓度较高的溴水,配平该反应的离子方程式。
__ Br﹣+__ BrO3﹣+__ H+→___ Br2+___ H2O。
(1)向浓缩的海水中通入某种气体,将海水中的Br﹣氧化为Br2,该气体是
(2)用热空气将Br2从上述溶液中吹出,并由浓Na2CO3溶液吸收,转变为NaBr、NaBrO3、1molBr2需消耗Na2CO3
(3)再将所得混合溶液用稀硫酸酸化,得到浓度较高的溴水,配平该反应的离子方程式。
您最近半年使用:0次
名校
6 . (1)铁元素的原子结构示意图为________ ;它在周期表中的位置是_________ 。
(2)某炼铜反应为: 上述反应中,氧化剂是
上述反应中,氧化剂是________ ;若反应中转移15 mol电子,则氧化产物的质量为___________ 。
(3)氧和硫分别形成的氢化物中比较稳定的是________ (写电子式)。
(4)与明矾相似, 也可用作净水剂,其净水的原理是
也可用作净水剂,其净水的原理是_________ 。
(5) 又称摩尔盐,它可作净水剂,还用作化学试剂、医药、冶金、电镀等,请你设计实验检验摩尔盐中的有色阳离子:
又称摩尔盐,它可作净水剂,还用作化学试剂、医药、冶金、电镀等,请你设计实验检验摩尔盐中的有色阳离子:_________________ 。
(2)某炼铜反应为:
 上述反应中,氧化剂是
上述反应中,氧化剂是(3)氧和硫分别形成的氢化物中比较稳定的是
(4)与明矾相似,
 也可用作净水剂,其净水的原理是
也可用作净水剂,其净水的原理是(5)
 又称摩尔盐,它可作净水剂,还用作化学试剂、医药、冶金、电镀等,请你设计实验检验摩尔盐中的有色阳离子:
又称摩尔盐,它可作净水剂,还用作化学试剂、医药、冶金、电镀等,请你设计实验检验摩尔盐中的有色阳离子:
您最近半年使用:0次
名校
7 . 向Na2S和Na2SO3的混合溶液中加入足量的稀硫酸溶液,发生以下反应:
________ Na2S+_________ Na2SO3+________ H2SO4→_______ Na2SO4+_______ S↓+______ H2O
(1)配平上述化学方程式,标出电子转移的方向和数目。________________
(2)反应中被氧化的元素是___________ 。
(3)反应中氧化产物和还原产物物质的量之比为__________ 。
(1)配平上述化学方程式,标出电子转移的方向和数目。
(2)反应中被氧化的元素是
(3)反应中氧化产物和还原产物物质的量之比为
您最近半年使用:0次



