解题方法
1 . 溴元素被称为海洋元素,它主要以溴离子形式存在于海水中。工业上制备粗溴( )的流程如图:
)的流程如图:

已知:①在酸性条件下, 具有强氧化性;②
具有强氧化性;② 。回答下列问题:
。回答下列问题:
(1)“置换”时通入 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(2)单质溴可用热空气吹出,其原因是___________ 。
(3)写出“酸化”时发生反应的化学方程式:___________ 。
(4)用 溶液而不用盐酸“酸化”的原因可能是
溶液而不用盐酸“酸化”的原因可能是___________ 。
(5)为了除去粗溴中微量的氯气,可向粗溴中加入适量___________ (填字母),充分反应后,分液。
a.饱和NaCl溶液 b.NaOH溶液 c. 溶液 d.
溶液 d. 溶液
溶液
 )的流程如图:
)的流程如图:
已知:①在酸性条件下,
 具有强氧化性;②
具有强氧化性;② 。回答下列问题:
。回答下列问题:(1)“置换”时通入
 发生反应的离子方程式为
发生反应的离子方程式为(2)单质溴可用热空气吹出,其原因是
(3)写出“酸化”时发生反应的化学方程式:
(4)用
 溶液而不用盐酸“酸化”的原因可能是
溶液而不用盐酸“酸化”的原因可能是(5)为了除去粗溴中微量的氯气,可向粗溴中加入适量
a.饱和NaCl溶液 b.NaOH溶液 c.
 溶液 d.
溶液 d. 溶液
溶液
您最近一年使用:0次
解题方法
2 . 工业上常采用碱性氯化法来处理高浓度氰化物污水,发生的主要反应为CN-+OH-+Cl2→CO2+N2+Cl-+H2O(未配平)。下列关于该反应的说法错误的是
| A.Cl2是氧化剂,CO2和N2是氧化产物 |
| B.若有1 mol CN-发生反应,则有5 mol电子发生转移 |
| C.若将反应设计成原电池,则CN-在负极上发生反应 |
| D.还原剂和氧化剂的化学计量数之比5:2 |
您最近一年使用:0次
名校
3 . 铜是人类发现最早并广泛使用的一种金属。回答下列问题:
(1)实验室使用稀硫酸和H2O2溶解铜片,该反应的化学方程式为_______________ 。
(2)配制的FeCl3溶液应保持____________ (填“酸性”“碱性”或“中性”),原因是_____________ 。
(1)实验室使用稀硫酸和H2O2溶解铜片,该反应的化学方程式为
(2)配制的FeCl3溶液应保持
您最近一年使用:0次
4 . 请回答下列问题:
(1) 是一种酸根离子,
是一种酸根离子, 中铁元素的化合价为
中铁元素的化合价为___________ 。 属于
属于___________ (填“酸”“碱”、“盐”或“氧化物”)。
(2)新型纳米材料氧缺位铁酸盐(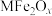 ,
,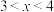 ,
, 、Zn、Ni,且均为
、Zn、Ni,且均为 价,下同)是由铁酸盐
价,下同)是由铁酸盐 经过高温反应得到的。将纳米材料氧缺位铁酸盐分散在蒸馏水中,所形成的分散系属于
经过高温反应得到的。将纳米材料氧缺位铁酸盐分散在蒸馏水中,所形成的分散系属于___________ ;铁酸盐 经过高温反应得到
经过高温反应得到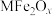 的反应属于
的反应属于___________ (填“氧化还原”或“非氧化还原”)反应。
(3)在酸性条件下, 容易转化为
容易转化为 ,某反应体系中共存在下列6种粒子:
,某反应体系中共存在下列6种粒子: 、
、 、
、 、
、 、
、 、
、 ,则该反应中的氧化剂是
,则该反应中的氧化剂是___________ ,还原剂是___________ 。
(4) 是重要的化工原料,从氧化还原反应的角度分析,下列制备
是重要的化工原料,从氧化还原反应的角度分析,下列制备 的方案理论上可行的是
的方案理论上可行的是___________ (填字母)。
a. b.
b. c.
c. d.
d.
(5)已知 能被
能被 氧化为
氧化为 ,则
,则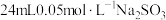 溶液与
溶液与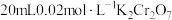 溶液恰好反应时,Cr元素在还原产物中的化合价为
溶液恰好反应时,Cr元素在还原产物中的化合价为___________ 。
(1)
 是一种酸根离子,
是一种酸根离子, 中铁元素的化合价为
中铁元素的化合价为 属于
属于(2)新型纳米材料氧缺位铁酸盐(
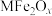 ,
,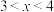 ,
, 、Zn、Ni,且均为
、Zn、Ni,且均为 价,下同)是由铁酸盐
价,下同)是由铁酸盐 经过高温反应得到的。将纳米材料氧缺位铁酸盐分散在蒸馏水中,所形成的分散系属于
经过高温反应得到的。将纳米材料氧缺位铁酸盐分散在蒸馏水中,所形成的分散系属于 经过高温反应得到
经过高温反应得到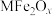 的反应属于
的反应属于(3)在酸性条件下,
 容易转化为
容易转化为 ,某反应体系中共存在下列6种粒子:
,某反应体系中共存在下列6种粒子: 、
、 、
、 、
、 、
、 、
、 ,则该反应中的氧化剂是
,则该反应中的氧化剂是(4)
 是重要的化工原料,从氧化还原反应的角度分析,下列制备
是重要的化工原料,从氧化还原反应的角度分析,下列制备 的方案理论上可行的是
的方案理论上可行的是a.
 b.
b. c.
c. d.
d.
(5)已知
 能被
能被 氧化为
氧化为 ,则
,则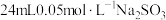 溶液与
溶液与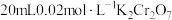 溶液恰好反应时,Cr元素在还原产物中的化合价为
溶液恰好反应时,Cr元素在还原产物中的化合价为
您最近一年使用:0次
2021-12-08更新
|
365次组卷
|
3卷引用:青海省西宁市2021-2022学年高三上学期期末统考化学试题
5 . 亚硝酸钠有咸味,有毒,暴露于空气中会与氧气反应生成硝酸钠。
已知: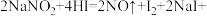 _____。
_____。
(1)上述方程式中横线处应填的是___________ 。
(2)上述反应的还原剂为___________ (填化学式);若反应中有 (标准状况下)气体生成则反应中转移电子的物质的量为
(标准状况下)气体生成则反应中转移电子的物质的量为___________  。
。
(3)在酸性条件下,高锰酸钾可将 氧化为
氧化为 ,所得溶液中锰元素仅以
,所得溶液中锰元素仅以 形式存在,写出此反应的离子方程式:
形式存在,写出此反应的离子方程式:___________ 。
(4) 加热到320℃以上会分解生成二氧化氮、一氧化氮和氧化钠,写出此反应的化学方程式并用双线桥法标明电子的转移方向和数目:
加热到320℃以上会分解生成二氧化氮、一氧化氮和氧化钠,写出此反应的化学方程式并用双线桥法标明电子的转移方向和数目:___________ 。反应中被氧化的元素和被还原的元素的物质的量之比为___________ 。
(5)某厂废液中,含有2%~5%的 ,直接排放会造成污染,
,直接排放会造成污染, 能使
能使 转化为
转化为 ,则反应中氧化剂和还原剂的质量之比为
,则反应中氧化剂和还原剂的质量之比为___________ 。
已知:
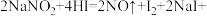 _____。
_____。(1)上述方程式中横线处应填的是
(2)上述反应的还原剂为
 (标准状况下)气体生成则反应中转移电子的物质的量为
(标准状况下)气体生成则反应中转移电子的物质的量为 。
。(3)在酸性条件下,高锰酸钾可将
 氧化为
氧化为 ,所得溶液中锰元素仅以
,所得溶液中锰元素仅以 形式存在,写出此反应的离子方程式:
形式存在,写出此反应的离子方程式:(4)
 加热到320℃以上会分解生成二氧化氮、一氧化氮和氧化钠,写出此反应的化学方程式并用双线桥法标明电子的转移方向和数目:
加热到320℃以上会分解生成二氧化氮、一氧化氮和氧化钠,写出此反应的化学方程式并用双线桥法标明电子的转移方向和数目:(5)某厂废液中,含有2%~5%的
 ,直接排放会造成污染,
,直接排放会造成污染, 能使
能使 转化为
转化为 ,则反应中氧化剂和还原剂的质量之比为
,则反应中氧化剂和还原剂的质量之比为
您最近一年使用:0次
解题方法
6 . 氧化还原反应在生产、生活中应用广泛,酸性KMnO4、H2O2、Fe(NO3)3是重要的氧化剂.已知在酸性条件下,KMnO4被还原为Mn2+。用所学知识回答问题:
(1)3H2SO4+2KMnO4+5H2O2=K2SO4+2MnSO4+5O2↑+8H2O,当有6mol H2SO4参加反应的过程中,有___ mol还原剂被氧化。
(2)在稀硫酸中,KMnO4能将H2C2O4氧化为CO2。该反应的离子方程式为___ 。
(3)取300mL2mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成KIO3,则消耗KMnO4的物质的量的是___ mol。
(4)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是___ ,又变为棕黄色的原因是___ 。
(1)3H2SO4+2KMnO4+5H2O2=K2SO4+2MnSO4+5O2↑+8H2O,当有6mol H2SO4参加反应的过程中,有
(2)在稀硫酸中,KMnO4能将H2C2O4氧化为CO2。该反应的离子方程式为
(3)取300mL2mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成KIO3,则消耗KMnO4的物质的量的是
(4)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是
您最近一年使用:0次



