名校
1 . 利用如图可以从不同角度研究含硫物质的性质及其转化关系。
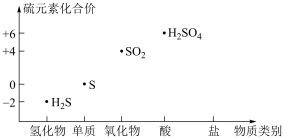
回答下列问题:
(1)H2S与SO2反应的化学方程式为____ ,反应中H2S体现____ (填“氧化性”或“还原性”)。
(2)加热时,浓硫酸与木炭反应的化学方程式为____ ,下列试剂不能用于验证生成物中含有SO2的是____ (填标号)。
a.品红溶液b.酸性KMnO4溶液c.澄清石灰水
(3)SO2的过度排放会引起酸雨,酸雨是指pH<____ 的雨水,其中NOx的排放也会导致酸雨的形成,写出NO2与水反应的化学方程式____ 。
(4)实验室可用碱液吸收法对NOx进行尾气处理,写出NO2与氢氧化钠溶液反应的离子方程式____ 。

回答下列问题:
(1)H2S与SO2反应的化学方程式为
(2)加热时,浓硫酸与木炭反应的化学方程式为
a.品红溶液b.酸性KMnO4溶液c.澄清石灰水
(3)SO2的过度排放会引起酸雨,酸雨是指pH<
(4)实验室可用碱液吸收法对NOx进行尾气处理,写出NO2与氢氧化钠溶液反应的离子方程式
您最近一年使用:0次
2 . 运用化学反应原理研究硫单质及其化合物的反应,对生产、生活、环境保护等领域有着重要的意义。
(1)工业上采用 催化还原
催化还原 ,不仅可以消除
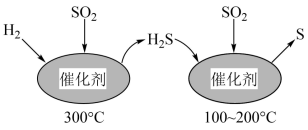
,不仅可以消除 污染,还可得到单质S。反应分两步完成,如图所示,
污染,还可得到单质S。反应分两步完成,如图所示, 催化还原
催化还原 第一步反应的化学方程式为
第一步反应的化学方程式为___________ 。
(2)工业上常用 溶液对燃煤烟气进行脱硫、脱硝。
溶液对燃煤烟气进行脱硫、脱硝。
已知 溶液具有强氧化性,酸性条件下
溶液具有强氧化性,酸性条件下 发生歧化反应生成
发生歧化反应生成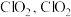 易溶于水,具有强氧化性,可氧化
易溶于水,具有强氧化性,可氧化 。
。
①实验室模拟脱硫过程:先加稀硫酸调节 吸收液的
吸收液的 为5,再向其中通入含
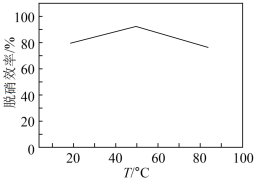
为5,再向其中通入含 的模拟烟气,测得脱硫效率(即
的模拟烟气,测得脱硫效率(即 的吸收率)随温度变化的曲线如图所示。结合已知信息分析,温度大于
的吸收率)随温度变化的曲线如图所示。结合已知信息分析,温度大于 时,随温度升高脱硫效率下降的原因是
时,随温度升高脱硫效率下降的原因是___________ 。
②煤燃烧排放的烟气含有 和
和 ,采用
,采用 溶液作为吸收剂可同时对烟气进行脱硫、脱硝。将含有
溶液作为吸收剂可同时对烟气进行脱硫、脱硝。将含有 和
和 的烟气通入盛有
的烟气通入盛有 溶液的反应器中,反应一段时间后,测得溶液中离子浓度的有关数据如表(其他离子忽略不计):
溶液的反应器中,反应一段时间后,测得溶液中离子浓度的有关数据如表(其他离子忽略不计):
表中y=_______ 。若该溶液为 (吸收前后溶液体积不变),该过程转移的电子数为
(吸收前后溶液体积不变),该过程转移的电子数为______ mol。(写出计算过程)。
(1)工业上采用
 催化还原
催化还原 ,不仅可以消除
,不仅可以消除 污染,还可得到单质S。反应分两步完成,如图所示,
污染,还可得到单质S。反应分两步完成,如图所示, 催化还原
催化还原 第一步反应的化学方程式为
第一步反应的化学方程式为
(2)工业上常用
 溶液对燃煤烟气进行脱硫、脱硝。
溶液对燃煤烟气进行脱硫、脱硝。已知
 溶液具有强氧化性,酸性条件下
溶液具有强氧化性,酸性条件下 发生歧化反应生成
发生歧化反应生成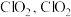 易溶于水,具有强氧化性,可氧化
易溶于水,具有强氧化性,可氧化 。
。①实验室模拟脱硫过程:先加稀硫酸调节
 吸收液的
吸收液的 为5,再向其中通入含
为5,再向其中通入含 的模拟烟气,测得脱硫效率(即
的模拟烟气,测得脱硫效率(即 的吸收率)随温度变化的曲线如图所示。结合已知信息分析,温度大于
的吸收率)随温度变化的曲线如图所示。结合已知信息分析,温度大于 时,随温度升高脱硫效率下降的原因是
时,随温度升高脱硫效率下降的原因是
②煤燃烧排放的烟气含有
 和
和 ,采用
,采用 溶液作为吸收剂可同时对烟气进行脱硫、脱硝。将含有
溶液作为吸收剂可同时对烟气进行脱硫、脱硝。将含有 和
和 的烟气通入盛有
的烟气通入盛有 溶液的反应器中,反应一段时间后,测得溶液中离子浓度的有关数据如表(其他离子忽略不计):
溶液的反应器中,反应一段时间后,测得溶液中离子浓度的有关数据如表(其他离子忽略不计):| 离子 |  |  |  |  |  |
浓度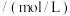 | 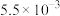 |  |  |  |  |
 (吸收前后溶液体积不变),该过程转移的电子数为
(吸收前后溶液体积不变),该过程转移的电子数为
您最近一年使用:0次
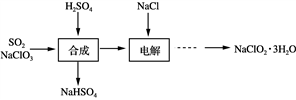
3 . NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其生产工艺如下:
(1) “合成”步骤可以得到ClO2,其反应的化学方程式为_____________________________ 。
(2) “电解”步骤阳极会生成一种气体,其化学式为____________ 。
(3) 反应生成的ClO2可用于高效脱除烟气中的SO2。以ClO2脱除SO2实验时SO2脱除率与溶液pH关系如右图所示。pH在3~7.6之间时,随pH增大,ClO2氧化性减弱,脱硫率降低。而当pH>7.6时,随pH增大,SO2脱除率又升高,其原因可能为_____________________________________ 。
(4) 国家标准规定产品中优级纯试剂纯度≥99.8%,分析纯试剂纯度≥99.7%,化学纯试剂纯度≥99.5%。为了确定某批次NaClO2产品的等级,研究小组设计测定方案如下:取10.00 g样品,用适量蒸馏水溶解后,加入略过量的KI溶液;充分反应后,将反应液定容至200 mL,取出20.00 mL于锥形瓶;向锥形瓶中滴加两滴淀粉溶液,用2.00 mol·L-1的Na2S2O3溶液与之反应,消耗Na2S2O3溶液22.00 ml。该样品可达________ 试剂纯度。(写出计算过程)
已知:ClO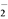 +4I-+4H+===2H2O+2I2+Cl-,I2+2S2O
+4I-+4H+===2H2O+2I2+Cl-,I2+2S2O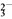 ===2I-+S4O
===2I-+S4O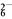
(1) “合成”步骤可以得到ClO2,其反应的化学方程式为
(2) “电解”步骤阳极会生成一种气体,其化学式为
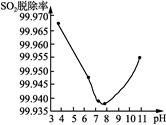
(3) 反应生成的ClO2可用于高效脱除烟气中的SO2。以ClO2脱除SO2实验时SO2脱除率与溶液pH关系如右图所示。pH在3~7.6之间时,随pH增大,ClO2氧化性减弱,脱硫率降低。而当pH>7.6时,随pH增大,SO2脱除率又升高,其原因可能为
(4) 国家标准规定产品中优级纯试剂纯度≥99.8%,分析纯试剂纯度≥99.7%,化学纯试剂纯度≥99.5%。为了确定某批次NaClO2产品的等级,研究小组设计测定方案如下:取10.00 g样品,用适量蒸馏水溶解后,加入略过量的KI溶液;充分反应后,将反应液定容至200 mL,取出20.00 mL于锥形瓶;向锥形瓶中滴加两滴淀粉溶液,用2.00 mol·L-1的Na2S2O3溶液与之反应,消耗Na2S2O3溶液22.00 ml。该样品可达
已知:ClO
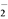 +4I-+4H+===2H2O+2I2+Cl-,I2+2S2O
+4I-+4H+===2H2O+2I2+Cl-,I2+2S2O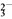 ===2I-+S4O
===2I-+S4O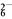
您最近一年使用:0次
4 . 某化学兴趣小组欲利用下列试剂:铁粉、锌粉、 溶液、KSCN溶液、新制氯水,探究
溶液、KSCN溶液、新制氯水,探究 的还原性,请回答下列问题:
的还原性,请回答下列问题:
(1)用所给试剂写出体现 具有还原性的离子反应方程式:
具有还原性的离子反应方程式:_______ ,由此得出,在配制 溶液时,
溶液时, 容易被氧化,欲检验
容易被氧化,欲检验 溶液是否变质,应加入的试剂是
溶液是否变质,应加入的试剂是_______ ;
(2)该小组同学用 溶液和NaOH溶液混合制备
溶液和NaOH溶液混合制备 ,观察到沉淀最终变成红褐色,原因是
,观察到沉淀最终变成红褐色,原因是_______ (用化学方程式解释);
(3)酸性条件下,某反应中反应物与生成物有 、
、 、
、 、
、 、
、 和一种未知离子X。
和一种未知离子X。
已知:反应中1mol 得5mol电子。
得5mol电子。
① 中Mn元素的化合价为
中Mn元素的化合价为_______ ,X离子是_______ 。
②该反应的离子方程式是_______ 。
 溶液、KSCN溶液、新制氯水,探究
溶液、KSCN溶液、新制氯水,探究 的还原性,请回答下列问题:
的还原性,请回答下列问题:(1)用所给试剂写出体现
 具有还原性的离子反应方程式:
具有还原性的离子反应方程式: 溶液时,
溶液时, 容易被氧化,欲检验
容易被氧化,欲检验 溶液是否变质,应加入的试剂是
溶液是否变质,应加入的试剂是(2)该小组同学用
 溶液和NaOH溶液混合制备
溶液和NaOH溶液混合制备 ,观察到沉淀最终变成红褐色,原因是
,观察到沉淀最终变成红褐色,原因是(3)酸性条件下,某反应中反应物与生成物有
 、
、 、
、 、
、 、
、 和一种未知离子X。
和一种未知离子X。已知:反应中1mol
 得5mol电子。
得5mol电子。①
 中Mn元素的化合价为
中Mn元素的化合价为②该反应的离子方程式是
您最近一年使用:0次
5 . 已知氧化性:BrO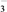 >ClO
>ClO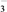 >Cl2>IO
>Cl2>IO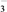 >I2。现将饱和氯水逐滴滴入KI淀粉溶液中至过量。
>I2。现将饱和氯水逐滴滴入KI淀粉溶液中至过量。
(1)可观察到的现象是
①_________________________________________________ ;
②_________________________________________________ 。
(2)写出有关反应的离子方程式:
①___________________________________________ ;
②___________________________________________ 。
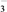 >ClO
>ClO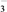 >Cl2>IO
>Cl2>IO >I2。现将饱和氯水逐滴滴入KI淀粉溶液中至过量。
>I2。现将饱和氯水逐滴滴入KI淀粉溶液中至过量。(1)可观察到的现象是
①
②
(2)写出有关反应的离子方程式:
①
②
您最近一年使用:0次
2017-09-23更新
|
176次组卷
|
2卷引用:2018届高三一轮复习化学:考点12-氧化性、还原性强弱的比较



