名校
1 . 硫有多种化合物,如 、
、 等,它们对环境均有一定的影响,含硫化合物的综合利用既可以消除污染,又可以带来一定的经济效益。
等,它们对环境均有一定的影响,含硫化合物的综合利用既可以消除污染,又可以带来一定的经济效益。
(1)有学者提出利用 、
、 等离子的作用。在常温下将
等离子的作用。在常温下将 氧化成
氧化成 而实现
而实现 的回收利用,写出
的回收利用,写出 将
将 氧化成
氧化成 反应的离子方程式
反应的离子方程式___________ 。
(2)含有 、
、 的硫酸盐混合溶液可用于吸收
的硫酸盐混合溶液可用于吸收 回收硫单质,其转化关系如图所示。该图示中总反应的化学方程式为
回收硫单质,其转化关系如图所示。该图示中总反应的化学方程式为___________ ,其中催化剂是___________ 。 的烟气,以减少其对环境造成的污染。“
的烟气,以减少其对环境造成的污染。“ 吸收塔”中发生反应的化学方程式为
吸收塔”中发生反应的化学方程式为___________ ,该流程中可循环利用的物质为___________ (填化学式)。 的含量符合标准才能排放。已知有V L(已换算成标准状况)尾气,通入足量
的含量符合标准才能排放。已知有V L(已换算成标准状况)尾气,通入足量 溶液吸收再加入足量
溶液吸收再加入足量 溶液充分反应后(不考虑尾气中其它成分的反应),过滤,洗涤、干燥、称量得到b g沉淀。
溶液充分反应后(不考虑尾气中其它成分的反应),过滤,洗涤、干燥、称量得到b g沉淀。 溶液的作用是
溶液的作用是___________ ;尾气中 含量(体积分数)的计算式是
含量(体积分数)的计算式是___________ (用含V、b的代数式表示)。
 、
、 等,它们对环境均有一定的影响,含硫化合物的综合利用既可以消除污染,又可以带来一定的经济效益。
等,它们对环境均有一定的影响,含硫化合物的综合利用既可以消除污染,又可以带来一定的经济效益。(1)有学者提出利用
 、
、 等离子的作用。在常温下将
等离子的作用。在常温下将 氧化成
氧化成 而实现
而实现 的回收利用,写出
的回收利用,写出 将
将 氧化成
氧化成 反应的离子方程式
反应的离子方程式(2)含有
 、
、 的硫酸盐混合溶液可用于吸收
的硫酸盐混合溶液可用于吸收 回收硫单质,其转化关系如图所示。该图示中总反应的化学方程式为
回收硫单质,其转化关系如图所示。该图示中总反应的化学方程式为
 的烟气,以减少其对环境造成的污染。“
的烟气,以减少其对环境造成的污染。“ 吸收塔”中发生反应的化学方程式为
吸收塔”中发生反应的化学方程式为
 的含量符合标准才能排放。已知有V L(已换算成标准状况)尾气,通入足量
的含量符合标准才能排放。已知有V L(已换算成标准状况)尾气,通入足量 溶液吸收再加入足量
溶液吸收再加入足量 溶液充分反应后(不考虑尾气中其它成分的反应),过滤,洗涤、干燥、称量得到b g沉淀。
溶液充分反应后(不考虑尾气中其它成分的反应),过滤,洗涤、干燥、称量得到b g沉淀。 溶液的作用是
溶液的作用是 含量(体积分数)的计算式是
含量(体积分数)的计算式是
您最近一年使用:0次
2 . 按要求完成以下填空:
(1)现有下列10种物质:①稀盐酸,②纯醋酸,③干冰,④H2SO4,⑤AgCl,⑥熔融硝酸钠,⑦液态氯化氢,⑧Ba(OH)2,⑨Al2O3,⑩C2H5OH
上述物质中能导电的是___________ (填序号),属于非电解质的有 ___________ (填序号),利用以上物质写出与离子方程式“H++OH- =H2O”相对应的一个化学方程式:___________ 。
(2)为治理汽车尾气中的NO和CO对环境的污染,可在汽车排气管上安装催化转化器,发生如下反应2NO+2CO N2+2CO2。
N2+2CO2。
①用双线桥标出电子转移的方向和数目___________ (注明得失)。
②当消耗3g的NO时得到氧化产物的质量为___________ ,转移的电子的物质的量是 ___________ 。
(3)下列所列举的是3张在一定温度下物质的导电能力(σ)随新物质加入量(V)的变化曲线图,向饱和食盐水中不断通入二氧化碳相符的变化曲线图是___________ (填字母)。
A.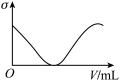 B.
B.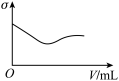 C.
C.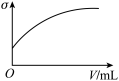
(1)现有下列10种物质:①稀盐酸,②纯醋酸,③干冰,④H2SO4,⑤AgCl,⑥熔融硝酸钠,⑦液态氯化氢,⑧Ba(OH)2,⑨Al2O3,⑩C2H5OH
上述物质中能导电的是
(2)为治理汽车尾气中的NO和CO对环境的污染,可在汽车排气管上安装催化转化器,发生如下反应2NO+2CO
 N2+2CO2。
N2+2CO2。①用双线桥标出电子转移的方向和数目
②当消耗3g的NO时得到氧化产物的质量为
(3)下列所列举的是3张在一定温度下物质的导电能力(σ)随新物质加入量(V)的变化曲线图,向饱和食盐水中不断通入二氧化碳相符的变化曲线图是
A.
 B.
B. C.
C.
您最近一年使用:0次
3 . 生活中离不开化学,家庭厨卫中有许多中学化学常见的物质,括号内为厨卫商品的主要成分:
①食盐(NaCl);②料酒(乙醇);③食醋(乙酸);④碱面( );⑤小苏打(
);⑤小苏打( );⑥84消毒液(NaClO);⑦洁厕灵(HCl);⑧净水剂(明矾);⑨铁锅(Fe)
);⑥84消毒液(NaClO);⑦洁厕灵(HCl);⑧净水剂(明矾);⑨铁锅(Fe)
回答下列问题:
(1)明矾的化学式为 ,属于
,属于______ (填“纯净物”或“混合物”)。
(2)小苏打的主要成分 ,在水溶液的电离方程式:
,在水溶液的电离方程式:______ 。
(3)厨卫用品的主要成分(括号内的物质)是电解质的有______ (填序号,下同),是非电解质的有______ ,能够导电的有______ 。
(4)⑥和⑦不能混用,原理为______ (用化学反应方程式表示)。
(5)已知 和碱反应生成
和碱反应生成 ,故
,故 为酸性氧化物,
为酸性氧化物, 与酸反应生成
与酸反应生成 ,故
,故 为碱性氧化物.
为碱性氧化物. 可以形成两种盐:
可以形成两种盐: 、
、 (微溶物),则
(微溶物),则 属于
属于______ 氧化物(填“酸性”或“碱性”、“两性”、“不成盐”).写出 与浓NaOH溶液反应的化学反应方程式:
与浓NaOH溶液反应的化学反应方程式:______ 。
①食盐(NaCl);②料酒(乙醇);③食醋(乙酸);④碱面(
 );⑤小苏打(
);⑤小苏打( );⑥84消毒液(NaClO);⑦洁厕灵(HCl);⑧净水剂(明矾);⑨铁锅(Fe)
);⑥84消毒液(NaClO);⑦洁厕灵(HCl);⑧净水剂(明矾);⑨铁锅(Fe)回答下列问题:
(1)明矾的化学式为
 ,属于
,属于(2)小苏打的主要成分
 ,在水溶液的电离方程式:
,在水溶液的电离方程式:(3)厨卫用品的主要成分(括号内的物质)是电解质的有
(4)⑥和⑦不能混用,原理为
(5)已知
 和碱反应生成
和碱反应生成 ,故
,故 为酸性氧化物,
为酸性氧化物, 与酸反应生成
与酸反应生成 ,故
,故 为碱性氧化物.
为碱性氧化物. 可以形成两种盐:
可以形成两种盐: 、
、 (微溶物),则
(微溶物),则 属于
属于 与浓NaOH溶液反应的化学反应方程式:
与浓NaOH溶液反应的化学反应方程式:
您最近一年使用:0次
4 . 回答下列问题:
(1)下列三组物质中,均有一种物质的类别与其他三种不同。
①MgO、Na2O、CO2、CuO ②HCl、H2O、H2SO4、HNO3 ③NaOH、Na2CO3、KOH、Cu(OH)2
三种物质依次是(填化学式):①_______ ;②_______ ;③_______ 。
(2)HCO 与H+、OH-在溶液都不能大量共存,试用离子方程式说明HCO
与H+、OH-在溶液都不能大量共存,试用离子方程式说明HCO 与OH-在溶液不能大量共存的原因:
与OH-在溶液不能大量共存的原因:_______ 。
(3)离子的摩尔电导率可用来衡量电解质溶液中离子导电能力的强弱,摩尔电导率越大,离子在溶液中的导电能力越强。已知Ca2+、OH-、HCO 的摩尔电导率分别为0.60、1.98、0.45。据此可判断,向饱和的澄清石灰水中通入过量的CO2,溶液导电能力随CO2通入量的变化趋势正确的是_______。
的摩尔电导率分别为0.60、1.98、0.45。据此可判断,向饱和的澄清石灰水中通入过量的CO2,溶液导电能力随CO2通入量的变化趋势正确的是_______。
(4)等质量的O2和O3所含氧原子个数之比_______ 。
(5)12.4g Na2R含Na+ 0.4mol,则Na2R的摩尔质量为_______ 。
(6)标况下, 16g二氧化碳和一氧化碳组成的混合气体,其体积为8.96L,则该混合气体含有_______ 个C原子。
(7)请配平下面方程式:_______ 。
_______KMnO4 +_______HCl —_______KCl +_______MnCl2 +_______Cl2↑ + _______H2O
(8)用双线桥法表示反应8NH3+3Cl2=6NH4Cl+N2的电子转:_______ 。
(1)下列三组物质中,均有一种物质的类别与其他三种不同。
①MgO、Na2O、CO2、CuO ②HCl、H2O、H2SO4、HNO3 ③NaOH、Na2CO3、KOH、Cu(OH)2
三种物质依次是(填化学式):①
(2)HCO
 与H+、OH-在溶液都不能大量共存,试用离子方程式说明HCO
与H+、OH-在溶液都不能大量共存,试用离子方程式说明HCO 与OH-在溶液不能大量共存的原因:
与OH-在溶液不能大量共存的原因:(3)离子的摩尔电导率可用来衡量电解质溶液中离子导电能力的强弱,摩尔电导率越大,离子在溶液中的导电能力越强。已知Ca2+、OH-、HCO
 的摩尔电导率分别为0.60、1.98、0.45。据此可判断,向饱和的澄清石灰水中通入过量的CO2,溶液导电能力随CO2通入量的变化趋势正确的是_______。
的摩尔电导率分别为0.60、1.98、0.45。据此可判断,向饱和的澄清石灰水中通入过量的CO2,溶液导电能力随CO2通入量的变化趋势正确的是_______。A.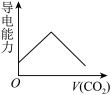 | B.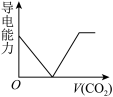 | C. | D.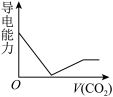 |
(4)等质量的O2和O3所含氧原子个数之比
(5)12.4g Na2R含Na+ 0.4mol,则Na2R的摩尔质量为
(6)标况下, 16g二氧化碳和一氧化碳组成的混合气体,其体积为8.96L,则该混合气体含有
(7)请配平下面方程式:
_______KMnO4 +_______HCl —_______KCl +_______MnCl2 +_______Cl2↑ + _______H2O
(8)用双线桥法表示反应8NH3+3Cl2=6NH4Cl+N2的电子转:
您最近一年使用:0次
名校
解题方法
5 . (一)工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:
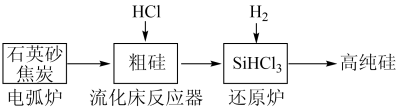
(1)工业上用石英砂和焦炭在电弧炉中高温加热到1600℃-1800℃生成粗硅的化学方程式为:___________ 。
(2)在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,粗硅生成SiHCl3的化学反应为:Si+3HCl SiHCl3+H2,生成物SiHCl3的结构式为:
SiHCl3+H2,生成物SiHCl3的结构式为:___________ 。
(二)某化学兴趣小组利用下列图示装置探究氨气的性质。
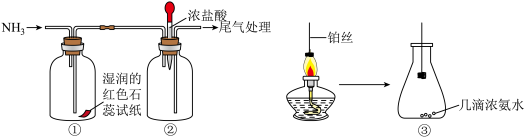
(3)①中湿润的红色石蕊试纸变蓝的原因:___________ (用化学方程式表示)。
(4)向②中滴入浓盐酸,现象为:___________ 。
(5)将灼热的铂丝伸入③中锥形瓶,可观察到铂丝保持红热,有红棕色气体及少量白烟生成。该过程会同时发生多个反应,写出NH3和O2催化氧化的化学方程式:___________ ,瓶中红棕色气体为___________ (填化学式)。
(三)某氨氮废水( 、
、 )的生物法处理流程如图所示:
)的生物法处理流程如图所示:

(6)检验氨氮废水中含有 的方法是:
的方法是:___________ 。
(7)过程Ⅱ在硝化细菌作用下实现 的转化,称为硝化过程。在碱性条件下实现上述硝化过程的总反应的离子方程式为:
的转化,称为硝化过程。在碱性条件下实现上述硝化过程的总反应的离子方程式为:___________ 。

(1)工业上用石英砂和焦炭在电弧炉中高温加热到1600℃-1800℃生成粗硅的化学方程式为:
(2)在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,粗硅生成SiHCl3的化学反应为:Si+3HCl
 SiHCl3+H2,生成物SiHCl3的结构式为:
SiHCl3+H2,生成物SiHCl3的结构式为:(二)某化学兴趣小组利用下列图示装置探究氨气的性质。

(3)①中湿润的红色石蕊试纸变蓝的原因:
(4)向②中滴入浓盐酸,现象为:
(5)将灼热的铂丝伸入③中锥形瓶,可观察到铂丝保持红热,有红棕色气体及少量白烟生成。该过程会同时发生多个反应,写出NH3和O2催化氧化的化学方程式:
(三)某氨氮废水(
 、
、 )的生物法处理流程如图所示:
)的生物法处理流程如图所示:
(6)检验氨氮废水中含有
 的方法是:
的方法是:(7)过程Ⅱ在硝化细菌作用下实现
 的转化,称为硝化过程。在碱性条件下实现上述硝化过程的总反应的离子方程式为:
的转化,称为硝化过程。在碱性条件下实现上述硝化过程的总反应的离子方程式为:
您最近一年使用:0次
名校
6 . 钠和铁都是重要的金属元素,被广泛应用于冶金、建筑等领域,有着重要的工业利用价值。
I.物质类别和核心元素的价态是学习元素及其化合物性质的两个重要视角。下图是钠及其化合物 的“价−类”二维图。
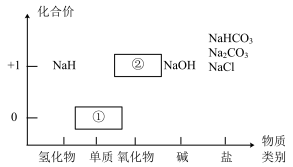
请回答下列问题:
(1)写出NaHCO3在水中电离的离子方程式________ 。
(2)银白色固体①应保存在______ 中;①可直接转化为淡黄色固体②,写出该反应的化学方程式_______ 。
(3)氢化钠(NaH)是一种储氢材料,室温下能结合CO2制氢:4NaH+3CO2=2Na2CO3+C+2H2。
①该反应中氧化产物和还原产物的物质的量之比为__________ 。
②由氢元素价态可知,NaH常用作_______ (填“氧化剂”或“还原剂”)。
II.绿矾(七水合硫酸亚铁,FeSO4·7H2O)能够用于处理工业废水中具有强氧化性的离子重铬酸根(Cr2O72−),反应原理为: Fe2++ Cr2O72−+ H+ = Fe3++ Cr3++ H2O
(4)填写空格,完成该反应方程式的配平________ 。
(5)该反应中______ 元素被氧化,还原产物是________ 。
I.物质类别和核心元素的价态是学习元素及其化合物性质的两个重要视角。下图是

请回答下列问题:
(1)写出NaHCO3在水中电离的离子方程式
(2)银白色固体①应保存在
(3)氢化钠(NaH)是一种储氢材料,室温下能结合CO2制氢:4NaH+3CO2=2Na2CO3+C+2H2。
①该反应中氧化产物和还原产物的物质的量之比为
②由氢元素价态可知,NaH常用作
II.绿矾(七水合硫酸亚铁,FeSO4·7H2O)能够用于处理工业废水中具有强氧化性的离子重铬酸根(Cr2O72−),反应原理为: Fe2++ Cr2O72−+ H+ = Fe3++ Cr3++ H2O
(4)填写空格,完成该反应方程式的配平
(5)该反应中
您最近一年使用:0次
7 . Ⅰ.某化学兴趣小组的同学学了金属的电化学腐蚀,对教材叙述[钢铁在酸性环境中发生析氢腐蚀;在酸性很弱或呈中性,溶有 的环境中发生吸氧腐蚀;钢铁等金属的腐蚀主要为吸氧腐蚀]产生疑问,决定用数字化实验模拟探究钢铁在酸性环境下的腐蚀情况。
的环境中发生吸氧腐蚀;钢铁等金属的腐蚀主要为吸氧腐蚀]产生疑问,决定用数字化实验模拟探究钢铁在酸性环境下的腐蚀情况。
(1)用图1所示装置进行实验:打开a________ (填仪器名称)的活塞,加入1mL溶液,测得压强随时间变化曲线如图2。
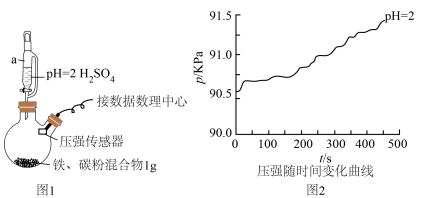
同学甲得出结论:酸性条件下,铁粉发生析氢腐蚀。
(2)同学乙认为甲的结论不科学,锥形瓶内压强变大还可能是___________ ,提出改进措施___________ 。改进后,再次实验,证明甲、乙的猜想均正确,请在图2绘制出改进后的曲线___________ 。
(3)同学丙认为甲、乙的实验不具代表性,建议用不同浓度的酸进行实验。在改进后的装置中分别用 、
、 的硫酸实验,测定压强随时间变化情况,结果如图3.同学丙得出:酸性较弱时,铁会发生吸氧腐蚀,其依据是
的硫酸实验,测定压强随时间变化情况,结果如图3.同学丙得出:酸性较弱时,铁会发生吸氧腐蚀,其依据是___________ 。
(4)对于图3中 时,铁是否发生了腐蚀?同学们意见不统一,经讨论,他们把压强传感器换成氧气传感器,得出不同pH时装置中
时,铁是否发生了腐蚀?同学们意见不统一,经讨论,他们把压强传感器换成氧气传感器,得出不同pH时装置中 浓度随时间的变化曲线如图4。
浓度随时间的变化曲线如图4。
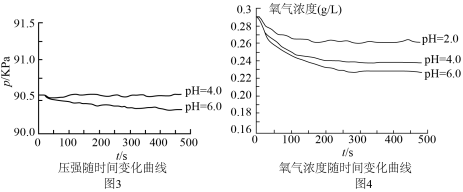
结合实验分析: 时,压强几乎不随时间改变是因为
时,压强几乎不随时间改变是因为___________ 。
综上,小组同学得出结论:教材表述科学严谨。
Ⅱ.拓展研究:
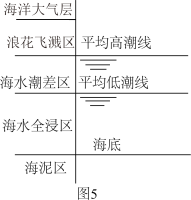
(5)侯保荣院士专门研究海洋钢架结构桥海洋大气层梁腐蚀,他发现腐蚀最严重的是浪花飞溅区浪花飞溅区(海洋环境分区如图5),请你解释原因___________ 。
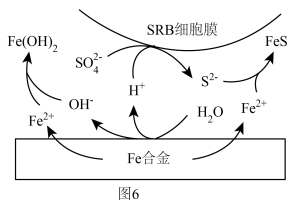
(6)科学家还发现在 浓度很小的海底也有厌氧微生物(如硫酸盐还原菌SRB)对海洋钢制部件的腐蚀,其原理如图6,已知溶液中的
浓度很小的海底也有厌氧微生物(如硫酸盐还原菌SRB)对海洋钢制部件的腐蚀,其原理如图6,已知溶液中的 完全转化为FeS,请写出该铁合金腐蚀的总反应
完全转化为FeS,请写出该铁合金腐蚀的总反应___________ (离子方程式)。
(7)请列举出生产生活中金属制品的防腐措施___________ (任写一点即可)。
 的环境中发生吸氧腐蚀;钢铁等金属的腐蚀主要为吸氧腐蚀]产生疑问,决定用数字化实验模拟探究钢铁在酸性环境下的腐蚀情况。
的环境中发生吸氧腐蚀;钢铁等金属的腐蚀主要为吸氧腐蚀]产生疑问,决定用数字化实验模拟探究钢铁在酸性环境下的腐蚀情况。(1)用图1所示装置进行实验:打开a

同学甲得出结论:酸性条件下,铁粉发生析氢腐蚀。
(2)同学乙认为甲的结论不科学,锥形瓶内压强变大还可能是
(3)同学丙认为甲、乙的实验不具代表性,建议用不同浓度的酸进行实验。在改进后的装置中分别用
 、
、 的硫酸实验,测定压强随时间变化情况,结果如图3.同学丙得出:酸性较弱时,铁会发生吸氧腐蚀,其依据是
的硫酸实验,测定压强随时间变化情况,结果如图3.同学丙得出:酸性较弱时,铁会发生吸氧腐蚀,其依据是(4)对于图3中
 时,铁是否发生了腐蚀?同学们意见不统一,经讨论,他们把压强传感器换成氧气传感器,得出不同pH时装置中
时,铁是否发生了腐蚀?同学们意见不统一,经讨论,他们把压强传感器换成氧气传感器,得出不同pH时装置中 浓度随时间的变化曲线如图4。
浓度随时间的变化曲线如图4。
结合实验分析:
 时,压强几乎不随时间改变是因为
时,压强几乎不随时间改变是因为综上,小组同学得出结论:教材表述科学严谨。
Ⅱ.拓展研究:
(5)侯保荣院士专门研究海洋钢架结构桥海洋大气层梁腐蚀,他发现腐蚀最严重的是浪花飞溅区浪花飞溅区(海洋环境分区如图5),请你解释原因

(6)科学家还发现在
 浓度很小的海底也有厌氧微生物(如硫酸盐还原菌SRB)对海洋钢制部件的腐蚀,其原理如图6,已知溶液中的
浓度很小的海底也有厌氧微生物(如硫酸盐还原菌SRB)对海洋钢制部件的腐蚀,其原理如图6,已知溶液中的 完全转化为FeS,请写出该铁合金腐蚀的总反应
完全转化为FeS,请写出该铁合金腐蚀的总反应
(7)请列举出生产生活中金属制品的防腐措施
您最近一年使用:0次
2024-01-05更新
|
939次组卷
|
2卷引用:广东省东莞中学、广州二中、惠州一中等六校联考2023-2024学年高三上学期11月期中化学试题
名校
8 . 根据氧化还原反应的相关知识,回答下列问题:
(1)化学实验中,如使其步骤中的有害产物作为另一步骤的反应物,形成一个循环,就可不再向环境排放该种有害物质。如图:
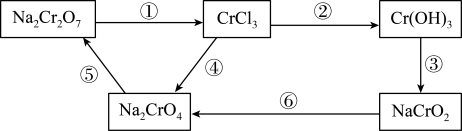
①需要加入氧化剂的反应是___________ (填编号,下同)。
②已知Na2Cr2O7在常温下,能与浓盐酸发生如下反应,请配平以下反应:__________ ,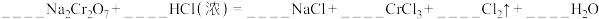 ,反应中:氧化剂是
,反应中:氧化剂是___________ ,氧化产物是___________ ;生成35.5gCl2时,被氧化的还原剂量为___________ g;浓盐酸体现出___________ 性。
(2)NaH可在野外作生氢剂,反应原理为 ,反应中氧化产物和还原产物的质量比为
,反应中氧化产物和还原产物的质量比为___________ 。
(3)有下列6种物质:K2SO4、K2SO3、I2、H2SO4、KIO3、H2O组成一个氧化还原反应,已知在反应中K2SO3失去电子,则反应的化学方程式为___________ 。
(1)化学实验中,如使其步骤中的有害产物作为另一步骤的反应物,形成一个循环,就可不再向环境排放该种有害物质。如图:

①需要加入氧化剂的反应是
②已知Na2Cr2O7在常温下,能与浓盐酸发生如下反应,请配平以下反应:
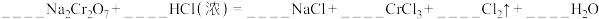 ,反应中:氧化剂是
,反应中:氧化剂是(2)NaH可在野外作生氢剂,反应原理为
 ,反应中氧化产物和还原产物的质量比为
,反应中氧化产物和还原产物的质量比为(3)有下列6种物质:K2SO4、K2SO3、I2、H2SO4、KIO3、H2O组成一个氧化还原反应,已知在反应中K2SO3失去电子,则反应的化学方程式为
您最近一年使用:0次
名校
9 . 完成下列问题。
(1)18世纪70年代,瑞典化学家舍勒将软锰矿(主要成分为 )与浓盐酸混合加热,产生了一种黄绿色有刺激性气味的气体。该反应的化学方程式为
)与浓盐酸混合加热,产生了一种黄绿色有刺激性气味的气体。该反应的化学方程式为_________ 。某同学拟用该原理按如下装置制备并收集纯净的氯气,在虚线框内选用的发生装置_________ (填“甲”“乙”或“丙”)。
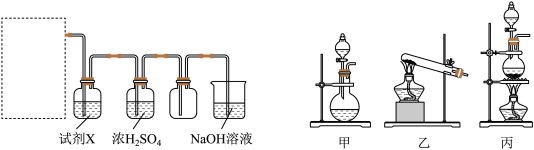
试剂X是________ 。可用NaOH溶液吸收尾气,反应的离子方程式为_______ 。
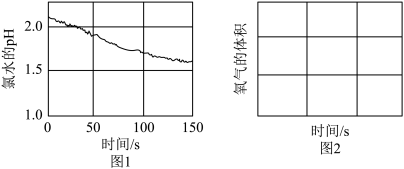
(2)通过大量实验证明,氯气与水反应生成次氯酸,次氯酸能杀菌消毒。可利用数字化实验探究次氯酸的化学性质,用强光照射氯水,得到氯水的pH随时间变化如图1所示,氯水的pH下降的原因是___________ (请用化学方程式说明),请在图2中画出氧气的体积随时间变化的趋势图___________ 。
(3)使用氯气消毒易产生危害人体健康的有机氯化物。用氯气和亚氯酸钠( )溶液可制备新的绿色消毒剂二氧化氯(
)溶液可制备新的绿色消毒剂二氧化氯( ),反应中还可得到氯化钠。该反应的化学方程式为
),反应中还可得到氯化钠。该反应的化学方程式为__________ 。
(4)随着科技的进步,科学家们又发现一种新型绿色消毒剂高铁酸钠。工业上制备高铁酸钠的一种方法的离子方程式为: 。分析
。分析 中Fe元素的化合价推测该微粒具有的性质
中Fe元素的化合价推测该微粒具有的性质__________ 。
(1)18世纪70年代,瑞典化学家舍勒将软锰矿(主要成分为
 )与浓盐酸混合加热,产生了一种黄绿色有刺激性气味的气体。该反应的化学方程式为
)与浓盐酸混合加热,产生了一种黄绿色有刺激性气味的气体。该反应的化学方程式为
试剂X是
(2)通过大量实验证明,氯气与水反应生成次氯酸,次氯酸能杀菌消毒。可利用数字化实验探究次氯酸的化学性质,用强光照射氯水,得到氯水的pH随时间变化如图1所示,氯水的pH下降的原因是

(3)使用氯气消毒易产生危害人体健康的有机氯化物。用氯气和亚氯酸钠(
 )溶液可制备新的绿色消毒剂二氧化氯(
)溶液可制备新的绿色消毒剂二氧化氯( ),反应中还可得到氯化钠。该反应的化学方程式为
),反应中还可得到氯化钠。该反应的化学方程式为(4)随着科技的进步,科学家们又发现一种新型绿色消毒剂高铁酸钠。工业上制备高铁酸钠的一种方法的离子方程式为:
 。分析
。分析 中Fe元素的化合价推测该微粒具有的性质
中Fe元素的化合价推测该微粒具有的性质
您最近一年使用:0次
名校
解题方法
10 . 金属钠是在1807年通过电解氢氧化钠制得的,这个原理应用于工业生产,约在1891年才获得成功。1921年实现了电解氯化钠制钠的工业方法,其反应原理是2NaCl(熔融) 2Na+Cl2↑。回答下列问题:
2Na+Cl2↑。回答下列问题:
(1)保存金属钠的正确方法是______。
(2)将一小块钠放在水平放置的试管中部,用酒精灯加热充分反应(如图所示,夹持装置略),请写出该反应的化学方程式:___________ ,生成物的颜色为___________ 。

(3) 、
、 久置于空气中最终都变为
久置于空气中最终都变为___________ (填化学式)。
(4)将一小块金属钠投入 溶液中,发生反应的总化学方程式为
溶液中,发生反应的总化学方程式为___________ 。
(5)配平化学方程式_________ 。
___________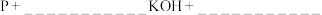 H2O=___________KH2PO2+______PH3
H2O=___________KH2PO2+______PH3
 2Na+Cl2↑。回答下列问题:
2Na+Cl2↑。回答下列问题:(1)保存金属钠的正确方法是______。
| A.放在棕色瓶中 | B.放在细沙中 | C.放在水中 | D.放在石蜡油中 |
(2)将一小块钠放在水平放置的试管中部,用酒精灯加热充分反应(如图所示,夹持装置略),请写出该反应的化学方程式:

(3)
 、
、 久置于空气中最终都变为
久置于空气中最终都变为(4)将一小块金属钠投入
 溶液中,发生反应的总化学方程式为
溶液中,发生反应的总化学方程式为(5)配平化学方程式
___________
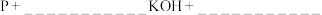 H2O=___________KH2PO2+______PH3
H2O=___________KH2PO2+______PH3
您最近一年使用:0次



