名校
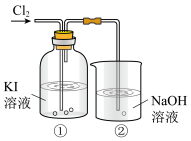
1 . 某研究小组利用下图所示装置探究卤素的性质。___________ (填“氧化性”或“还原性”)。
(2)①中溶液有I2生成,发生反应的化学方程式是___________ 。
(3)②中NaOH溶液的作用是吸收多余的氯气,发生反应的离子方程式是___________ 。
(2)①中溶液有I2生成,发生反应的化学方程式是
(3)②中NaOH溶液的作用是吸收多余的氯气,发生反应的离子方程式是
您最近一年使用:0次
2 . 现有下列六种物质:①液态氯化氢;②二氧化碳;③硫酸铜溶液;④熔融氯化钠;⑤ 固体;⑥铁丝.
固体;⑥铁丝.
(1)上述六种物质中,属于非电解质的是__________ ,能导电的电解质是__________ (填序号)。
(2)③和⑥反应的基本反应类型为__________ ,其离子方程式为__________ 。
(3)氯化氢在水溶液中的电离方程式为__________ 。
(4)向③中加入⑤的水溶液的现象为__________ 。
(5) 与⑤可能会发生如下反应,配平该方程式,并用双线桥标出电子得失
与⑤可能会发生如下反应,配平该方程式,并用双线桥标出电子得失______ 。
__________ __________
__________ __________
__________ __________
__________ __________
__________
 固体;⑥铁丝.
固体;⑥铁丝.(1)上述六种物质中,属于非电解质的是
(2)③和⑥反应的基本反应类型为
(3)氯化氢在水溶液中的电离方程式为
(4)向③中加入⑤的水溶液的现象为
(5)
 与⑤可能会发生如下反应,配平该方程式,并用双线桥标出电子得失
与⑤可能会发生如下反应,配平该方程式,并用双线桥标出电子得失__________
 __________
__________ __________
__________ __________
__________ __________
__________
您最近一年使用:0次
3 . 改善大气质量、进行污水处理和将垃圾资源化等要靠化学等科学的发展。
(1)为了保护环境,防治酸雨的方法是减少________ 的排放(填“ ”或“氟氯代烷”);减缓臭氧层受损的方法是减少使用
”或“氟氯代烷”);减缓臭氧层受损的方法是减少使用________ 。(填“ ”或“氟氯代烷”)
”或“氟氯代烷”)
(2)垃圾是放错地方的资源。下列垃圾处理方式正确的是________ (填字母代号)。
a.回收利用易拉罐 b.焚烧废旧报纸 c.随意丢弃废旧电池
我国“十四五”规划中已明确提到“碳达峰”、“碳中和”的目标,请回答下列问题:
(3)写出碳元素的两种同素异形体名称________ 。(任写两种)
(4)“碳达峰”、“碳中和”的“碳”主要指的具体物质是________ ,其所属物质类别为________ 。(填写下列正确的选项代号)
A.电解质 B.非电解质 C.酸性氧化物
(5)我国科学家合成一种新型催化剂,将二氧化碳和水反应生成甲烷和氧气,该反应的化学方程为:________ ,该反应中还原剂是________ 。
(6)某化学兴趣小组同学将燃烧的镁条插入盛满 的集气瓶内,发现镁条继续燃烧,生成白色固体,并有黑色物质附着在集气瓶内壁,反应的化学方程式为
的集气瓶内,发现镁条继续燃烧,生成白色固体,并有黑色物质附着在集气瓶内壁,反应的化学方程式为 ,试用双线桥分析该反应电子的得失及数目:
,试用双线桥分析该反应电子的得失及数目:________ 。
(1)为了保护环境,防治酸雨的方法是减少
 ”或“氟氯代烷”);减缓臭氧层受损的方法是减少使用
”或“氟氯代烷”);减缓臭氧层受损的方法是减少使用 ”或“氟氯代烷”)
”或“氟氯代烷”)(2)垃圾是放错地方的资源。下列垃圾处理方式正确的是
a.回收利用易拉罐 b.焚烧废旧报纸 c.随意丢弃废旧电池
我国“十四五”规划中已明确提到“碳达峰”、“碳中和”的目标,请回答下列问题:

(3)写出碳元素的两种同素异形体名称
(4)“碳达峰”、“碳中和”的“碳”主要指的具体物质是
A.电解质 B.非电解质 C.酸性氧化物
(5)我国科学家合成一种新型催化剂,将二氧化碳和水反应生成甲烷和氧气,该反应的化学方程为:
(6)某化学兴趣小组同学将燃烧的镁条插入盛满
 的集气瓶内,发现镁条继续燃烧,生成白色固体,并有黑色物质附着在集气瓶内壁,反应的化学方程式为
的集气瓶内,发现镁条继续燃烧,生成白色固体,并有黑色物质附着在集气瓶内壁,反应的化学方程式为 ,试用双线桥分析该反应电子的得失及数目:
,试用双线桥分析该反应电子的得失及数目:
您最近一年使用:0次
4 . A、储氢纳米碳管的研制成功体现了科技的进步。用电弧法合成的碳纳米管常伴有大量的杂质—碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其反应中的反应物和生成物有C、 、
、 、
、 、
、 、
、 和
和 七种。
七种。
(1)请用上述物质填空(不用配平):_____
 。
。
(2)上述反应中氧化剂是(填化学式)______ ,被氧化的元素是(填元素符号)______ 。
(3) 在上述反应中表现出来的性质是(填选项序号)______。
在上述反应中表现出来的性质是(填选项序号)______。
B、 与浓盐酸在一定温度下反应会生成黄绿色的易爆物质二氧化氯,其变化可表述为:
与浓盐酸在一定温度下反应会生成黄绿色的易爆物质二氧化氯,其变化可表述为: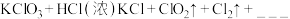
(4)请完成该化学方程式__________________
(5)浓盐酸在反应中显示出来的性质是______ (填写编号)。
①只有还原性②还原性和酸性③只有氧化性④氧化性和酸性
(6)若产生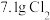 ,则生成
,则生成 的质量为
的质量为_____  。
。
(7) 具有很强的氧化性,因此常被用作消毒剂,其消毒的效率(用单位质量得到的电子数表示)是
具有很强的氧化性,因此常被用作消毒剂,其消毒的效率(用单位质量得到的电子数表示)是 的
的_____ 倍(小数点后保留两位数字)。
 、
、 、
、 、
、 、
、 和
和 七种。
七种。(1)请用上述物质填空(不用配平):
 。
。(2)上述反应中氧化剂是(填化学式)
(3)
 在上述反应中表现出来的性质是(填选项序号)______。
在上述反应中表现出来的性质是(填选项序号)______。| A.氧化性 | B.氧化性和酸性 | C.酸性 | D.还原性和酸性 |
B、
 与浓盐酸在一定温度下反应会生成黄绿色的易爆物质二氧化氯,其变化可表述为:
与浓盐酸在一定温度下反应会生成黄绿色的易爆物质二氧化氯,其变化可表述为: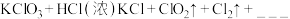
(4)请完成该化学方程式
(5)浓盐酸在反应中显示出来的性质是
①只有还原性②还原性和酸性③只有氧化性④氧化性和酸性
(6)若产生
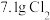 ,则生成
,则生成 的质量为
的质量为 。
。(7)
 具有很强的氧化性,因此常被用作消毒剂,其消毒的效率(用单位质量得到的电子数表示)是
具有很强的氧化性,因此常被用作消毒剂,其消毒的效率(用单位质量得到的电子数表示)是 的
的
您最近一年使用:0次
解题方法
5 . 按要求写出或完成下列方程式。(共15分)
(1)HNO3的电离方程式:___________ 。
(2)Na2CO3的电离方程式:___________ 。
(3)Zn与HCl反应的离子方程式:___________ 。
(4)HCl和NaOH反应的离子方程式:___________ 。
(5)将下列方程式配平:___________ 。
_______KMnO4+_______HCl(浓) _______KCl+_______MnCl2+_______H2O+_______Cl2↑
(1)HNO3的电离方程式:
(2)Na2CO3的电离方程式:
(3)Zn与HCl反应的离子方程式:
(4)HCl和NaOH反应的离子方程式:
(5)将下列方程式配平:
_______KMnO4+_______HCl(浓) _______KCl+_______MnCl2+_______H2O+_______Cl2↑
您最近一年使用:0次
名校
6 . 填空
(1)某一反应体系有反应物和生成物共五种物质: 、
、 、
、 、
、 、
、 。已知该反应中
。已知该反应中 只发生如下过程:
只发生如下过程:
①该反应中的还原剂是______ .
②该反应中,发生还原反应的过程是______ .
③写出该反应的化学方程式,并用单线桥标出电子转移的方向和数目______ .
④如反应转移了0.3mol电子,则产生的气体在标准状况下体积为______ .
(2)在反应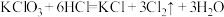 中,还原产物是
中,还原产物是______ ,反应中的氧化剂与还原剂物质的量之比为______ .
(1)某一反应体系有反应物和生成物共五种物质:
 、
、 、
、 、
、 、
、 。已知该反应中
。已知该反应中 只发生如下过程:
只发生如下过程:
①该反应中的还原剂是
②该反应中,发生还原反应的过程是
③写出该反应的化学方程式,并用单线桥标出电子转移的方向和数目
④如反应转移了0.3mol电子,则产生的气体在标准状况下体积为
(2)在反应
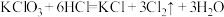 中,还原产物是
中,还原产物是
您最近一年使用:0次
解题方法
7 . 元素的价类二维图是我们学习元素及其化合物相关知识的重要模型和工具。如图是钠的价类二维图:
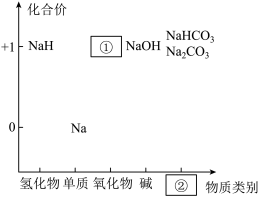
(1)②处应填的物质类别是___________ ;
(2)将钠放入水中发生反应的离子方程式是___________ ;
(3)Na可用石蜡封存,实验室少量Na保存于___________ 中;
(4)将Na2O2投入盛有CuSO4溶液的烧杯中,观察到的现象是___________(填标号);
(5)向酸性KMnO4溶液中加入Na2O2粉末,观察到溶液褪色,发生如下反应:
____ +____Na2O2+______→ ______Mn2++______Na++_____+_____H2O(未配平)
+____Na2O2+______→ ______Mn2++______Na++_____+_____H2O(未配平)
首先请补全方程式并配平__________ ,然后回答反应中被还原的元素是___________ ;反应中每消耗1molNa2O2的同时有___________ mol电子转移。

(1)②处应填的物质类别是
(2)将钠放入水中发生反应的离子方程式是
(3)Na可用石蜡封存,实验室少量Na保存于
(4)将Na2O2投入盛有CuSO4溶液的烧杯中,观察到的现象是___________(填标号);
| A.有气体生成 | B.无气体生成 | C.有蓝色沉淀生成 | D.大量红色固体铜生成 |
(5)向酸性KMnO4溶液中加入Na2O2粉末,观察到溶液褪色,发生如下反应:
____
 +____Na2O2+______→ ______Mn2++______Na++_____+_____H2O(未配平)
+____Na2O2+______→ ______Mn2++______Na++_____+_____H2O(未配平)首先请补全方程式并配平
您最近一年使用:0次
8 . Ⅰ.我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成,爆炸时发生的反应为: 请回答:
请回答:
(1)X的化学式是___________ 。
(2)在上述反应中,氧化剂是(填化学式)___________ 。
(3)写出在澄清石灰水溶液中通入过量的X气体发生反应的化学方程式___________ 。
II.高铁酸钠( )是一种新型绿色消毒剂,主要用于饮用水处理。工业制备高铁酸钠有多种方法。其中一种方法的化学原理可用离子方程式表示为:
)是一种新型绿色消毒剂,主要用于饮用水处理。工业制备高铁酸钠有多种方法。其中一种方法的化学原理可用离子方程式表示为:
(4)用单线桥 标出上述方程式的电子转移方向和数目___________ 。
(5)干法制备高铁酸钠主要反应为: ,
, 中铁元素的化合价是
中铁元素的化合价是___________ 价,每生成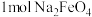 ,转移
,转移___________ 个电子。
(6) 与稀硫酸反应生成
与稀硫酸反应生成 和
和 ,通过测定生成
,通过测定生成 的质量,可计算
的质量,可计算 的纯度
的纯度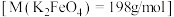 ,取
,取 产品与稀硫酸反应,测得生成
产品与稀硫酸反应,测得生成 的质量为ag。
的质量为ag。
①计算 的纯度=
的纯度=___________ (用最简分数表示)
②若将稀硫酸换成稀盐酸,生成的气体中含有 ,导致
,导致 的纯度的计算值
的纯度的计算值___________ 。(填“偏大”“偏小”或“无影响”)
 请回答:
请回答:(1)X的化学式是
(2)在上述反应中,氧化剂是(填化学式)
(3)写出在澄清石灰水溶液中通入过量的X气体发生反应的化学方程式
II.高铁酸钠(
 )是一种新型绿色消毒剂,主要用于饮用水处理。工业制备高铁酸钠有多种方法。其中一种方法的化学原理可用离子方程式表示为:
)是一种新型绿色消毒剂,主要用于饮用水处理。工业制备高铁酸钠有多种方法。其中一种方法的化学原理可用离子方程式表示为:
(4)用
(5)干法制备高铁酸钠主要反应为:
 ,
, 中铁元素的化合价是
中铁元素的化合价是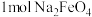 ,转移
,转移(6)
 与稀硫酸反应生成
与稀硫酸反应生成 和
和 ,通过测定生成
,通过测定生成 的质量,可计算
的质量,可计算 的纯度
的纯度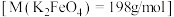 ,取
,取 产品与稀硫酸反应,测得生成
产品与稀硫酸反应,测得生成 的质量为ag。
的质量为ag。①计算
 的纯度=
的纯度=②若将稀硫酸换成稀盐酸,生成的气体中含有
 ,导致
,导致 的纯度的计算值
的纯度的计算值
您最近一年使用:0次
名校
9 . 氧化还原反应在日常生活和工业生产中有重要应用。
I. 是火柴工业用作制造火柴头的原料之一。已知反应:
是火柴工业用作制造火柴头的原料之一。已知反应: 。
。
(1)该反应中被氧化的元素是_______ ,还原产物是_______ 。
(2)该反应中氧化剂与还原剂的个数比为_______ 。
(3)生成标准状况下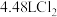 ,转移的电子个数为
,转移的电子个数为_______ (用 表示)。
表示)。
II.阅读下面一段材料并回答问题。
(4)K2FeO4中铁元素的化合价为_______ 。
(5)下列关于K2FeO4的说法中,不正确的是_______ 。
a.是强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(6)将K2FeO4与水反应的化学方程式补充完整并配平:_______ 。
_______K2FeO4+_______H2O=_______FeOH3(胶体)+_______+_______KOH
I.
 是火柴工业用作制造火柴头的原料之一。已知反应:
是火柴工业用作制造火柴头的原料之一。已知反应: 。
。(1)该反应中被氧化的元素是
(2)该反应中氧化剂与还原剂的个数比为
(3)生成标准状况下
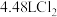 ,转移的电子个数为
,转移的电子个数为 表示)。
表示)。II.阅读下面一段材料并回答问题。
| 高铁酸钾使用说明书 【化学式】  【性状】暗紫色具有金属光泽的粉末,无臭无味 【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气。K2FeO4通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。K2FeO4与水反应还能产生具有强吸附性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用 【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理 【用量】消毒净化1L水投放5mgK2FeO4即可达到卫生标准 |
(5)下列关于K2FeO4的说法中,不正确的是
a.是强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(6)将K2FeO4与水反应的化学方程式补充完整并配平:
_______K2FeO4+_______H2O=_______FeOH3(胶体)+_______+_______KOH
您最近一年使用:0次
名校
解题方法
10 . Ⅰ.请回答以下问题:
(1)等质量的两种气体 、
、 分子数之比为
分子数之比为___________ ,相同条件下密度之比为___________ 。
(2)已知CO、 混合气体的质量共12.0g,在标准状况下的体积为6.72L,则混合气体中CO的质量分数为
混合气体的质量共12.0g,在标准状况下的体积为6.72L,则混合气体中CO的质量分数为___________ 。
Ⅱ.用电弧法合成碳纳米管,常伴有大量杂质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应方程式为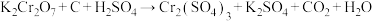 。
。
(3)配平该反应方程式:___________
(4)此反应的氧化产物为___________ 。
(5)要使10mL 1.0mol/L 溶液被还原至少要加入
溶液被还原至少要加入___________ mL 2.0mol/L的 溶液。
溶液。
(6)若产生6.72L (标准状况下)气体,该反应转移电子的物质的量为
(标准状况下)气体,该反应转移电子的物质的量为___________ mol。
(1)等质量的两种气体
 、
、 分子数之比为
分子数之比为(2)已知CO、
 混合气体的质量共12.0g,在标准状况下的体积为6.72L,则混合气体中CO的质量分数为
混合气体的质量共12.0g,在标准状况下的体积为6.72L,则混合气体中CO的质量分数为Ⅱ.用电弧法合成碳纳米管,常伴有大量杂质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应方程式为
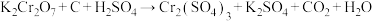 。
。(3)配平该反应方程式:
(4)此反应的氧化产物为
(5)要使10mL 1.0mol/L
 溶液被还原至少要加入
溶液被还原至少要加入 溶液。
溶液。(6)若产生6.72L
 (标准状况下)气体,该反应转移电子的物质的量为
(标准状况下)气体,该反应转移电子的物质的量为
您最近一年使用:0次



