名校
1 . 无机化合物可根据其组成和性质进行分类,分类比较是研究物质性质常用的一类方法。
(1)砷有多种化合物,其中As2O5溶于水缓慢化合生成一种三元酸(H3AsO4)。某工业废渣中含有As2O5、Fe2O3和MgO三种物质。现要分离提取 出砷元素,有同学建议用NaOH溶液,理由是_______ 。
(2)As2O3俗称砒霜,是宫廷剧中“鹤顶红”的有效成分,可以用马氏试砷法来检测砒霜。具体方法是:用Zn、盐酸和试样混在一起,将生成的气体导入热玻璃管,若试样中有砒霜,就会在热玻璃管中产生As,As积集而成亮黑色的“砷镜”。生成“砷镜”过程中共发生两个反应,①_______ ;②2AsH3=2As+3H2
(1)砷有多种化合物,其中As2O5溶于水缓慢化合生成一种三元酸(H3AsO4)。某工业废渣中含有As2O5、Fe2O3和MgO三种物质。现要
(2)As2O3俗称砒霜,是宫廷剧中“鹤顶红”的有效成分,可以用马氏试砷法来检测砒霜。具体方法是:用Zn、盐酸和试样混在一起,将生成的气体导入热玻璃管,若试样中有砒霜,就会在热玻璃管中产生As,As积集而成亮黑色的“砷镜”。生成“砷镜”过程中共发生两个反应,①
您最近一年使用:0次
2 . 高锰酸钾是一种典型的强氧化剂。完成下列填空:
Ⅰ:在用 酸性溶液处理
酸性溶液处理 和CuS的混合物时,发生的反应如下:
和CuS的混合物时,发生的反应如下:
①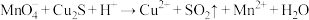 (未配平)
(未配平)
②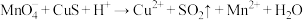 (未配平)
(未配平)
(1)下列关于反应①的说法中错误的是___________ (填字母序号)。
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8:5
c.生成2.24L(标况下) ,转移电子的物质的量是0.8mol
,转移电子的物质的量是0.8mol
d.还原性的强弱关系是: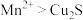
Ⅱ:在稀硫酸中, 与也能发生氧化还原反应。
与也能发生氧化还原反应。
(2)配平 与
与 反应的离子方程式:
反应的离子方程式:___________

(3)欲配制480mL0.1mol/L 溶液,需称取
溶液,需称取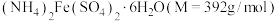 的质量为
的质量为___________ g,需要的玻璃仪器有___________ 。
Ⅲ:实验室可由软锰矿(主要成分为 )制备
)制备 ,方法如下:高温下使软锰矿与过量
,方法如下:高温下使软锰矿与过量 和
和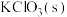 反应,生成
反应,生成 (锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液,
(锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液, 转化为
转化为 和
和 ;再滤去沉淀
;再滤去沉淀 ,浓缩结晶得到
,浓缩结晶得到 晶体。请回答:
晶体。请回答:
(4)用软锰矿制备 的化学方程式是:
的化学方程式是:___________ 。
(5) 转化为
转化为 的反应中氧化剂和还原剂的物质的量之比为
的反应中氧化剂和还原剂的物质的量之比为___________ 。
Ⅰ:在用
 酸性溶液处理
酸性溶液处理 和CuS的混合物时,发生的反应如下:
和CuS的混合物时,发生的反应如下:①
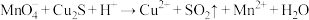 (未配平)
(未配平)②
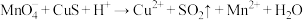 (未配平)
(未配平)(1)下列关于反应①的说法中错误的是
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8:5
c.生成2.24L(标况下)
 ,转移电子的物质的量是0.8mol
,转移电子的物质的量是0.8mold.还原性的强弱关系是:
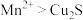
Ⅱ:在稀硫酸中,
 与也能发生氧化还原反应。
与也能发生氧化还原反应。(2)配平
 与
与 反应的离子方程式:
反应的离子方程式:
(3)欲配制480mL0.1mol/L
 溶液,需称取
溶液,需称取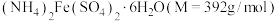 的质量为
的质量为Ⅲ:实验室可由软锰矿(主要成分为
 )制备
)制备 ,方法如下:高温下使软锰矿与过量
,方法如下:高温下使软锰矿与过量 和
和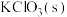 反应,生成
反应,生成 (锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液,
(锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液, 转化为
转化为 和
和 ;再滤去沉淀
;再滤去沉淀 ,浓缩结晶得到
,浓缩结晶得到 晶体。请回答:
晶体。请回答:(4)用软锰矿制备
 的化学方程式是:
的化学方程式是:(5)
 转化为
转化为 的反应中氧化剂和还原剂的物质的量之比为
的反应中氧化剂和还原剂的物质的量之比为
您最近一年使用:0次
解题方法
3 . 采用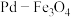 双催化剂,可实现用
双催化剂,可实现用 消除酸性废水中的
消除酸性废水中的 和
和 ,反应历程如图所示。其中
,反应历程如图所示。其中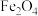 中
中 和
和 分别用
分别用 (II)、
(II)、 (III)表示。
(III)表示。
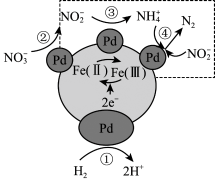
(1)用该法处理废水后,溶液的
_______ (填“降低”“升高”或“不变”)。
(2)写出过程④反应的离子方程式_______ 。
(3)反应历程中虚线方框内 生成
生成 的过程可描述为
的过程可描述为_______ 。
 双催化剂,可实现用
双催化剂,可实现用 消除酸性废水中的
消除酸性废水中的 和
和 ,反应历程如图所示。其中
,反应历程如图所示。其中 中
中 和
和 分别用
分别用 (II)、
(II)、 (III)表示。
(III)表示。
(1)用该法处理废水后,溶液的

(2)写出过程④反应的离子方程式
(3)反应历程中虚线方框内
 生成
生成 的过程可描述为
的过程可描述为
您最近一年使用:0次
4 .  、
、 、NO是有害气体,有多种方法处理有害气体的工艺。
、NO是有害气体,有多种方法处理有害气体的工艺。
Ⅰ.一种脱除 回收硫碘工艺的两个阶段主要反应分别如下:
回收硫碘工艺的两个阶段主要反应分别如下:
第一阶段: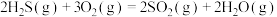
第二阶段:
(1)该工艺需控制第一阶段与第二阶段参加反应的 的物质的量之比
的物质的量之比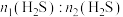 约为1:2.若过大,会导致
约为1:2.若过大,会导致_______ 。
(2) 溶液脱除空气中
溶液脱除空气中 并再生的原理如图所示。
并再生的原理如图所示。 溶液脱除空气中
溶液脱除空气中 的总反应化学方程式为
的总反应化学方程式为_______ 。

Ⅱ.有氧条件下,NO在催化剂作用下可被 还原为
还原为 。在钒基催化剂
。在钒基催化剂 作用下的脱硝反应机理如图所示。
作用下的脱硝反应机理如图所示。
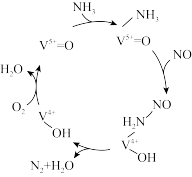
(3)根据如图机理,等物质的量的NO、 在有氧条件下的总化学方程式是
在有氧条件下的总化学方程式是_______ 。
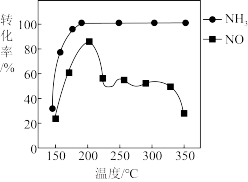
(4)按上述图中 、NO和
、NO和 的比例进行催化脱硝反应。相同反应时间,
的比例进行催化脱硝反应。相同反应时间, 和NO的转化率与温度的关系如图所示,200℃后,NO转化率急剧下降的原因是
和NO的转化率与温度的关系如图所示,200℃后,NO转化率急剧下降的原因是_______ 。
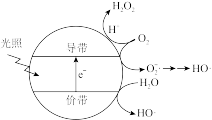
(5)羟基自由基(HO·)也可以用于脱硫脱硝。如图表示光催化氧化技术可生成HO·;光照时,价带失去电子产生有强氧化性的空穴,价带上 直接转化为HO·;描述产生HO·的另一种过程:
直接转化为HO·;描述产生HO·的另一种过程:_______ 。
 、
、 、NO是有害气体,有多种方法处理有害气体的工艺。
、NO是有害气体,有多种方法处理有害气体的工艺。Ⅰ.一种脱除
 回收硫碘工艺的两个阶段主要反应分别如下:
回收硫碘工艺的两个阶段主要反应分别如下:第一阶段:
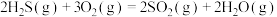
第二阶段:

(1)该工艺需控制第一阶段与第二阶段参加反应的
 的物质的量之比
的物质的量之比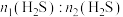 约为1:2.若过大,会导致
约为1:2.若过大,会导致(2)
 溶液脱除空气中
溶液脱除空气中 并再生的原理如图所示。
并再生的原理如图所示。 溶液脱除空气中
溶液脱除空气中 的总反应化学方程式为
的总反应化学方程式为
Ⅱ.有氧条件下,NO在催化剂作用下可被
 还原为
还原为 。在钒基催化剂
。在钒基催化剂 作用下的脱硝反应机理如图所示。
作用下的脱硝反应机理如图所示。
(3)根据如图机理,等物质的量的NO、
 在有氧条件下的总化学方程式是
在有氧条件下的总化学方程式是(4)按上述图中
 、NO和
、NO和 的比例进行催化脱硝反应。相同反应时间,
的比例进行催化脱硝反应。相同反应时间, 和NO的转化率与温度的关系如图所示,200℃后,NO转化率急剧下降的原因是
和NO的转化率与温度的关系如图所示,200℃后,NO转化率急剧下降的原因是
(5)羟基自由基(HO·)也可以用于脱硫脱硝。如图表示光催化氧化技术可生成HO·;光照时,价带失去电子产生有强氧化性的空穴,价带上
 直接转化为HO·;描述产生HO·的另一种过程:
直接转化为HO·;描述产生HO·的另一种过程:
您最近一年使用:0次
2022-05-28更新
|
724次组卷
|
5卷引用:湖南省2022-2023学年第十五届中学生数理化生综合实践活动高一化学应用知识展示A卷
湖南省2022-2023学年第十五届中学生数理化生综合实践活动高一化学应用知识展示A卷江苏省徐州市沛县2021-2022学年高一下学期第二次学情调研化学试题(已下线)期末模拟预测卷B-2022-2023学年高一化学下学期期中期末考点大串讲(人教版2019必修第二册)(已下线)第八章 化学与可持续发展(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第二册)(已下线)第八章 化学与可持续发展【单元测试B卷】
5 . 已知稀硝酸与足量的铁发生如下反应:Fe +HNO3 —— Fe(NO3)2+NO↑+H2O (未配平)
(1)该反应的氧化剂是_________ ,氧化产物是_________ 。
(2)请将方程式配平并用双线桥法表示出电子转移的方向和数目:________
□Fe +□HNO3 ==□Fe(NO3)2+□NO↑+□H2O
(3)当反应中转移 1.5mol 电子,计算被还原的HNO3的物质的量以及生成标准状况下NO气体的体积。_________ (要求写出解答过程)
(1)该反应的氧化剂是
(2)请将方程式配平并用双线桥法表示出电子转移的方向和数目:
□Fe +□HNO3 ==□Fe(NO3)2+□NO↑+□H2O
(3)当反应中转移 1.5mol 电子,计算被还原的HNO3的物质的量以及生成标准状况下NO气体的体积。
您最近一年使用:0次



