1 . 某元素X的氧化物很多,其中常见的有A、B两种
(1)A为黄绿色气体,其中X元素在化合物中化合价为+4价,氧含量为47.4%,可用于漂白木浆和水处理,A在液态和浓缩的气态时具有爆炸性,该气体为_______ ;
(2)B为黄棕色气体,氧含量为18.41%,当加热或遇电火花时会发生爆炸,该气体为_______ 。
(3)你认为这两种气体是否可以在防SARS中作为消毒剂_______
(4)写出气体A与NaOH反应的化学方程式_______ 。由于工业上大量使用的A具有爆炸性,A适宜存放在_______ (填“酸”或“碱”)性溶液中。
(5)用SO2还原X的+5价的盐,可制得A,写出该反应的离子方程式_______ 。
(1)A为黄绿色气体,其中X元素在化合物中化合价为+4价,氧含量为47.4%,可用于漂白木浆和水处理,A在液态和浓缩的气态时具有爆炸性,该气体为
(2)B为黄棕色气体,氧含量为18.41%,当加热或遇电火花时会发生爆炸,该气体为
(3)你认为这两种气体是否可以在防SARS中作为消毒剂_______
| A.都可以 | B.都不可以 | C.只有气体A可以 | D.只有气体B可以 |
(5)用SO2还原X的+5价的盐,可制得A,写出该反应的离子方程式
您最近一年使用:0次
2 . 铬化学丰富多彩,由于铬光泽度好,常将铬镀在其他金属表面,同铁、镍组成各种性能的不锈钢,CrO3 大量地用于电镀工业中。
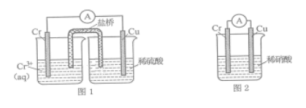
(1)在下图装置中,观察到图1装置铜电极上产生大量的无色气泡,而图2装置中铜电极上无气体产生,铬电极上产生大量有色气体。根据上述现象试推测金属铬的两个重要化学性质___________ 、___________ 。
(2) CrO3 具有强氧化性,遇到有机物(如酒精)时,猛烈反应以至着火,若该过程中乙醇被氧化成乙酸,CrO3 被还原成绿色的硫酸铬[Cr2(SO4)3]。则该反应的化学方程式为___________ 。
(3) CrO3 的热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如下图所示。
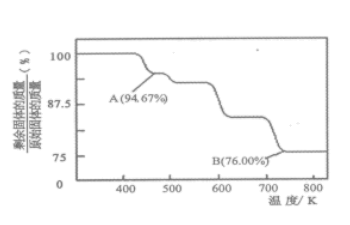
①A点时剩余固体的成分是___________ (填化学式)
②从开始加热到750K 时总反应方程式为___________ 。
(4) CrO3和K2Cr2O7 均易溶于水,这是工业上造成铬污染的主要原因。净化处理方法之一是将含+6价Cr的废水放入电解槽内,用铁作阳极,加入适量的NaCl进行电解:阳极区生成的Fe2+和Cr2O 发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3 和Cr(OH)3沉淀除去[已知KspFe(OH)3=4.0×10-38,KspCr(OH)3=6. 0 × 10-31]。
发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3 和Cr(OH)3沉淀除去[已知KspFe(OH)3=4.0×10-38,KspCr(OH)3=6. 0 × 10-31]。
①电解过程中NaCl的作用是___________ 。
②已知电解后的溶液中c(Fe3+)为2.0×10-13mol·L-1,则溶液中c(Cr3+)为___________ mol·L-1。
(1)在下图装置中,观察到图1装置铜电极上产生大量的无色气泡,而图2装置中铜电极上无气体产生,铬电极上产生大量有色气体。根据上述现象试推测金属铬的两个重要化学性质

(2) CrO3 具有强氧化性,遇到有机物(如酒精)时,猛烈反应以至着火,若该过程中乙醇被氧化成乙酸,CrO3 被还原成绿色的硫酸铬[Cr2(SO4)3]。则该反应的化学方程式为
(3) CrO3 的热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如下图所示。

①A点时剩余固体的成分是
②从开始加热到750K 时总反应方程式为
(4) CrO3和K2Cr2O7 均易溶于水,这是工业上造成铬污染的主要原因。净化处理方法之一是将含+6价Cr的废水放入电解槽内,用铁作阳极,加入适量的NaCl进行电解:阳极区生成的Fe2+和Cr2O
 发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3 和Cr(OH)3沉淀除去[已知KspFe(OH)3=4.0×10-38,KspCr(OH)3=6. 0 × 10-31]。
发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3 和Cr(OH)3沉淀除去[已知KspFe(OH)3=4.0×10-38,KspCr(OH)3=6. 0 × 10-31]。①电解过程中NaCl的作用是
②已知电解后的溶液中c(Fe3+)为2.0×10-13mol·L-1,则溶液中c(Cr3+)为
您最近一年使用:0次
解题方法
3 . 写出下列反应的方程式
(1)硫代硫酸钠与稀盐酸混合,生成有刺激性气味的气体_______
(2)氯酸钾、硫酸锰与氢氧化钾共熔,生成绿色物质_______
(3)在重铬酸钾溶液中加入少量银离子,生成砖红色沉淀_______
(4)金溶解在王水中_______
(1)硫代硫酸钠与稀盐酸混合,生成有刺激性气味的气体
(2)氯酸钾、硫酸锰与氢氧化钾共熔,生成绿色物质
(3)在重铬酸钾溶液中加入少量银离子,生成砖红色沉淀
(4)金溶解在王水中
您最近一年使用:0次
4 . 根据英国地质调查局的报告,我国是世界上锑产量最大的国家,产量占全球的84%。锑在自然界中主要存在于辉锑矿(Sb2S3)中,湖南省冷水江市的锡矿山是世界最大锑矿,估计储量为210万吨。
(1)写出锑原子的核外电子排布,并以此判断其最常见的三个化合价:_______ 。
(2)在一些安全火柴的火柴头中使用了三硫化二锑。写出其燃烧时的化学反应方程式:_______ 。
(3)锑有两种常见氟化物。取其高价态的氟化物,在它的HF溶液中慢慢加入H2O2,得锑含量为44.97%的白色离子化合物A,其阴离子呈八面体结构。A的结构简式为_______ ,A不稳定,易缓慢分解为B和某种气体,写出生成B的化学方程式:_______ 。
(1)写出锑原子的核外电子排布,并以此判断其最常见的三个化合价:
(2)在一些安全火柴的火柴头中使用了三硫化二锑。写出其燃烧时的化学反应方程式:
(3)锑有两种常见氟化物。取其高价态的氟化物,在它的HF溶液中慢慢加入H2O2,得锑含量为44.97%的白色离子化合物A,其阴离子呈八面体结构。A的结构简式为
您最近一年使用:0次
5 . 烟道气中的NOx是主要的大气污染物之一,为了监测某工厂烟道气中NOx含量,采集标准状况下50.00mL烟道气经除尘、干燥后缓慢通入适量酸化的H2O2的溶液中,使NOx完全被氧化为NO ,除去多余的H2O2并加水稀释至100.00mL。量取20.00mL该溶液,加入30.00mL0.01000mol/LFeSO4标准溶液(过量),充分反应后,用0.001000mol/LK2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液10.00mL。(假设NO
,除去多余的H2O2并加水稀释至100.00mL。量取20.00mL该溶液,加入30.00mL0.01000mol/LFeSO4标准溶液(过量),充分反应后,用0.001000mol/LK2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液10.00mL。(假设NO 的还原产物全为NO,且NO全部从溶液中逸出)
的还原产物全为NO,且NO全部从溶液中逸出)
(1)写出NO被H2O2氧化为NO 的离子方程式
的离子方程式_______
(2)与量取的20.00mL溶液中NO 反应的Fe2+为
反应的Fe2+为_______ mol?若FeSO4标准溶液部分变质,会使NOx含量测定结果如何_______ (答偏高、偏低或者无影响)
(3)标准状况下该工程烟道气中NOx(折合为NO2)的含量为每立方米_______ 毫克?
 ,除去多余的H2O2并加水稀释至100.00mL。量取20.00mL该溶液,加入30.00mL0.01000mol/LFeSO4标准溶液(过量),充分反应后,用0.001000mol/LK2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液10.00mL。(假设NO
,除去多余的H2O2并加水稀释至100.00mL。量取20.00mL该溶液,加入30.00mL0.01000mol/LFeSO4标准溶液(过量),充分反应后,用0.001000mol/LK2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液10.00mL。(假设NO 的还原产物全为NO,且NO全部从溶液中逸出)
的还原产物全为NO,且NO全部从溶液中逸出)(1)写出NO被H2O2氧化为NO
 的离子方程式
的离子方程式(2)与量取的20.00mL溶液中NO
 反应的Fe2+为
反应的Fe2+为(3)标准状况下该工程烟道气中NOx(折合为NO2)的含量为每立方米
您最近一年使用:0次



