1 . 次氯酸钠溶液和二氯异氰尿酸钠(C3N3O3Cl2Na)都是常用的杀菌消毒剂。 NaClO可用于制备二氯异氰尿酸钠.
(1)NaClO溶液可由低温下将Cl2缓慢通入NaOH溶液中而制得。制备 NaClO的离子方程式为__________ ;用于环境杀菌消毒的NaClO溶液须稀释并及时使用,若在空气中暴露时间过长且见光,将会导致消毒作用减弱,其原因是__________________ 。
(2)二氯异氰尿酸钠优质品要求有效氯大于60%。通过下列实验检测二氯异氰尿酸钠样品是否达到优质品标准。实验检测原理为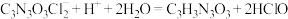


准确称取1.1200g样品,用容量瓶配成250.0mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;用 Na2S2O3标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液20.00mL。
Na2S2O3标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液20.00mL。
①通过计算判断该样品是否为优质品_______ 。(写出计算过程,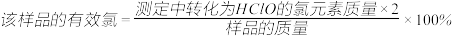 )
)
②若在检测中加入稀硫酸的量过少,将导致样品的有效氯测定值____________ (填“偏高”或“偏低”)。
(1)NaClO溶液可由低温下将Cl2缓慢通入NaOH溶液中而制得。制备 NaClO的离子方程式为
(2)二氯异氰尿酸钠优质品要求有效氯大于60%。通过下列实验检测二氯异氰尿酸钠样品是否达到优质品标准。实验检测原理为
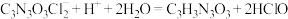


准确称取1.1200g样品,用容量瓶配成250.0mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;用
 Na2S2O3标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液20.00mL。
Na2S2O3标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液20.00mL。①通过计算判断该样品是否为优质品
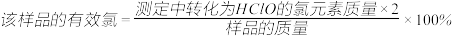 )
)②若在检测中加入稀硫酸的量过少,将导致样品的有效氯测定值
您最近一年使用:0次
2020-07-11更新
|
5032次组卷
|
16卷引用:2020年江苏卷化学高考试题
2020年江苏卷化学高考试题江苏省苏州中学2020-2021学年高一下学期期初化学试卷江苏省徐州市王杰中学2021-2022学年高三10月学情调研化学试题(已下线)2020年江苏卷化学高考真题变式题16-21(已下线)实验综合题(已下线)专题13 元素及其化合物知识的综合应用-2020年高考真题和模拟题化学分项汇编(已下线)专题08 常见无机物及其应用——备战2021年高考化学纠错笔记(已下线)小题25 定量实验 ——备战2021年高考化学经典小题考前必刷(全国通用)(已下线)考点31 物质的制备 定量分析-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点33 物质的定性与定量分析-备战2022年高考化学一轮复习考点帮(浙江专用)甘肃省天水市一中2022届高三上学期8月第一次考试化学试题(已下线)解密02 物质的量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密02 物质的量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)考点05 氧化还原反应-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点52 定量分析-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第22讲 水的电离与溶液的pH(讲)-2023年高考化学一轮复习讲练测(新教材新高考)
真题
2 . 过氧化钙(CaO2·8H2O)是一种在水产养殖中广泛使用的供氧剂。
(1)Ca(OH)2悬浊液与H2O2溶液反应可制备CaO2·8H2O。
Ca(OH)2+H2O2+6H2O=CaO2·8H2O
反应时通常加入过量的Ca(OH)2,其目的是___________ 。
(2)向池塘水中加入一定量的CaO2·8H2O后,池塘水中浓度增加的离子有___________ (填序号)。
A.Ca2+B.H+C.CO D.OH−
D.OH−
(3)水中溶解氧的测定方法如下:向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置;加入适量稀H2SO4,待MnO(OH)2与I−完全反应生成Mn2+和I2后,以淀粉作指示剂,用Na2S2O3标准溶液滴定至终点,测定过程中物质的转化关系如下:
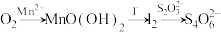
①写出O2将Mn2+氧化成MnO(OH)2的离子方程式:___________ 。
②取加过一定量CaO2·8H2O的池塘水样100.00mL,按上述方法测定水中溶解氧量,消耗0.01000mol·L−1Na2S2O3标准溶液13.50mL。计算该水样中的溶解氧(以mg·L−1表示),写出计算过程___________ 。
(1)Ca(OH)2悬浊液与H2O2溶液反应可制备CaO2·8H2O。
Ca(OH)2+H2O2+6H2O=CaO2·8H2O
反应时通常加入过量的Ca(OH)2,其目的是
(2)向池塘水中加入一定量的CaO2·8H2O后,池塘水中浓度增加的离子有
A.Ca2+B.H+C.CO
 D.OH−
D.OH−(3)水中溶解氧的测定方法如下:向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置;加入适量稀H2SO4,待MnO(OH)2与I−完全反应生成Mn2+和I2后,以淀粉作指示剂,用Na2S2O3标准溶液滴定至终点,测定过程中物质的转化关系如下:
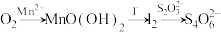
①写出O2将Mn2+氧化成MnO(OH)2的离子方程式:
②取加过一定量CaO2·8H2O的池塘水样100.00mL,按上述方法测定水中溶解氧量,消耗0.01000mol·L−1Na2S2O3标准溶液13.50mL。计算该水样中的溶解氧(以mg·L−1表示),写出计算过程
您最近一年使用:0次
2016-12-09更新
|
8612次组卷
|
7卷引用:2016年全国普通高等学校招生统一考试化学(江苏卷精编版)
真题
名校
3 . 硫化氢的转化是资源利用和环境保护的重要研究课题。由硫化氢获得硫单质有多种方法。
(1)将烧碱吸收H2S后的溶液加入到如题图—1所示的电解池的阳极区进行电解。电解过程中阳极区发生如下反应:S2-—2e-=S(n—1)S+ S2-=Sn2-。
①写出电解时阴极的电极反应式:__________________ 。
②电解后阳极区的溶液用稀硫酸酸化得到硫单质,其离子方程式可写成_____________ 。
(2)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如题图—2所示。
①在图示的转化中,化合价不变的元素是___________ 。
②反应中当有1molH2S转化为硫单质时,保持溶液中Fe3+的物质的量不变,需要消耗O2的物质的量为_______________ 。
③在温度一定和不补加溶液的条件下,缓慢通入混合气体,并充分搅拌。欲使生成的硫单质中不含CuS,可采取的措施有___________________ 。
(3)H2S在高温下分解生成硫蒸气和H2。若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如题图—3所示,H2S在高温下分解反应的化学方程式为_____________ 。
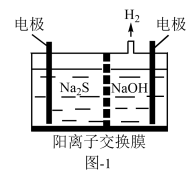


(1)将烧碱吸收H2S后的溶液加入到如题图—1所示的电解池的阳极区进行电解。电解过程中阳极区发生如下反应:S2-—2e-=S(n—1)S+ S2-=Sn2-。
①写出电解时阴极的电极反应式:
②电解后阳极区的溶液用稀硫酸酸化得到硫单质,其离子方程式可写成
(2)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如题图—2所示。
①在图示的转化中,化合价不变的元素是
②反应中当有1molH2S转化为硫单质时,保持溶液中Fe3+的物质的量不变,需要消耗O2的物质的量为
③在温度一定和不补加溶液的条件下,缓慢通入混合气体,并充分搅拌。欲使生成的硫单质中不含CuS,可采取的措施有
(3)H2S在高温下分解生成硫蒸气和H2。若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如题图—3所示,H2S在高温下分解反应的化学方程式为



您最近一年使用:0次
2016-12-09更新
|
2718次组卷
|
5卷引用:2014年全国普通高等学校招生统一考试理科综合能力测试化学(江苏卷)
2014年全国普通高等学校招生统一考试理科综合能力测试化学(江苏卷)2016届江苏省南通市天星湖中学高三上学期第一次阶段测化学试卷(已下线)2019高考备考二轮复习精品资料-专题3 氧化还原反应(教学案)北京市海淀区中央民族大学附属中学2020届高三考前热身化学试题北京市清华大学附属中学2020届高三三模试卷化学试题
真题
4 . 废旧印刷电路板的回收利用可实现资源再生,并减少污染。废旧印刷电路板经粉碎分离,能得到非金属粉末和金属粉末。
(1)下列处理印刷电路板非金属粉末的方法中,不符合环境保护理念的是___ (填字母)
(2)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) △H=64.39kJ·mol-1
2H2O2(l)=2H2O(l)+O2(g) △H=-196.46kJ·mol-1
H2(g)+1/2O2(g)=H2O(l) △H=-285.84kJ·mol-1
在H2SO4溶液中Cu 与H2O2反应生成Cu2+和H2O的热化学方程式为:__________ 。
(3)控制其它条件相同,印刷电路板的金属粉末用10%H2O2 和3.0mol·L-1
H2SO4溶液处理,测得不同温度下铜的平均溶解速率(见下表)
当温度高于40℃时,铜的平均溶解速率随着反应温度的升高而下降,
其主要原因是_________________________________________ 。
(4)在提纯后的CuSO4溶液中加入一定量的Na2SO3和NaCl 溶液,加热,生成
CuCl 的离子方程式是___________________________________ 。
(1)下列处理印刷电路板非金属粉末的方法中,不符合环境保护理念的是
| A.热裂解形成燃油 | B.露天焚烧 |
| C.作为有机复合建筑材料的原料 | D.直接填埋 |
(2)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) △H=64.39kJ·mol-1
2H2O2(l)=2H2O(l)+O2(g) △H=-196.46kJ·mol-1
H2(g)+1/2O2(g)=H2O(l) △H=-285.84kJ·mol-1
在H2SO4溶液中Cu 与H2O2反应生成Cu2+和H2O的热化学方程式为:
(3)控制其它条件相同,印刷电路板的金属粉末用10%H2O2 和3.0mol·L-1
H2SO4溶液处理,测得不同温度下铜的平均溶解速率(见下表)
| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 铜的平均溶解速率 (×10-3mol·L-1·min-1) | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
当温度高于40℃时,铜的平均溶解速率随着反应温度的升高而下降,
其主要原因是
(4)在提纯后的CuSO4溶液中加入一定量的Na2SO3和NaCl 溶液,加热,生成
CuCl 的离子方程式是
您最近一年使用:0次
2016-12-09更新
|
1513次组卷
|
3卷引用:2009年普通高等学校招生统一考试化学试题(江苏卷)



