21-22高二下·江苏扬州·开学考试
1 . 脱硝技术主要用于脱除燃煤烟气中的NO。
I.配合物生物脱硝法
以Fe(II)EDTA2-为吸收剂结合微生物进行脱硝的原理如图所示:

已知:NO 、NO
、NO 会使微生物总量下降。
会使微生物总量下降。
(1)若烟气中参与反应的n(NO):n(O2)=1:1,碳源为C6H12O6,写出过程中脱硝总反应的化学方程式_______ 。
(2)该原理中将“化学吸收”与“生物还原”分开在不同容器中进行的原因是_______ 。
Ⅱ.ClO2氧化脱硝法
电解NaClO3制备ClO2的装置如图所示。

(3)写出该电解过程中总反应的化学方程式_______ 。
(4)ClO2氧化脱硝过程发生的反应是:5NO+3ClO2+4H2O=5HNO3+3HCl。已知:①ClO2与水能产生•OH,•OH更易与NO反应;②ClO2受热易分解,反应为2ClO2=Cl2+2O2。当烟气流速、烟气中NO浓度及n(ClO2)/n(NO)一定时,温度对NO脱除效率的影响如图所示。温度升高,脱硝率变化不大的原因可能是_______ 。

(5)烟气中混有的SO2能与ClO2反应。
①写出SO2与溶液中ClO2反应的离子方程式_______ 。
②其他条件一定时,SO2浓度的增加对脱硝率影响不大,其原因可能是_______ 。
I.配合物生物脱硝法
以Fe(II)EDTA2-为吸收剂结合微生物进行脱硝的原理如图所示:

已知:NO
 、NO
、NO 会使微生物总量下降。
会使微生物总量下降。(1)若烟气中参与反应的n(NO):n(O2)=1:1,碳源为C6H12O6,写出过程中脱硝总反应的化学方程式
(2)该原理中将“化学吸收”与“生物还原”分开在不同容器中进行的原因是
Ⅱ.ClO2氧化脱硝法
电解NaClO3制备ClO2的装置如图所示。

(3)写出该电解过程中总反应的化学方程式
(4)ClO2氧化脱硝过程发生的反应是:5NO+3ClO2+4H2O=5HNO3+3HCl。已知:①ClO2与水能产生•OH,•OH更易与NO反应;②ClO2受热易分解,反应为2ClO2=Cl2+2O2。当烟气流速、烟气中NO浓度及n(ClO2)/n(NO)一定时,温度对NO脱除效率的影响如图所示。温度升高,脱硝率变化不大的原因可能是

(5)烟气中混有的SO2能与ClO2反应。
①写出SO2与溶液中ClO2反应的离子方程式
②其他条件一定时,SO2浓度的增加对脱硝率影响不大,其原因可能是
您最近一年使用:0次
2022·江苏·一模
名校
解题方法
2 . 水溶性硝态氮(以NO 、NO
、NO 等形式存在)是水体污染物之一,须处理达到国家规定的标准后才能排放。
等形式存在)是水体污染物之一,须处理达到国家规定的标准后才能排放。
(1)在反硝化细菌作用下,用葡萄糖处理酸性废水中的NO ,产生两种对大气无污染的气体。该反应的离子方程式为
,产生两种对大气无污染的气体。该反应的离子方程式为___________ 。
(2)纳米铁铜双金属有巨大的比表面积和很高的反应活性,可用于水体脱硝。
① 纳米铁铜双金属与普通铁铜双金属脱硝效果(以处理某硝酸盐为例)如图-1所示。在0到20min内,纳米铁铜双金属脱硝效果显著,其原因可能是___________ 。
② 研究表明水体中溶解氧的存在降低了纳米铁铜双金属脱硝的效果,验证的实验方案是______ 。

(3)Jetten 等人提出了利用厌氧氨氧化菌细胞中的三种酶处理废水中NH3和NO 的生化反应模型,其反应机理如图-2所示。在NR酶和HH酶作用下的反应过程可分别描述为
的生化反应模型,其反应机理如图-2所示。在NR酶和HH酶作用下的反应过程可分别描述为___________ 、___________ 。
 、NO
、NO 等形式存在)是水体污染物之一,须处理达到国家规定的标准后才能排放。
等形式存在)是水体污染物之一,须处理达到国家规定的标准后才能排放。(1)在反硝化细菌作用下,用葡萄糖处理酸性废水中的NO
 ,产生两种对大气无污染的气体。该反应的离子方程式为
,产生两种对大气无污染的气体。该反应的离子方程式为(2)纳米铁铜双金属有巨大的比表面积和很高的反应活性,可用于水体脱硝。
① 纳米铁铜双金属与普通铁铜双金属脱硝效果(以处理某硝酸盐为例)如图-1所示。在0到20min内,纳米铁铜双金属脱硝效果显著,其原因可能是
② 研究表明水体中溶解氧的存在降低了纳米铁铜双金属脱硝的效果,验证的实验方案是

(3)Jetten 等人提出了利用厌氧氨氧化菌细胞中的三种酶处理废水中NH3和NO
 的生化反应模型,其反应机理如图-2所示。在NR酶和HH酶作用下的反应过程可分别描述为
的生化反应模型,其反应机理如图-2所示。在NR酶和HH酶作用下的反应过程可分别描述为
您最近一年使用:0次
2022-01-11更新
|
897次组卷
|
5卷引用:江苏省南京市、盐城市2021-2022学年高三第一次模拟考试(原理综合题)
(已下线)江苏省南京市、盐城市2021-2022学年高三第一次模拟考试(原理综合题)(已下线)江苏省南京市、盐城市2021-2022学年高三第一次模拟考试(反应原理-氧化还原反应)(已下线)江苏省南京市、盐城市2021-2022学年高三第一次模拟考试(原理综合题)江苏省南京市、盐城市2021-2022学年高三第一次模拟考试化学试题江苏省丹阳高级中学2022-2023学年高一下学期第二次月考化学试卷
2022·江苏·一模
名校
3 . 电解法制取高纯镍的原料液中含Cu(II)(主要以Cu2+、CuCl+、CuCl2等形式存在)杂质,为保证高纯镍产品的纯度,电解前须将Cu(II)除去,方法如下。
(1)S−SO2除铜:向原料液中加入适量细硫粉并鼓入SO2,将Cu(II)转化为CuS沉淀除去。Cu2+沉淀时发生反应的离子方程式为___________ 。
(2)NiS除铜:向原料液中加入活性NiS粉末,将Cu(II)转化为CuS沉淀除去。过滤后的滤渣即为除铜渣(含NiS、CuS等)。
① 室温下,CuCl+和活性NiS粉末反应的离子方程式为___________ ;该反应的平衡常数表达式为K=___________ 。
② 如图−1所示,将活性NiS粉末陈化(露置)超过7小时后再用于除铜的效果明显变差,其原因可能是___________ 。

③ 除铜渣中铜镍质量比随原料液pH的变化如图−2所示,实验测得溶液pH=3.5时除铜渣中铜镍质量比最大,其原因可能是___________ 。
(1)S−SO2除铜:向原料液中加入适量细硫粉并鼓入SO2,将Cu(II)转化为CuS沉淀除去。Cu2+沉淀时发生反应的离子方程式为
(2)NiS除铜:向原料液中加入活性NiS粉末,将Cu(II)转化为CuS沉淀除去。过滤后的滤渣即为除铜渣(含NiS、CuS等)。
① 室温下,CuCl+和活性NiS粉末反应的离子方程式为
② 如图−1所示,将活性NiS粉末陈化(露置)超过7小时后再用于除铜的效果明显变差,其原因可能是

③ 除铜渣中铜镍质量比随原料液pH的变化如图−2所示,实验测得溶液pH=3.5时除铜渣中铜镍质量比最大,其原因可能是
您最近一年使用:0次
2022-01-11更新
|
873次组卷
|
4卷引用:江苏省南京市、盐城市2021-2022学年高三第一次模拟考试(原理综合题)
(已下线)江苏省南京市、盐城市2021-2022学年高三第一次模拟考试(原理综合题)(已下线)江苏省南京市、盐城市2021-2022学年高三第一次模拟考试(原理综合题)江苏省南京市、盐城市2021-2022学年高三第一次模拟考试化学试题湖南师范大学附属中学2022届高三月考(七)化学试题
21-22高二上·海南省直辖县级单位·阶段练习
4 . 合理利用或转化NO2、NO、CO等污染性气体是人们共同关注的课题。
(1)实验证明汽车尾气中的NO与CO反应生成无污染气体而除去。
已知:i.N2(g)和O2(g)生成NO(g)过程中的能量变化如下:
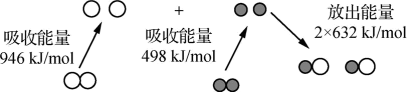
ii.NO2(g)+CO(g) CO2(g)+NO(g) ΔH=-234kJ·mol−1
CO2(g)+NO(g) ΔH=-234kJ·mol−1
iii.1mol NO(g)被O2(g)氧化时放出的热量为56.15kJ
①反应2NO(g)+2CO(g) 2CO2(g)+N2(g) ΔH=
2CO2(g)+N2(g) ΔH=_____ kJ·mol−1。
②工业上常用醋酸亚铜氨溶液来吸收CO,反应的化学方程式如下:CH3COOCu(NH3)2(aq)+CO(g) CH3COOCu(NH3)2·CO(aq) ΔH<0,吸收CO后的溶液经过适当处理又可以重新生成醋酸亚铜氨,可采取的处理措施有
CH3COOCu(NH3)2·CO(aq) ΔH<0,吸收CO后的溶液经过适当处理又可以重新生成醋酸亚铜氨,可采取的处理措施有_____ (选填序号)。
A.适当升高温度 B.适当降低温度 C.适当增大压强 D.适当减小压强
(2)选择性催化还原技术(SCR)是目前较为成熟的烟气脱硝技术,一般采用NH3或尿素[CO(NH2)2]作还原剂,基本流程如图所示:
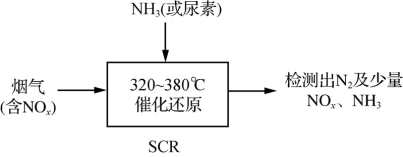
①SCR脱硝技术中用NH3作还原剂还原NO的主要反应为4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g) ΔH<0,1mol O2能氧化NH3的物质的量是
4N2(g)+6H2O(g) ΔH<0,1mol O2能氧化NH3的物质的量是_____ 。若用CO(NH2)2作还原剂,还原NO2的化学方程式为___________ 。
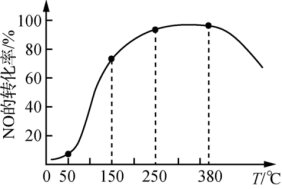
②其他条件不变,在相同时间内,NO转化为N2的转化率随温度的变化如图所示。反应温度在50℃~150℃范围内,NO转化为N2的转化率迅速上升,原因有___________ 。
(1)实验证明汽车尾气中的NO与CO反应生成无污染气体而除去。
已知:i.N2(g)和O2(g)生成NO(g)过程中的能量变化如下:

ii.NO2(g)+CO(g)
 CO2(g)+NO(g) ΔH=-234kJ·mol−1
CO2(g)+NO(g) ΔH=-234kJ·mol−1iii.1mol NO(g)被O2(g)氧化时放出的热量为56.15kJ
①反应2NO(g)+2CO(g)
 2CO2(g)+N2(g) ΔH=
2CO2(g)+N2(g) ΔH=②工业上常用醋酸亚铜氨溶液来吸收CO,反应的化学方程式如下:CH3COOCu(NH3)2(aq)+CO(g)
 CH3COOCu(NH3)2·CO(aq) ΔH<0,吸收CO后的溶液经过适当处理又可以重新生成醋酸亚铜氨,可采取的处理措施有
CH3COOCu(NH3)2·CO(aq) ΔH<0,吸收CO后的溶液经过适当处理又可以重新生成醋酸亚铜氨,可采取的处理措施有A.适当升高温度 B.适当降低温度 C.适当增大压强 D.适当减小压强
(2)选择性催化还原技术(SCR)是目前较为成熟的烟气脱硝技术,一般采用NH3或尿素[CO(NH2)2]作还原剂,基本流程如图所示:

①SCR脱硝技术中用NH3作还原剂还原NO的主要反应为4NH3(g)+4NO(g)+O2(g)
 4N2(g)+6H2O(g) ΔH<0,1mol O2能氧化NH3的物质的量是
4N2(g)+6H2O(g) ΔH<0,1mol O2能氧化NH3的物质的量是②其他条件不变,在相同时间内,NO转化为N2的转化率随温度的变化如图所示。反应温度在50℃~150℃范围内,NO转化为N2的转化率迅速上升,原因有

您最近一年使用:0次
21-22高三上·江苏南通·开学考试
5 . 烟气中SO2和NO的转化和综合利用既有利于节约资源,又有利于保护环境。
(1)采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝,在一定浓度的NaClO2溶液中通入含有SO2和NO的烟气,反应温度为323K。
已知: 4H++ClO =4ClO2+Cl-+2H2O;ClO2氧化性大于NaClO2。
=4ClO2+Cl-+2H2O;ClO2氧化性大于NaClO2。
①写出NaClO2溶液将NO氧化为NO 的离子方程式:
的离子方程式:___________ 。
②已知脱硫反应速率大于脱硝反应速率,原因是除了SO2和NO在烟气中的初始浓度不同,还可能是___________ 。
③当调节溶液初始pH由7升至12时,通入烟气后,NO转化率由100%降为51%,可能的原因是___________ 。
(2)有氧条件下,NO在催化剂作用下可被NH3还原为N2。在钒基催化剂(V2O5)作用下的脱硝反应机理如图1所示。
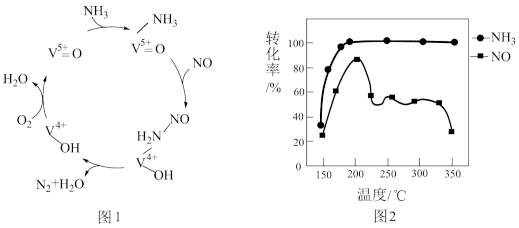
①根据图1机理,NO、NH3在有氧条件下的总化学方程式是___________ 。
②按上述图1中NH3、NO和O2的比例进行催化脱硝反应。相同反应时间,NH3和NO的转化率与温度的关系如图2所示,200℃后,NO转化率急剧下降的原因是___________ 。
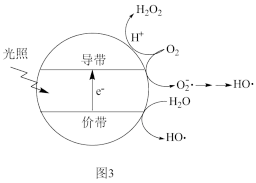
(3)羟基自由基(HO·)也可以用于脱硫脱硝。图3表示光催化氧化技术可生成HO·:光照时,价带失去电子产生有强氧化性的空穴,价带上生成HO·;描述产生HO·的另一种过程:___________ 。
(1)采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝,在一定浓度的NaClO2溶液中通入含有SO2和NO的烟气,反应温度为323K。
已知: 4H++ClO
 =4ClO2+Cl-+2H2O;ClO2氧化性大于NaClO2。
=4ClO2+Cl-+2H2O;ClO2氧化性大于NaClO2。①写出NaClO2溶液将NO氧化为NO
 的离子方程式:
的离子方程式:②已知脱硫反应速率大于脱硝反应速率,原因是除了SO2和NO在烟气中的初始浓度不同,还可能是
③当调节溶液初始pH由7升至12时,通入烟气后,NO转化率由100%降为51%,可能的原因是
(2)有氧条件下,NO在催化剂作用下可被NH3还原为N2。在钒基催化剂(V2O5)作用下的脱硝反应机理如图1所示。

①根据图1机理,NO、NH3在有氧条件下的总化学方程式是
②按上述图1中NH3、NO和O2的比例进行催化脱硝反应。相同反应时间,NH3和NO的转化率与温度的关系如图2所示,200℃后,NO转化率急剧下降的原因是
(3)羟基自由基(HO·)也可以用于脱硫脱硝。图3表示光催化氧化技术可生成HO·:光照时,价带失去电子产生有强氧化性的空穴,价带上生成HO·;描述产生HO·的另一种过程:

您最近一年使用:0次
2021-09-12更新
|
527次组卷
|
4卷引用:常见无机物的性质
(已下线)常见无机物的性质江苏省海安市2021-2022学年高三上学期期初学业质量监测化学试题江苏省宿迁青华中学2021-2022学年高三上学期9月月考化学试题(已下线)第12讲 化学反应的调控-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)
2021·江苏南通·模拟预测
名校
6 . 铬铁矿主要成分为铬尖晶石(FeCr2O4),以铬铁矿为原料可制备Cr2(SO4)3溶液。铬铁矿的尖晶石结构在通常条件下难以被破坏,其中的二价铁被氧化后,会促进尖晶石结构分解,有利于其参与化学反应。
(1)铬铁矿中的基态二价铁被氧化过程中,失去的电子所处的能级为_______ 。
(2)120℃时,向铬铁矿矿粉中加入50%的H2SO4,不断搅拌,铬铁矿溶解速率很慢。向溶液中加入一定量的CrO3,矿粉溶解速率明显加快,得到含较多Cr3+和Fe3+的溶液。写出加入CrO3后促进尖晶石溶解的离子方程式:_______ 。
(3)其它条件不变,测得不同温度下Cr3+的浸出率随酸浸时间的变化如图1所示。实际酸浸过程中选择120℃的原因是_______ 。

(4)已知:室温下Ksp[Cr(OH)3]=8×10-31,Ksp [Fe(OH)3]=3×10-39,可通过调节溶液的pH,除去酸浸后混合液中的Fe3+。实验测得除铁率和铬损失率随混合液pH的变化如图2所示。pH=3时铬损失率高达38%的原因是_______ 。

(5)在酸浸后的混合液中加入有机萃取剂,萃取后,Fe2(SO4)3进入有机层,Cr2(SO4)3进入水层。取10.00mL水层溶液于锥形瓶中,先加入氢氧化钠调节溶液至碱性,再加入足量过氧化氢溶液。充分反应后,加热煮沸除去过量过氧化氢。待溶液冷却至室温,加入硫酸和磷酸的混合酸酸化,此时溶液中Cr全部为+6价。在酸化后的溶液中加入足量KI溶液,以淀粉溶液作指示剂,用0.3000mol·L-1Na2S2O3溶液滴定,发生反应:I2+2S2O =S4O
=S4O +2I-,滴定至终点时消耗Na2S2O3溶液19.80mL,计算萃取所得水层溶液中Cr3+的物质的量浓度
+2I-,滴定至终点时消耗Na2S2O3溶液19.80mL,计算萃取所得水层溶液中Cr3+的物质的量浓度_______ 。(写出计算过程)
(1)铬铁矿中的基态二价铁被氧化过程中,失去的电子所处的能级为
(2)120℃时,向铬铁矿矿粉中加入50%的H2SO4,不断搅拌,铬铁矿溶解速率很慢。向溶液中加入一定量的CrO3,矿粉溶解速率明显加快,得到含较多Cr3+和Fe3+的溶液。写出加入CrO3后促进尖晶石溶解的离子方程式:
(3)其它条件不变,测得不同温度下Cr3+的浸出率随酸浸时间的变化如图1所示。实际酸浸过程中选择120℃的原因是

(4)已知:室温下Ksp[Cr(OH)3]=8×10-31,Ksp [Fe(OH)3]=3×10-39,可通过调节溶液的pH,除去酸浸后混合液中的Fe3+。实验测得除铁率和铬损失率随混合液pH的变化如图2所示。pH=3时铬损失率高达38%的原因是

(5)在酸浸后的混合液中加入有机萃取剂,萃取后,Fe2(SO4)3进入有机层,Cr2(SO4)3进入水层。取10.00mL水层溶液于锥形瓶中,先加入氢氧化钠调节溶液至碱性,再加入足量过氧化氢溶液。充分反应后,加热煮沸除去过量过氧化氢。待溶液冷却至室温,加入硫酸和磷酸的混合酸酸化,此时溶液中Cr全部为+6价。在酸化后的溶液中加入足量KI溶液,以淀粉溶液作指示剂,用0.3000mol·L-1Na2S2O3溶液滴定,发生反应:I2+2S2O
 =S4O
=S4O +2I-,滴定至终点时消耗Na2S2O3溶液19.80mL,计算萃取所得水层溶液中Cr3+的物质的量浓度
+2I-,滴定至终点时消耗Na2S2O3溶液19.80mL,计算萃取所得水层溶液中Cr3+的物质的量浓度
您最近一年使用:0次
2021·江苏徐州·模拟预测
名校
7 . 金常以微细粒浸染于黄铁矿、含砷黄铁矿中,此类矿石的预氧化处理方法主要有:焙烧氧化、生物氧化和湿法氧化。
(1)含砷黄铁矿(主要成分为FeAsS)高温焙烧氧化后,再用氰化钠(NaCN)溶液浸出。已知:氢氰酸(HCN)易挥发,有剧毒。
①焙烧氧化的产物有As4O6、Fe3O4,该反应的化学方程式为_______ 。
②焙烧氧化的缺点为_______ 。
③采用电解法除去反应剩余液中有毒物质,CN-在阳极区被去除。在pH=10时,CN-去除效果最佳且能耗最低,原因是____ 。
(2)利用细菌进行生物氧化提取金,pH对金的浸出率影响如图-1,pH影响金浸出率的原因是_____ 。

(3)湿法氧化是在溶液中化学物质的作用下提取金。已知Au的硫酸盐难溶于水,Au+与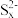 、
、 等形成配合物。
等形成配合物。
①工业上利用硫代硫酸盐可浸出金生成Au(S2O3) ,但在富氧条件下浸出率明显降低,原因是
,但在富氧条件下浸出率明显降低,原因是___ 。
②常温下,已知H2S-HS--S2-粒子体系随pH变化各组分分布如图-2,δ(H2S)= 。多硫化物浸金的一种原理是:混合体系在通空气条件下氧化时,体系中S2-先被氧化为S,再转化为
。多硫化物浸金的一种原理是:混合体系在通空气条件下氧化时,体系中S2-先被氧化为S,再转化为 。研究发现
。研究发现 可将Au氧化为AuS-,pH=11时
可将Au氧化为AuS-,pH=11时 将Au氧化的离子方程式为
将Au氧化的离子方程式为_______ 。
(1)含砷黄铁矿(主要成分为FeAsS)高温焙烧氧化后,再用氰化钠(NaCN)溶液浸出。已知:氢氰酸(HCN)易挥发,有剧毒。
①焙烧氧化的产物有As4O6、Fe3O4,该反应的化学方程式为
②焙烧氧化的缺点为
③采用电解法除去反应剩余液中有毒物质,CN-在阳极区被去除。在pH=10时,CN-去除效果最佳且能耗最低,原因是
(2)利用细菌进行生物氧化提取金,pH对金的浸出率影响如图-1,pH影响金浸出率的原因是

(3)湿法氧化是在溶液中化学物质的作用下提取金。已知Au的硫酸盐难溶于水,Au+与
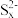 、
、 等形成配合物。
等形成配合物。①工业上利用硫代硫酸盐可浸出金生成Au(S2O3)
 ,但在富氧条件下浸出率明显降低,原因是
,但在富氧条件下浸出率明显降低,原因是②常温下,已知H2S-HS--S2-粒子体系随pH变化各组分分布如图-2,δ(H2S)=
 。多硫化物浸金的一种原理是:混合体系在通空气条件下氧化时,体系中S2-先被氧化为S,再转化为
。多硫化物浸金的一种原理是:混合体系在通空气条件下氧化时,体系中S2-先被氧化为S,再转化为 。研究发现
。研究发现 可将Au氧化为AuS-,pH=11时
可将Au氧化为AuS-,pH=11时 将Au氧化的离子方程式为
将Au氧化的离子方程式为
您最近一年使用:0次
2021-05-25更新
|
570次组卷
|
5卷引用:溶液中的离子平衡
(已下线)溶液中的离子平衡江苏省徐州市2021届高三年级5月考前模拟化学试题(已下线)【镇江新东方】镇江中学高三年级第三次适应性考试江苏省扬州中学2021-2022学年高三上学期10月考化学试题(已下线)2020年江苏卷化学高考真题变式题16-21
2021·江苏·二模
名校
8 .  可通过
可通过 与
与 在碱性溶液中反应制备。
在碱性溶液中反应制备。 和
和 均可用于氧化去除高氯(含高浓度
均可用于氧化去除高氯(含高浓度 )废水中的有机物。
)废水中的有机物。
(1)用 处理高氯废水中的有机物时,需在一定条件下使用。
处理高氯废水中的有机物时,需在一定条件下使用。
① 时,
时,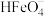 分解放出
分解放出 并产生
并产生 沉淀,该反应的离子方程式为
沉淀,该反应的离子方程式为_______ 。
②酸性溶液中 的氧化性大于
的氧化性大于 的氧化性。
的氧化性。 处理高氯废水中的有机物需在碱性条件下进行,其原因是
处理高氯废水中的有机物需在碱性条件下进行,其原因是_______ 。
(2)用 处理高氯废水中的有机物时,研究了“
处理高氯废水中的有机物时,研究了“ ”和“
”和“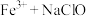 ”两种体系对高氯废水中有机物的氧化率(废水中被氧化有机物的量占废水中有机物总量的百分率)。
”两种体系对高氯废水中有机物的氧化率(废水中被氧化有机物的量占废水中有机物总量的百分率)。
①当废水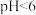 时,仅使用
时,仅使用 处理高氯废水,有机物的氧化率较低,其原因是
处理高氯废水,有机物的氧化率较低,其原因是_______ 。
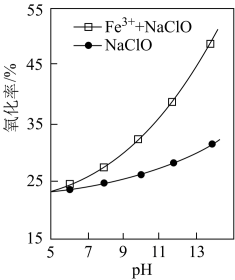
②当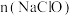 相同时,使用“
相同时,使用“ ”与“
”与“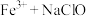 ”处理高氯废水,废水中有机物的氧化率随废水
”处理高氯废水,废水中有机物的氧化率随废水 的变化如题图所示。与“
的变化如题图所示。与“ ”体系相比,“
”体系相比,“ ”体系中有机物氧化率随着废水
”体系中有机物氧化率随着废水 升高显著增大的可能原因是
升高显著增大的可能原因是_______ 。
 可通过
可通过 与
与 在碱性溶液中反应制备。
在碱性溶液中反应制备。 和
和 均可用于氧化去除高氯(含高浓度
均可用于氧化去除高氯(含高浓度 )废水中的有机物。
)废水中的有机物。(1)用
 处理高氯废水中的有机物时,需在一定条件下使用。
处理高氯废水中的有机物时,需在一定条件下使用。①
 时,
时, 分解放出
分解放出 并产生
并产生 沉淀,该反应的离子方程式为
沉淀,该反应的离子方程式为②酸性溶液中
 的氧化性大于
的氧化性大于 的氧化性。
的氧化性。 处理高氯废水中的有机物需在碱性条件下进行,其原因是
处理高氯废水中的有机物需在碱性条件下进行,其原因是(2)用
 处理高氯废水中的有机物时,研究了“
处理高氯废水中的有机物时,研究了“ ”和“
”和“ ”两种体系对高氯废水中有机物的氧化率(废水中被氧化有机物的量占废水中有机物总量的百分率)。
”两种体系对高氯废水中有机物的氧化率(废水中被氧化有机物的量占废水中有机物总量的百分率)。①当废水
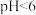 时,仅使用
时,仅使用 处理高氯废水,有机物的氧化率较低,其原因是
处理高氯废水,有机物的氧化率较低,其原因是②当
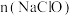 相同时,使用“
相同时,使用“ ”与“
”与“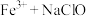 ”处理高氯废水,废水中有机物的氧化率随废水
”处理高氯废水,废水中有机物的氧化率随废水 的变化如题图所示。与“
的变化如题图所示。与“ ”体系相比,“
”体系相比,“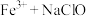 ”体系中有机物氧化率随着废水
”体系中有机物氧化率随着废水 升高显著增大的可能原因是
升高显著增大的可能原因是
您最近一年使用:0次
2021-04-19更新
|
648次组卷
|
3卷引用:常见无机物的性质
2020·江苏·高考真题
9 . 次氯酸钠溶液和二氯异氰尿酸钠(C3N3O3Cl2Na)都是常用的杀菌消毒剂。 NaClO可用于制备二氯异氰尿酸钠.
(1)NaClO溶液可由低温下将Cl2缓慢通入NaOH溶液中而制得。制备 NaClO的离子方程式为__________ ;用于环境杀菌消毒的NaClO溶液须稀释并及时使用,若在空气中暴露时间过长且见光,将会导致消毒作用减弱,其原因是__________________ 。
(2)二氯异氰尿酸钠优质品要求有效氯大于60%。通过下列实验检测二氯异氰尿酸钠样品是否达到优质品标准。实验检测原理为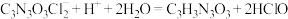


准确称取1.1200g样品,用容量瓶配成250.0mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;用 Na2S2O3标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液20.00mL。
Na2S2O3标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液20.00mL。
①通过计算判断该样品是否为优质品_______ 。(写出计算过程,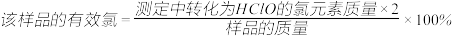 )
)
②若在检测中加入稀硫酸的量过少,将导致样品的有效氯测定值____________ (填“偏高”或“偏低”)。
(1)NaClO溶液可由低温下将Cl2缓慢通入NaOH溶液中而制得。制备 NaClO的离子方程式为
(2)二氯异氰尿酸钠优质品要求有效氯大于60%。通过下列实验检测二氯异氰尿酸钠样品是否达到优质品标准。实验检测原理为
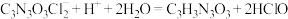


准确称取1.1200g样品,用容量瓶配成250.0mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;用
 Na2S2O3标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液20.00mL。
Na2S2O3标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液20.00mL。①通过计算判断该样品是否为优质品
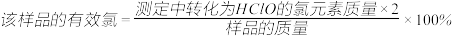 )
)②若在检测中加入稀硫酸的量过少,将导致样品的有效氯测定值
您最近一年使用:0次
2020-07-11更新
|
5023次组卷
|
16卷引用:实验综合题
(已下线)实验综合题2020年江苏卷化学高考试题(已下线)专题13 元素及其化合物知识的综合应用-2020年高考真题和模拟题化学分项汇编江苏省苏州中学2020-2021学年高一下学期期初化学试卷(已下线)专题08 常见无机物及其应用——备战2021年高考化学纠错笔记(已下线)小题25 定量实验 ——备战2021年高考化学经典小题考前必刷(全国通用)(已下线)考点31 物质的制备 定量分析-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点33 物质的定性与定量分析-备战2022年高考化学一轮复习考点帮(浙江专用)江苏省徐州市王杰中学2021-2022学年高三10月学情调研化学试题(已下线)解密02 物质的量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)2020年江苏卷化学高考真题变式题16-21(已下线)解密02 物质的量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)考点05 氧化还原反应-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点52 定量分析-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第22讲 水的电离与溶液的pH(讲)-2023年高考化学一轮复习讲练测(新教材新高考)甘肃省天水市一中2022届高三上学期8月第一次考试化学试题
2020·江苏扬州·三模
10 . 聚合氯化铁[Fe2(OH)nCl6-n]m简称PFC,是一种新型高效的无机高分子净水剂。以FeCl2·4H2O为原料,溶于稀盐酸并加入少量的NaNO2,经氧化、水解、聚合等步骤,可制备PFC。
(1)在稀盐酸中,NaNO2会与Fe2+反应生成一种无色气体M,气体M对该反应有催化作用,其催化原理如图所示。 M的化学式为______ ; Fe2+在酸性条件下被O2氧化的离子方程式为_______ 。

(2)盐基度[B= × 100%]是衡量净水剂优劣的一个重要指标。盐基度越小,净水剂对水pH变化的影响
× 100%]是衡量净水剂优劣的一个重要指标。盐基度越小,净水剂对水pH变化的影响______ 。(填“越大”、“越小”或“无影响”)
(3)PFC样品中盐基度(B)的测定:
已知:PFC样品的密度ρ = 1.40 g·mL−1,样品中铁的质量分数ω(Fe) = 16%
步骤1:准确量取1.00 mL PFC样品置于锥形瓶中。
步骤2:加入一定体积0.05000 mol·L−1的盐酸标准溶液,室温静置后,加入一定体积的氟化钾溶液(与Fe3+反应,消除Fe3+对实验的干扰),滴加数滴酚酞作指示剂,立即用0.05000 mol·L−1氢氧化钠标准溶液滴定至终点,消耗氢氧化钠标准溶液13.00 mL。
步骤3:准确量取1.00 mL蒸馏水样品置于锥形瓶中,重复步骤2操作,消耗氢氧化钠标准溶液49.00 mL。
根据以上实验数据计算PFC样品的盐基度(B)(写出计算过程)_______ 。
(1)在稀盐酸中,NaNO2会与Fe2+反应生成一种无色气体M,气体M对该反应有催化作用,其催化原理如图所示。 M的化学式为

(2)盐基度[B=
 × 100%]是衡量净水剂优劣的一个重要指标。盐基度越小,净水剂对水pH变化的影响
× 100%]是衡量净水剂优劣的一个重要指标。盐基度越小,净水剂对水pH变化的影响(3)PFC样品中盐基度(B)的测定:
已知:PFC样品的密度ρ = 1.40 g·mL−1,样品中铁的质量分数ω(Fe) = 16%
步骤1:准确量取1.00 mL PFC样品置于锥形瓶中。
步骤2:加入一定体积0.05000 mol·L−1的盐酸标准溶液,室温静置后,加入一定体积的氟化钾溶液(与Fe3+反应,消除Fe3+对实验的干扰),滴加数滴酚酞作指示剂,立即用0.05000 mol·L−1氢氧化钠标准溶液滴定至终点,消耗氢氧化钠标准溶液13.00 mL。
步骤3:准确量取1.00 mL蒸馏水样品置于锥形瓶中,重复步骤2操作,消耗氢氧化钠标准溶液49.00 mL。
根据以上实验数据计算PFC样品的盐基度(B)(写出计算过程)
您最近一年使用:0次



