烟气中SO2和NO的转化和综合利用既有利于节约资源,又有利于保护环境。
(1)采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝,在一定浓度的NaClO2溶液中通入含有SO2和NO的烟气,反应温度为323K。
已知: 4H++ClO =4ClO2+Cl-+2H2O;ClO2氧化性大于NaClO2。
=4ClO2+Cl-+2H2O;ClO2氧化性大于NaClO2。
①写出NaClO2溶液将NO氧化为NO 的离子方程式:
的离子方程式:___________ 。
②已知脱硫反应速率大于脱硝反应速率,原因是除了SO2和NO在烟气中的初始浓度不同,还可能是___________ 。
③当调节溶液初始pH由7升至12时,通入烟气后,NO转化率由100%降为51%,可能的原因是___________ 。
(2)有氧条件下,NO在催化剂作用下可被NH3还原为N2。在钒基催化剂(V2O5)作用下的脱硝反应机理如图1所示。
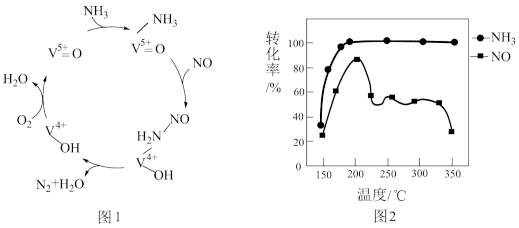
①根据图1机理,NO、NH3在有氧条件下的总化学方程式是___________ 。
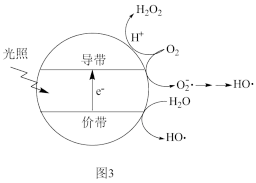
②按上述图1中NH3、NO和O2的比例进行催化脱硝反应。相同反应时间,NH3和NO的转化率与温度的关系如图2所示,200℃后,NO转化率急剧下降的原因是___________ 。
(3)羟基自由基(HO·)也可以用于脱硫脱硝。图3表示光催化氧化技术可生成HO·:光照时,价带失去电子产生有强氧化性的空穴,价带上生成HO·;描述产生HO·的另一种过程:___________ 。
(1)采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝,在一定浓度的NaClO2溶液中通入含有SO2和NO的烟气,反应温度为323K。
已知: 4H++ClO
 =4ClO2+Cl-+2H2O;ClO2氧化性大于NaClO2。
=4ClO2+Cl-+2H2O;ClO2氧化性大于NaClO2。①写出NaClO2溶液将NO氧化为NO
 的离子方程式:
的离子方程式:②已知脱硫反应速率大于脱硝反应速率,原因是除了SO2和NO在烟气中的初始浓度不同,还可能是
③当调节溶液初始pH由7升至12时,通入烟气后,NO转化率由100%降为51%,可能的原因是
(2)有氧条件下,NO在催化剂作用下可被NH3还原为N2。在钒基催化剂(V2O5)作用下的脱硝反应机理如图1所示。

①根据图1机理,NO、NH3在有氧条件下的总化学方程式是
②按上述图1中NH3、NO和O2的比例进行催化脱硝反应。相同反应时间,NH3和NO的转化率与温度的关系如图2所示,200℃后,NO转化率急剧下降的原因是
(3)羟基自由基(HO·)也可以用于脱硫脱硝。图3表示光催化氧化技术可生成HO·:光照时,价带失去电子产生有强氧化性的空穴,价带上生成HO·;描述产生HO·的另一种过程:

21-22高三上·江苏南通·开学考试 查看更多[4]
(已下线)常见无机物的性质(已下线)第12讲 化学反应的调控-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)江苏省宿迁青华中学2021-2022学年高三上学期9月月考化学试题江苏省海安市2021-2022学年高三上学期期初学业质量监测化学试题
更新时间:2021-09-12 15:47:52
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】氯酸钾和浓盐酸之间有下列反应:2KClO3+4HCl(浓)=2KCl+Cl2↑+2ClO2+2H2O
(1)该反应中发生还原反应的物质是___________ 。氧化产物是___________ 。
(2)用双线桥标出方程式中的电子得失。2KClO3+4HCl(浓)=2KCl+Cl2↑+2ClO2+2H2O,___________
(3)当有0.2mol电子发生转移时,生成的氯气的体积为___________ L(标准状况)。被氧化的HCl的物质的量为___________ mol。
(4)若分别用①KMnO4(还原产物是Mn2+);②MnO2(还原产物是Mn2+);③Ca(ClO)2(还原产物是Cl2)氧化浓盐酸制备氯气,当浓盐酸足量且这三种氧化剂的物质的量相同时,生成氯气的物质的量最少的是___________ (填编号)。
(5)有下列6种物质:K2SO4、K2SO3、I2、H2SO4、KIO3、H2O组成一个氧化还原反应,已知在反应中K2SO3失去电子。请回答下列问题:将这6种物质分别填入下面对应的横线上,组成一个配平 的化学方程式:___________+___________+H2SO4→___________+___________+___________(填化学式),___________
(1)该反应中发生还原反应的物质是
(2)用双线桥标出方程式中的电子得失。2KClO3+4HCl(浓)=2KCl+Cl2↑+2ClO2+2H2O,
(3)当有0.2mol电子发生转移时,生成的氯气的体积为
(4)若分别用①KMnO4(还原产物是Mn2+);②MnO2(还原产物是Mn2+);③Ca(ClO)2(还原产物是Cl2)氧化浓盐酸制备氯气,当浓盐酸足量且这三种氧化剂的物质的量相同时,生成氯气的物质的量最少的是
(5)有下列6种物质:K2SO4、K2SO3、I2、H2SO4、KIO3、H2O组成一个氧化还原反应,已知在反应中K2SO3失去电子。请回答下列问题:将这6种物质分别填入下面对应的横线上,组成一个
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】当用CaSO3水悬浮液吸收经O3预处理的烟气时,清液(pH约为8)中SO 将NO2转化为NO
将NO2转化为NO ,其离子方程式:
,其离子方程式:___________ 。
 将NO2转化为NO
将NO2转化为NO ,其离子方程式:
,其离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】除去烟气中的NO,能促进生态文明建设。
(1)含 和
和 的酸性吸收液可以处理烟气中NO,原理是:
的酸性吸收液可以处理烟气中NO,原理是: 催化
催化 产生
产生 ,后者将NO最终氧化成
,后者将NO最终氧化成 。
。
①写出 将NO氧化成
将NO氧化成 的离子方程式为:
的离子方程式为:_______ 。
②吸收液的初始pH和温度对 氧化NO的效果分别如图1和图2所示。
氧化NO的效果分别如图1和图2所示。

当吸收液的初始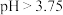 时,NO氧化率明显降低,原因可能是:
时,NO氧化率明显降低,原因可能是:
(i)pH较大时, 容易发生歧化反应,导致
容易发生歧化反应,导致 浓度降低,氧化能力减弱:
浓度降低,氧化能力减弱:
(ii)_______ 。
③当超过60℃时,NO的氧化率明显降低,原因可能是:_______ 。
(2) 可在
可在 催化下还原烟气中NO,温度对该反应的影响如图3所示。
催化下还原烟气中NO,温度对该反应的影响如图3所示。
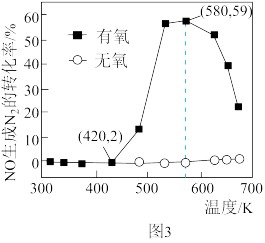
①在420~580K之间,有氧条件下NO生成 的转化率明显高于无氧条件,原因可能是
的转化率明显高于无氧条件,原因可能是_______ 。
②进一步研究发现,以 为催化利时,
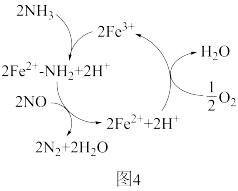
为催化利时, 在有氧条件下还原NO的机理如图4所示。该反应的总化学方程式为:
在有氧条件下还原NO的机理如图4所示。该反应的总化学方程式为:_______ 。
(1)含
 和
和 的酸性吸收液可以处理烟气中NO,原理是:
的酸性吸收液可以处理烟气中NO,原理是: 催化
催化 产生
产生 ,后者将NO最终氧化成
,后者将NO最终氧化成 。
。①写出
 将NO氧化成
将NO氧化成 的离子方程式为:
的离子方程式为:②吸收液的初始pH和温度对
 氧化NO的效果分别如图1和图2所示。
氧化NO的效果分别如图1和图2所示。
当吸收液的初始
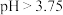 时,NO氧化率明显降低,原因可能是:
时,NO氧化率明显降低,原因可能是:(i)pH较大时,
 容易发生歧化反应,导致
容易发生歧化反应,导致 浓度降低,氧化能力减弱:
浓度降低,氧化能力减弱:(ii)
③当超过60℃时,NO的氧化率明显降低,原因可能是:
(2)
 可在
可在 催化下还原烟气中NO,温度对该反应的影响如图3所示。
催化下还原烟气中NO,温度对该反应的影响如图3所示。
①在420~580K之间,有氧条件下NO生成
 的转化率明显高于无氧条件,原因可能是
的转化率明显高于无氧条件,原因可能是②进一步研究发现,以
 为催化利时,
为催化利时, 在有氧条件下还原NO的机理如图4所示。该反应的总化学方程式为:
在有氧条件下还原NO的机理如图4所示。该反应的总化学方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】NH3的催化氧化是工业制取硝酸的关键步骤之一,该反应的化学方程式为:4NH3(g)+5O2(g)  4NO(g)+6H2O(g),△H<0。
4NO(g)+6H2O(g),△H<0。
请回答下列问题:
(1)在恒温恒容下判断该反应达到平衡状态的标志是______ (填字母)。
a.NH3和NO浓度相等 b.NO百分含量保持不变
c.容器中气体的压强不变 d.NH3的生成速率与NO的消耗速率相等
(2)当该反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高NH3平衡转化率的是_____________ 。(填字母)
a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.降低温度
(3)将0.050 mol NH3 (g)和0.060 mol O2(g)放入容积为1L的密闭容器中,在一定条件下达到平衡,测得c(NO)=0.040 mol/L。计算该条件下反应的NH3的转化率。平衡时,NH3的转化率α(NH3 )=_________ 。
 4NO(g)+6H2O(g),△H<0。
4NO(g)+6H2O(g),△H<0。请回答下列问题:
(1)在恒温恒容下判断该反应达到平衡状态的标志是
a.NH3和NO浓度相等 b.NO百分含量保持不变
c.容器中气体的压强不变 d.NH3的生成速率与NO的消耗速率相等
(2)当该反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高NH3平衡转化率的是
a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.降低温度
(3)将0.050 mol NH3 (g)和0.060 mol O2(g)放入容积为1L的密闭容器中,在一定条件下达到平衡,测得c(NO)=0.040 mol/L。计算该条件下反应的NH3的转化率。平衡时,NH3的转化率α(NH3 )=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】中国环境监测总站数据显示,颗粒物 等
等 为连续雾霾过程影响空气质量最显著的污染物,其主要来源为燃煤、机动车尾气等。因此,对
为连续雾霾过程影响空气质量最显著的污染物,其主要来源为燃煤、机动车尾气等。因此,对 、
、 、
、 等进行研究具有重要意义。请回答下列问题:
等进行研究具有重要意义。请回答下列问题:
(1)将 样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据计算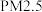 待测试样的pH =
待测试样的pH =___________ 。
(2)汽车发动机工作时会引发 和
和 反应,当尾气中空气不足时,
反应,当尾气中空气不足时, 在催化转化器中被还原成
在催化转化器中被还原成 排出。写出NO被CO还原的化学方程式
排出。写出NO被CO还原的化学方程式________ 。
(3)碘循环工艺不仅能吸收 降低环境污染,同时又能制得氢气,具体流程如下:
降低环境污染,同时又能制得氢气,具体流程如下:
①用离子方程式表示反应器中发生的反应_______ 。
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出 的目的是
的目的是_______ 。
(4)下图是用 脱除烟气中NO的原理。
脱除烟气中NO的原理。
①该脱硝原理中,NO最终转化为________  填化学式
填化学式 和H2O。
和H2O。
②当消耗 和
和 时,除去的NO在标准状况下的体积为
时,除去的NO在标准状况下的体积为____ L。
 等
等 为连续雾霾过程影响空气质量最显著的污染物,其主要来源为燃煤、机动车尾气等。因此,对
为连续雾霾过程影响空气质量最显著的污染物,其主要来源为燃煤、机动车尾气等。因此,对 、
、 、
、 等进行研究具有重要意义。请回答下列问题:
等进行研究具有重要意义。请回答下列问题: (1)将
 样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表: | 离子 |  |  |  |  | 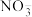 |  |
浓度 | 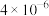 | 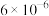 | 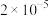 | 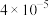 | 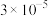 | 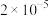 |
根据表中数据计算
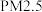 待测试样的pH =
待测试样的pH =(2)汽车发动机工作时会引发
 和
和 反应,当尾气中空气不足时,
反应,当尾气中空气不足时, 在催化转化器中被还原成
在催化转化器中被还原成 排出。写出NO被CO还原的化学方程式
排出。写出NO被CO还原的化学方程式(3)碘循环工艺不仅能吸收
 降低环境污染,同时又能制得氢气,具体流程如下:
降低环境污染,同时又能制得氢气,具体流程如下: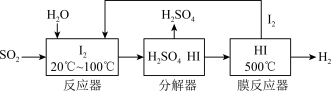
①用离子方程式表示反应器中发生的反应
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出
 的目的是
的目的是(4)下图是用
 脱除烟气中NO的原理。
脱除烟气中NO的原理。
①该脱硝原理中,NO最终转化为
 填化学式
填化学式 和H2O。
和H2O。②当消耗
 和
和 时,除去的NO在标准状况下的体积为
时,除去的NO在标准状况下的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】工业上采用高温分解H2S制取氢气,其反应为2H2S(g) 2H2(g)+S2(g),在膜反应器中分离出H2。
2H2(g)+S2(g),在膜反应器中分离出H2。
(1)在密闭容器中,充入0.10molH2S(g),发生反应2H2S(g) 2H2(g)+S2(g),控制不同的温度和压强进行实验,结果如图。
2H2(g)+S2(g),控制不同的温度和压强进行实验,结果如图。

图中压强p1、p2、p3由大到小的顺序为___ 。
(2)若容器的容积为2.0L,则压强为p3,温度为950℃时,反应经3h达到平衡,化学反应速率v(S2)=___ 。
(3)若压强p2=7.2MPa、温度为975℃时,该反应的平衡常数Kp=__ (用平衡分压代替平衡浓度,分压=总压×物质的量分数,结果保留两位有效数字)。
 2H2(g)+S2(g),在膜反应器中分离出H2。
2H2(g)+S2(g),在膜反应器中分离出H2。(1)在密闭容器中,充入0.10molH2S(g),发生反应2H2S(g)
 2H2(g)+S2(g),控制不同的温度和压强进行实验,结果如图。
2H2(g)+S2(g),控制不同的温度和压强进行实验,结果如图。
图中压强p1、p2、p3由大到小的顺序为
(2)若容器的容积为2.0L,则压强为p3,温度为950℃时,反应经3h达到平衡,化学反应速率v(S2)=
(3)若压强p2=7.2MPa、温度为975℃时,该反应的平衡常数Kp=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】环戊二烯(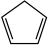 )是重要的有机化工原料,可通过反应
)是重要的有机化工原料,可通过反应 (g)+I2(g)
(g)+I2(g)
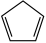 (g)+2HI(g)制得。回答下列问题。
(g)+2HI(g)制得。回答下列问题。
(1)某温度下,在固定容积的密闭容器中发生该反应,该反应达到平衡的标志是_______。
(2)1mol碘和1mol环戊烯(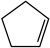 )在10L恒容容器内发生反应。
)在10L恒容容器内发生反应。
①不同温度下环戊烯的物质的量与反应时间的关系如图所示。
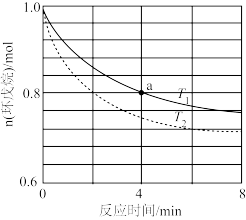
计算a点时,0-4分钟内HI的生成速率v=_______ mol·L-1·min-1。根据上图可得出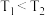 的理由是
的理由是_______ 。
②某温度下,若起始压强为 ,平衡时总压强增加了15%,环戊烯的转化率为
,平衡时总压强增加了15%,环戊烯的转化率为_______ ,该反应的平衡常数
_______ (列出计算表达式)。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
③欲增加环戊烯的平衡转化率,但K值不变,可采取的措施有_______ (填标号)。
A.通入惰性气体 B.增加碘浓度 C.增加环戊烯浓度 D.提高温度
 )是重要的有机化工原料,可通过反应
)是重要的有机化工原料,可通过反应 (g)+I2(g)
(g)+I2(g)
 (g)+2HI(g)制得。回答下列问题。
(g)+2HI(g)制得。回答下列问题。(1)某温度下,在固定容积的密闭容器中发生该反应,该反应达到平衡的标志是_______。
| A.容器内总压不变 | B.容器内气体颜色不变 |
| C.容器内气体密度不变 | D.生成1molC=C双键的同时生成2molH-I键 |
 )在10L恒容容器内发生反应。
)在10L恒容容器内发生反应。①不同温度下环戊烯的物质的量与反应时间的关系如图所示。

计算a点时,0-4分钟内HI的生成速率v=
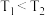 的理由是
的理由是②某温度下,若起始压强为
 ,平衡时总压强增加了15%,环戊烯的转化率为
,平衡时总压强增加了15%,环戊烯的转化率为
③欲增加环戊烯的平衡转化率,但K值不变,可采取的措施有
A.通入惰性气体 B.增加碘浓度 C.增加环戊烯浓度 D.提高温度
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】汽车使用乙醇汽油并不能减少 的排放,某研究小组在实验室以耐高温试剂
的排放,某研究小组在实验室以耐高温试剂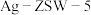 催化,测得
催化,测得 转化为
转化为 的转化率随温度变化情况如下图所示。
的转化率随温度变化情况如下图所示。
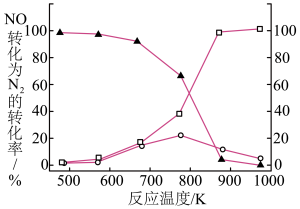
○无 时
时 直接分解为
直接分解为 的产率
的产率
▲ 剩余的百分率
剩余的百分率
□ 条件下,
条件下, 还原为
还原为 转化率
转化率
(1)在 条件下,最佳温度应控制在
条件下,最佳温度应控制在_______ 左右。
(2)若不使用 ,温度超过
,温度超过 ,发现
,发现 的分解率降低,其可能的原因为
的分解率降低,其可能的原因为_______ 。
(3)用平衡移动原理解释为什么加入 后
后 转化为
转化为 的转化率增大:
的转化率增大:_______ 。
 的排放,某研究小组在实验室以耐高温试剂
的排放,某研究小组在实验室以耐高温试剂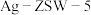 催化,测得
催化,测得 转化为
转化为 的转化率随温度变化情况如下图所示。
的转化率随温度变化情况如下图所示。
○无
 时
时 直接分解为
直接分解为 的产率
的产率▲
 剩余的百分率
剩余的百分率□
 条件下,
条件下, 还原为
还原为 转化率
转化率(1)在
 条件下,最佳温度应控制在
条件下,最佳温度应控制在(2)若不使用
 ,温度超过
,温度超过 ,发现
,发现 的分解率降低,其可能的原因为
的分解率降低,其可能的原因为(3)用平衡移动原理解释为什么加入
 后
后 转化为
转化为 的转化率增大:
的转化率增大:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】工业合成氨反应具有非常重要的意义。
(1)对可逆反应N2(g)+3H2(g) 2NH3(g) ΔH<0,若起始投料n(N2)∶n(H2)=1∶1,达到平衡后,降低温度,N2的体积分数
2NH3(g) ΔH<0,若起始投料n(N2)∶n(H2)=1∶1,达到平衡后,降低温度,N2的体积分数_____ 。
A.增大 B.减小 C.不变 D.不能判断
(2)T ℃,以CO2和NH3为原料可合成化肥尿素:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(l);在2 L的密闭容器中,通入1.2 mol NH3和0.6 mol CO2,2 min时反应刚好达到平衡,此时c(NH3)=0.2 mol·L-1,c(CO2)=0.1 mol·L-1。
CO(NH2)2(s)+H2O(l);在2 L的密闭容器中,通入1.2 mol NH3和0.6 mol CO2,2 min时反应刚好达到平衡,此时c(NH3)=0.2 mol·L-1,c(CO2)=0.1 mol·L-1。
①T ℃时该反应的平衡常数K=_____ 。
②若2 min时保持T ℃和平衡时容器的压强不变,再向体积可变的容器中充入0.6 mol NH3,则此时v正____ v逆(填“>”“<”或“=”)。
③若保持T ℃,在2 min时把容器体积瞬间压缩到1 L且保持体积不变,3 min时达到新平衡,请在图中画出2 min到3 min内NH3浓度的变化曲线。_______

(3)NH3催化还原氮氧化物是目前应用广泛的烟气脱硝技术。已知:6NO2(g)+8NH3(g) 7N2(g)+12H2O(l) ΔH,向容积为2 L的恒容密闭容器中,充入NO2和NH3的混合气体0.14 mol充分反应。不同投料比时,NO2的平衡转化率与温度的关系如图中曲线所示[投料比=n(NO2)/n(NH3)]。
7N2(g)+12H2O(l) ΔH,向容积为2 L的恒容密闭容器中,充入NO2和NH3的混合气体0.14 mol充分反应。不同投料比时,NO2的平衡转化率与温度的关系如图中曲线所示[投料比=n(NO2)/n(NH3)]。

①ΔH____ 0(填“>”“<”或“=”),理由是_____ 。
②x_____ 3∶4(填“>”“<”或“=”),理由是_____ 。
③400 K时,该反应的平衡常数表达式为____ 。
④投料比为3∶4时,Q点v逆(NH3)____ P点v逆(NH3)(填“>”“<”或“=”)。
(1)对可逆反应N2(g)+3H2(g)
 2NH3(g) ΔH<0,若起始投料n(N2)∶n(H2)=1∶1,达到平衡后,降低温度,N2的体积分数
2NH3(g) ΔH<0,若起始投料n(N2)∶n(H2)=1∶1,达到平衡后,降低温度,N2的体积分数A.增大 B.减小 C.不变 D.不能判断
(2)T ℃,以CO2和NH3为原料可合成化肥尿素:2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(l);在2 L的密闭容器中,通入1.2 mol NH3和0.6 mol CO2,2 min时反应刚好达到平衡,此时c(NH3)=0.2 mol·L-1,c(CO2)=0.1 mol·L-1。
CO(NH2)2(s)+H2O(l);在2 L的密闭容器中,通入1.2 mol NH3和0.6 mol CO2,2 min时反应刚好达到平衡,此时c(NH3)=0.2 mol·L-1,c(CO2)=0.1 mol·L-1。①T ℃时该反应的平衡常数K=
②若2 min时保持T ℃和平衡时容器的压强不变,再向体积可变的容器中充入0.6 mol NH3,则此时v正
③若保持T ℃,在2 min时把容器体积瞬间压缩到1 L且保持体积不变,3 min时达到新平衡,请在图中画出2 min到3 min内NH3浓度的变化曲线。

(3)NH3催化还原氮氧化物是目前应用广泛的烟气脱硝技术。已知:6NO2(g)+8NH3(g)
 7N2(g)+12H2O(l) ΔH,向容积为2 L的恒容密闭容器中,充入NO2和NH3的混合气体0.14 mol充分反应。不同投料比时,NO2的平衡转化率与温度的关系如图中曲线所示[投料比=n(NO2)/n(NH3)]。
7N2(g)+12H2O(l) ΔH,向容积为2 L的恒容密闭容器中,充入NO2和NH3的混合气体0.14 mol充分反应。不同投料比时,NO2的平衡转化率与温度的关系如图中曲线所示[投料比=n(NO2)/n(NH3)]。 
①ΔH
②x
③400 K时,该反应的平衡常数表达式为
④投料比为3∶4时,Q点v逆(NH3)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】将甲醇转化耦合到丁烯裂解过程中生产丙烯,主要涉及下列反应:
①
②
③
已知:甲醇吸附在催化剂上,可以活化催化剂;甲醇浓度过大也会抑制丁烯在催化剂上的转化。
(1)下图是 及某些副产物的产率与
及某些副产物的产率与 的关系曲线,最佳的
的关系曲线,最佳的 约为
约为_______ 。

(2)下图是某压强下,将 和
和 按一定的物质的量之比投料,反应达到平衡时
按一定的物质的量之比投料,反应达到平衡时 的体积分数随温度的变化曲线。由图可知平衡时
的体积分数随温度的变化曲线。由图可知平衡时 的体积分数随温度的升高呈现先升高后降低的变化,其原因可能是
的体积分数随温度的升高呈现先升高后降低的变化,其原因可能是_______ 。

①

②

③

已知:甲醇吸附在催化剂上,可以活化催化剂;甲醇浓度过大也会抑制丁烯在催化剂上的转化。
(1)下图是
 及某些副产物的产率与
及某些副产物的产率与 的关系曲线,最佳的
的关系曲线,最佳的 约为
约为
(2)下图是某压强下,将
 和
和 按一定的物质的量之比投料,反应达到平衡时
按一定的物质的量之比投料,反应达到平衡时 的体积分数随温度的变化曲线。由图可知平衡时
的体积分数随温度的变化曲线。由图可知平衡时 的体积分数随温度的升高呈现先升高后降低的变化,其原因可能是
的体积分数随温度的升高呈现先升高后降低的变化,其原因可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】煤燃烧排放的烟气含有SO2和NOx,形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝,回答下列问题:
(1)在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323 K,NaClO2溶液浓度为5×10−3mol·L−1。反应一段时间后溶液中离子浓度的分析结果如下表
①写出NaClO2溶液脱硝过程中主要反应的离子方程式____________ 。
②由实验结果可知,脱硫反应速率______ 脱硝反应速率(填“大于”或“小于”)。原因是除了SO2和NO在烟气中的初始浓度不同,还可能是_____________ 。

(2)在不同温度下,NaClO2溶液脱硫、脱硝的反应中,SO2和NO的平衡分压pc如图所示。
①由图分析可知,反应温度升高,脱硫、脱硝反应的平衡常数均_______ (填“增大”“不变”或“减小”)。
②反应ClO2−+2SO32−===2SO42−+Cl−的平衡常数K表达式为________________ 。
(3)如果采用NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果。
①从化学平衡原理分析,Ca(ClO)2相比NaClO具有的优点是______________ 。
②已知下列反应:
SO2(g)+2OH− (aq) =SO32− (aq)+H2O(l) ΔH1
ClO− (aq)+SO32− (aq) =SO42− (aq)+Cl− (aq) ΔH2
CaSO4(s) ===Ca2+(aq)+SO42−(aq) ΔH3
则反应SO2(g)+ Ca2+(aq)+ ClO− (aq) +2OH− (aq) === CaSO4(s) +H2O(l) +Cl− (aq)的ΔH=_______ 。
(1)在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323 K,NaClO2溶液浓度为5×10−3mol·L−1。反应一段时间后溶液中离子浓度的分析结果如下表
| 离子 | SO42− | SO32− | NO3− | NO2− | Cl− |
| c/(mol·L−1) | 8.35×10−4 | 6.87×10−6 | 1.5×10−4 | 1.2×10−5 | 3.4×10−3 |
①写出NaClO2溶液脱硝过程中主要反应的离子方程式
②由实验结果可知,脱硫反应速率

(2)在不同温度下,NaClO2溶液脱硫、脱硝的反应中,SO2和NO的平衡分压pc如图所示。
①由图分析可知,反应温度升高,脱硫、脱硝反应的平衡常数均
②反应ClO2−+2SO32−===2SO42−+Cl−的平衡常数K表达式为
(3)如果采用NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果。
①从化学平衡原理分析,Ca(ClO)2相比NaClO具有的优点是
②已知下列反应:
SO2(g)+2OH− (aq) =SO32− (aq)+H2O(l) ΔH1
ClO− (aq)+SO32− (aq) =SO42− (aq)+Cl− (aq) ΔH2
CaSO4(s) ===Ca2+(aq)+SO42−(aq) ΔH3
则反应SO2(g)+ Ca2+(aq)+ ClO− (aq) +2OH− (aq) === CaSO4(s) +H2O(l) +Cl− (aq)的ΔH=
您最近一年使用:0次

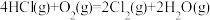 。如图为刚性容器中,进料浓度比
。如图为刚性容器中,进料浓度比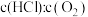 分别等于1∶1、4∶1、7∶1时
分别等于1∶1、4∶1、7∶1时 平衡转化率随温度变化的关系:
平衡转化率随温度变化的关系: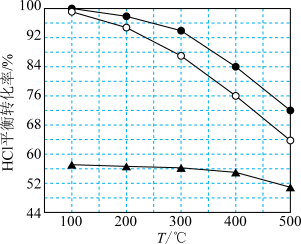
 ,根据进料浓度比
,根据进料浓度比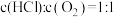 的数据计算K(400℃)=
的数据计算K(400℃)=

