Deacon发明的直接氧化法为: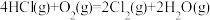 。如图为刚性容器中,进料浓度比
。如图为刚性容器中,进料浓度比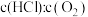 分别等于1∶1、4∶1、7∶1时
分别等于1∶1、4∶1、7∶1时 平衡转化率随温度变化的关系:
平衡转化率随温度变化的关系:
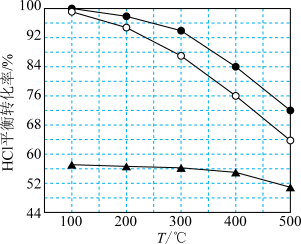
可知反应平衡常数K(300℃)________ K(400℃)(填“大于”或“小于”)。设 初始浓度为
初始浓度为 ,根据进料浓度比
,根据进料浓度比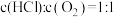 的数据计算K(400℃)=
的数据计算K(400℃)=________ (列出计算式)。按化学计量比进料可以保持反应物高转化率,同时降低产物分离的能耗。进料浓度比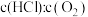 过低、过高的不利影响分别是
过低、过高的不利影响分别是____________ 、_______________ 。
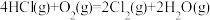 。如图为刚性容器中,进料浓度比
。如图为刚性容器中,进料浓度比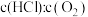 分别等于1∶1、4∶1、7∶1时
分别等于1∶1、4∶1、7∶1时 平衡转化率随温度变化的关系:
平衡转化率随温度变化的关系:
可知反应平衡常数K(300℃)
 初始浓度为
初始浓度为 ,根据进料浓度比
,根据进料浓度比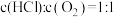 的数据计算K(400℃)=
的数据计算K(400℃)=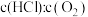 过低、过高的不利影响分别是
过低、过高的不利影响分别是
2020高三·全国·专题练习 查看更多[6]
(已下线)考点23 化学平衡常数-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点19 化学平衡常数 化学反应进行的方向-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点19 化学平衡常数 化学反应进行的方向-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)第二章 化学反应速率与化学平衡(基础过关)-2020-2021学年高二化学单元测试定心卷(人教版2019选择性必修一)鲁科版(2019)选择性必修1 第2章 化学反应的方向、限度与速率 第2节 化学反应的限度(已下线)专题十一 化学反应速率和化学平衡(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训
更新时间:2020-09-20 10:50:05
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】工业合成氨是人类科学技术的一项重大突破。回答下列问题:
(1)合成氨工业中采用循环操作,主要是为了________ (填选项字母)。
(2)在密闭容器中通入amolN2和6molH2,若在一定条件下反应达到平衡状态,容器中剩余cmolN2。
①达到平衡时,H2转化率为________ 。
②若把容器的体积扩大一倍,则正反应速率_______ (填“增大”、“减小”或“不变”,下同),逆反应速率________ ,H2的转化率_______ 。
(3)研究发现铁催化剂表面上合成氨的反应历程如图所示,其中吸附在铁催化剂表面上的微粒用*标注。
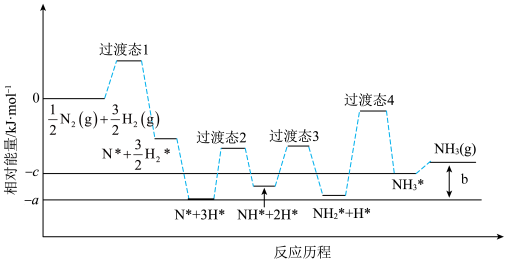
该反应历程中最大活化能对应步骤的化学方程式为_______ 。合成氨反应: N2(g)+
N2(g)+ H2(g)
H2(g) NH3(g)的△H=
NH3(g)的△H=_______ kJ/mol(用图中字母表示)。
(1)合成氨工业中采用循环操作,主要是为了
| A.增大化学反应速率 | B.提高氮气和氢气的利用率 |
| C.降低氨的沸点 | D.提高平衡混合物中氨的含量 |
(2)在密闭容器中通入amolN2和6molH2,若在一定条件下反应达到平衡状态,容器中剩余cmolN2。
①达到平衡时,H2转化率为
②若把容器的体积扩大一倍,则正反应速率
(3)研究发现铁催化剂表面上合成氨的反应历程如图所示,其中吸附在铁催化剂表面上的微粒用*标注。

该反应历程中最大活化能对应步骤的化学方程式为
 N2(g)+
N2(g)+ H2(g)
H2(g) NH3(g)的△H=
NH3(g)的△H=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知萃取剂A、B中pH对钴离子、锰离子萃取率的影响如图所示,为了除去Mn2+,应选择萃取剂___________ (填“A”或“B”)。


您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I、近年来我国大力加强CO2与H2催化合成甲醇(CH3OH)技术的工业化量产研究,实现可持续发展。下表是不同条件下合成氨反应达平衡时反应混合物中氨的体积分数(%)。
(1)目前,我国合成氨工业生产中采用的压强一般不高于30MPa,主要原因是_____ 。
Ⅱ、
(2)250℃时,在体积为2.0L的恒容密闭容器中加入6molH2、2molCO2和催化剂,10min时反应达到平衡,测得c(CH3OH)=0.75mol/L。
①下列描述中能说明上述反应已达平衡的是_____ (填编号)。
A.3ν正(H2)=ν逆(CH3OH)
B.容器中气体压强不随时间而变化
C.c(H2) ∶c(CO2)=1∶1
D.容器中气体平均相对分子质量不随时间而变化
②化学平衡常数K=_____ 。
(3)合成总反应在起始物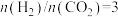 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为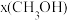 ,在恒温
,在恒温 ℃下的
℃下的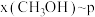 、在恒压
、在恒压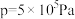 下的
下的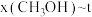 如图所示。
如图所示。
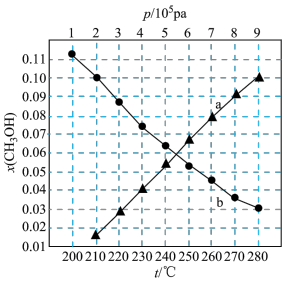
①请用各物质的平衡分压(p(H2)、p(CO2)、p(CH3OH)、p(H2O))表示总反应的平衡常数,表达式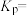
_____
②图中对应等压过程的曲线是_____ ,判断的理由是_____ ;
③当 时,
时, 的平衡转化率
的平衡转化率
_____ (保留小数点后一位)
| 0.1MPa | 10MPa | 20MPa | 30MPa | 60MPa | |
| 500℃ | 0.10 | 10.6 | 19.1 | 26.4 | 42.2 |
| 600℃ | 0.05 | 4.50 | 9.10 | 13.8 | 23.1 |
(1)目前,我国合成氨工业生产中采用的压强一般不高于30MPa,主要原因是
Ⅱ、
(2)250℃时,在体积为2.0L的恒容密闭容器中加入6molH2、2molCO2和催化剂,10min时反应达到平衡,测得c(CH3OH)=0.75mol/L。
①下列描述中能说明上述反应已达平衡的是
A.3ν正(H2)=ν逆(CH3OH)
B.容器中气体压强不随时间而变化
C.c(H2) ∶c(CO2)=1∶1
D.容器中气体平均相对分子质量不随时间而变化
②化学平衡常数K=
(3)合成总反应在起始物
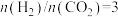 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为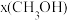 ,在恒温
,在恒温 ℃下的
℃下的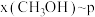 、在恒压
、在恒压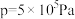 下的
下的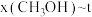 如图所示。
如图所示。
①请用各物质的平衡分压(p(H2)、p(CO2)、p(CH3OH)、p(H2O))表示总反应的平衡常数,表达式
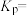
②图中对应等压过程的曲线是
③当
 时,
时, 的平衡转化率
的平衡转化率
您最近一年使用:0次
【推荐1】在一定容积的密闭容器中,进行如下化学反应: ,其化学平衡常数K和温度T的关系如表所示:
,其化学平衡常数K和温度T的关系如表所示:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=____________ 。
(2)该反应为________ (填“吸热”或“放热”)反应。
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为________ ℃。该温度下加入1 mol CO2(g)和1 mol H2(g),充分反应,达到平衡时,CO2的转化率为________ 。
 ,其化学平衡常数K和温度T的关系如表所示:
,其化学平衡常数K和温度T的关系如表所示:T/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K=
(2)该反应为
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】T℃时,在一个体积为 2L 的容器中,A 气体与 B 气体反应生成 C 气体,反应过程中 A、B、C 的变化如图所示。
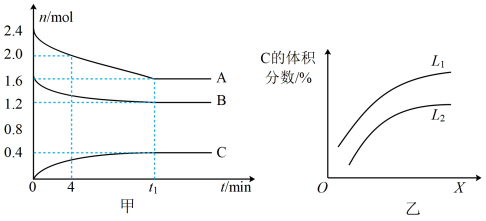
(1)根据甲图,写出反应的化学方程式_______ 。
(2)0~4min 时,A的平均反应速率为_______ 。
(3)已知:K(300℃)>K(350℃),该反应是_______ (填“吸热”或“放热”)反应。
(4)如乙图是上述反应平衡混合气中C的体积分数随温度或压强变化的曲线,图中L(L1、L2)、X分别代表温度或压强。其中 X 代表的是_______ (填“温度”或“压强”)。判断 L1_______ L2(填“>” 或“<”),理由是_______ 。

(1)根据甲图,写出反应的化学方程式
(2)0~4min 时,A的平均反应速率为
(3)已知:K(300℃)>K(350℃),该反应是
(4)如乙图是上述反应平衡混合气中C的体积分数随温度或压强变化的曲线,图中L(L1、L2)、X分别代表温度或压强。其中 X 代表的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氮氧化物在含能材料、医药等方面有着广泛应用。请回答:
(1)一定温度下,在恒容密闭容器中 可发生下列反应:
可发生下列反应: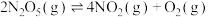

①该反应自发进行的条件是________ 。
②下表为反应在 温度下的部分实验数据:
温度下的部分实验数据:
在500s时,
________ 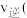 填“
填“ ”、“
”、“ ”或“
”或“ ”
” 。若在
。若在 温度下进行实验,1000s时测得反应体系中
温度下进行实验,1000s时测得反应体系中 浓度为
浓度为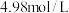 ,则
,则
________ 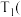 填“
填“ ”、“
”、“ ”或“
”或“ ”
” 。
。
(2)在 与
与 之间存在反应:
之间存在反应: 。将
。将 放入1L恒容密闭容器中,测得其平衡转化率
放入1L恒容密闭容器中,测得其平衡转化率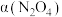 随温度变化如图所示。
随温度变化如图所示。
①337.5K时,反应平衡常数
________ 。
②已知:
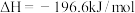
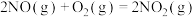

则反应 的
的
________  。
。
(3)某学习小组设想利用A装置电解制备绿色硝化剂 ,装置如下
,装置如下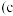 、d为惰性电极
、d为惰性电极 :
:

已知:无水硝酸可在液态 中发生微弱电离。写出生成
中发生微弱电离。写出生成 的电极反应式
的电极反应式________ 。
(1)一定温度下,在恒容密闭容器中
 可发生下列反应:
可发生下列反应: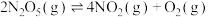

①该反应自发进行的条件是
②下表为反应在
 温度下的部分实验数据:
温度下的部分实验数据: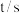 | 0 | 500 | 1000 |
 |  | 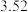 | 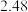 |
在500s时,

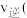 填“
填“ ”、“
”、“ ”或“
”或“ ”
” 。若在
。若在 温度下进行实验,1000s时测得反应体系中
温度下进行实验,1000s时测得反应体系中 浓度为
浓度为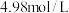 ,则
,则
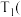 填“
填“ ”、“
”、“ ”或“
”或“ ”
” 。
。(2)在
 与
与 之间存在反应:
之间存在反应: 。将
。将 放入1L恒容密闭容器中,测得其平衡转化率
放入1L恒容密闭容器中,测得其平衡转化率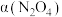 随温度变化如图所示。
随温度变化如图所示。
①337.5K时,反应平衡常数

②已知:

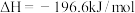
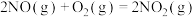

则反应
 的
的
 。
。(3)某学习小组设想利用A装置电解制备绿色硝化剂
 ,装置如下
,装置如下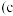 、d为惰性电极
、d为惰性电极 :
:
已知:无水硝酸可在液态
 中发生微弱电离。写出生成
中发生微弱电离。写出生成 的电极反应式
的电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】工业合成氨原理为:N2(g)+3H2(g)⇌2NH3(g),在T1 ℃时,向2 L恒容密闭容器中充入1 mol N2和3 mol H2发生上述反应,测得N2的体积分数φ(N2)随时间(t)的变化如下表:
请回答下列问题:
(1)0~40 min内,用H2表示该反应的平均速率为_______ 。
(2)N2的平衡转化率为_______ (保留三位有效数字)。
(3)若反应开始时,容器内的压强为0.6 MPa,则第40 min末时容器内的压强为_______ MPa;该反应在T1℃时的压强平衡常数Kp=_______ (MPa)-2。
(4)T1℃时,向该容器中投入三种成分的浓度如下:
该时刻,正、逆反应速率的大小关系为:v正(N2)_______ v逆(N2)(填“>”“<”或“=”)。
| t/min | 0 | 10 | 20 | 30 | 40 | 50 |
| φ(N2) | 0.250 | 0.225 | 0.210 | 0.203 | 0.200 | 0.200 |
(1)0~40 min内,用H2表示该反应的平均速率为
(2)N2的平衡转化率为
(3)若反应开始时,容器内的压强为0.6 MPa,则第40 min末时容器内的压强为
(4)T1℃时,向该容器中投入三种成分的浓度如下:
| 物质 | N2 | H2 | NH3 |
| c/(mol·L-1) | 2 | 5 | 3 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】合成氨工业在国民生产中有重要意义。以下是关于合成氨的有关问题,请回答。
(1)在容积为 的恒温密闭容器中加入
的恒温密闭容器中加入 的
的 和
和 的
的 在一定条件下发生反应:
在一定条件下发生反应:
 ,在5分钟时反应恰好达到平衡,此时测得
,在5分钟时反应恰好达到平衡,此时测得 的物质的量为
的物质的量为 。这段时间内用
。这段时间内用 表示的反应速率为
表示的反应速率为 =
=___________ 。
(2)下列各项能作为判断该反应达到化学平衡状态的依据是___________(填序号字母)。
(3)已知合成氨反应 在
在 时平衡常数
时平衡常数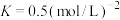 。某实验小组在
。某实验小组在 时,测得某时刻
时,测得某时刻 、
、 、
、 ,此时刻该反应的化学平衡速率v(正)
,此时刻该反应的化学平衡速率v(正)___________ v(逆)(填“>”、“=”或“<”)。
(4)如下图表示:若在 、
、 条件下,向一密闭容器中通入N2、H2(按物质的量之比
条件下,向一密闭容器中通入N2、H2(按物质的量之比 )发生反应,测得容器内总压强
)发生反应,测得容器内总压强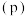 与反应时间
与反应时间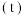 的关系如图所示。
的关系如图所示。
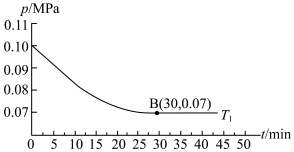
图中 点的分压平衡常数Kp=
点的分压平衡常数Kp=___________ MPa-2 (用平衡分压代替平衡浓度计算,结果保留两位小数,气体分压=气体总压×物质的量分数)。
(1)在容积为
 的恒温密闭容器中加入
的恒温密闭容器中加入 的
的 和
和 的
的 在一定条件下发生反应:
在一定条件下发生反应:
 ,在5分钟时反应恰好达到平衡,此时测得
,在5分钟时反应恰好达到平衡,此时测得 的物质的量为
的物质的量为 。这段时间内用
。这段时间内用 表示的反应速率为
表示的反应速率为 =
=(2)下列各项能作为判断该反应达到化学平衡状态的依据是___________(填序号字母)。
A.容器内 、 、 、 、 的物质的量浓度之比为 的物质的量浓度之比为 |
B. |
| C.混合气体的密度保持不变 |
| D.容器内压强保持不变 |
(3)已知合成氨反应
 在
在 时平衡常数
时平衡常数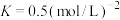 。某实验小组在
。某实验小组在 时,测得某时刻
时,测得某时刻 、
、 、
、 ,此时刻该反应的化学平衡速率v(正)
,此时刻该反应的化学平衡速率v(正)(4)如下图表示:若在
 、
、 条件下,向一密闭容器中通入N2、H2(按物质的量之比
条件下,向一密闭容器中通入N2、H2(按物质的量之比 )发生反应,测得容器内总压强
)发生反应,测得容器内总压强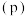 与反应时间
与反应时间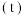 的关系如图所示。
的关系如图所示。
图中
 点的分压平衡常数Kp=
点的分压平衡常数Kp=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)碳、氮和铝的单质及其化合物在工农业生产和生活中有重要作用。真空碳热还原一氯化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
2Al2O3(s)+ 2AlCl3(g)+ 6C(s)=6AlCl(g)+ 6CO(g);△H= a kJ•mol-1
3AlCl(g)= 2Al(l)+ AlCl3(g);△H= b kJ•mol-1
反应Al2O3(s)+ 3C(s)= 2Al(l)+ 3CO(g)的△H=______ kJ•mol-1(用含a、b的代数式表示)。
(2)830K时,在密闭容器中发生下列可逆反应:CO(g)+H2O(g)⇌CO2(g)+H2(g)△H<0,试回答下列问题:
①若起始时c(CO)=2mol•L﹣1,c(H2O)=3mol•L﹣1,达到平衡时CO的转化率为60%,则在该温度下,该反应的平衡常数K=__ .
②在相同温度下,若起始时c(CO)=1mol•L﹣1,c(H2O)=2mol•L﹣1,反应进行一段时间后,测得H2的浓度为0.5mol•L﹣1,则此时该反应是否达到平衡状态__ (填“是”与“否”),此时v(正)__ v(逆)(填“大于”“小于”或“等于”),你判断的依据是____________________
③若降低温度,该反应的K值将__ ,该反应的化学反应速率将__ (均填“增大”“减小”或“不变”).
2Al2O3(s)+ 2AlCl3(g)+ 6C(s)=6AlCl(g)+ 6CO(g);△H= a kJ•mol-1
3AlCl(g)= 2Al(l)+ AlCl3(g);△H= b kJ•mol-1
反应Al2O3(s)+ 3C(s)= 2Al(l)+ 3CO(g)的△H=
(2)830K时,在密闭容器中发生下列可逆反应:CO(g)+H2O(g)⇌CO2(g)+H2(g)△H<0,试回答下列问题:
①若起始时c(CO)=2mol•L﹣1,c(H2O)=3mol•L﹣1,达到平衡时CO的转化率为60%,则在该温度下,该反应的平衡常数K=
②在相同温度下,若起始时c(CO)=1mol•L﹣1,c(H2O)=2mol•L﹣1,反应进行一段时间后,测得H2的浓度为0.5mol•L﹣1,则此时该反应是否达到平衡状态
③若降低温度,该反应的K值将
您最近一年使用:0次



