解题方法
1 . 若做实验时不小心粘上高锰酸钾,皮肤上的斑要很久才能消除,而用 的稀溶液在稀硫酸条件下洗涤,可以马上消除,发生反应的化学方程式为
的稀溶液在稀硫酸条件下洗涤,可以马上消除,发生反应的化学方程式为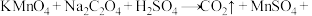

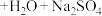 (未配平),下列关于此反应的叙述正确的是
(未配平),下列关于此反应的叙述正确的是
 的稀溶液在稀硫酸条件下洗涤,可以马上消除,发生反应的化学方程式为
的稀溶液在稀硫酸条件下洗涤,可以马上消除,发生反应的化学方程式为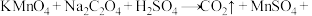

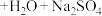 (未配平),下列关于此反应的叙述正确的是
(未配平),下列关于此反应的叙述正确的是A.当有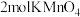 参加反应时,该反应转移10 mol电子 参加反应时,该反应转移10 mol电子 |
B.该反应右边方框内的产物是 |
C.该反应的氧化剂是 |
D.配平后, 的化学计量数是10 的化学计量数是10 |
您最近一年使用:0次
2 . 城市污水中含有一定量的 、
、 ,向污水中加入菌体和
,向污水中加入菌体和 溶液,在菌体的作用下依次发生过程Ⅰ、过程Ⅱ,从而实现
溶液,在菌体的作用下依次发生过程Ⅰ、过程Ⅱ,从而实现 、
、 的脱除,其过程如图所示。下列说法正确的是
的脱除,其过程如图所示。下列说法正确的是
 、
、 ,向污水中加入菌体和
,向污水中加入菌体和 溶液,在菌体的作用下依次发生过程Ⅰ、过程Ⅱ,从而实现
溶液,在菌体的作用下依次发生过程Ⅰ、过程Ⅱ,从而实现 、
、 的脱除,其过程如图所示。下列说法正确的是
的脱除,其过程如图所示。下列说法正确的是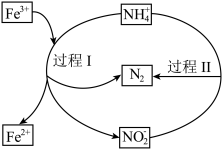
A.“过程Ⅰ”中 为催化剂 为催化剂 |
B. 的氧化性强于 的氧化性强于 |
C.“过程Ⅱ”中氧化产物和还原产物的质量之比为 |
D.“过程Ⅰ”中 和 和 的物质的量之比为 的物质的量之比为 ,则氧化剂与还原剂物质的量之比为 ,则氧化剂与还原剂物质的量之比为 |
您最近一年使用:0次
2023-09-23更新
|
584次组卷
|
10卷引用:湖南省湘西州吉首市2024届高三上学期第二届中小学生教师解题大赛化学试题
湖南省湘西州吉首市2024届高三上学期第二届中小学生教师解题大赛化学试题湘豫名校联考2023-2024学年高三上学期一轮诊断化学试题河南省信阳市信阳高级中学2024届高三上学期9月一模化学试题山东省滨州市2023-2024学年高三上学期11月期中考试化学试题黑龙江省双鸭山市第一中学2023-2024学年高三上学期10月月考化学试题(已下线)选择题11-15江西省赣州市信丰中学2023-2024学年高一上学期11月月考化学试题河南省南阳市邓州市第一高级中学校2023-2024学年高一上学期期末考试化学试题(已下线)选择题6-10河南省洛阳市宜阳县第一高级中学2023-2024学年高一上学期(研学班)期末考试化学试卷
名校
解题方法
3 . 已知电离常数:Ka(HCN)=5×10-10,H2CO3:Ka1=4.3×10-7,Ka2=5.6×10-11,下列离子方程式书写正确的是
A.向KCN(aq)中通入少量的CO2气体:CO2+H2O+2CN-=2HCN+CO |
| B.少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO |
| C.氢氧化铁沉淀溶解于过量氢碘酸溶液中:2Fe(OH)3+6H++2I-=2Fe2++6H2O+I2 |
D.向Ba(OH)2溶液中加入少量的NaHCO3溶液:2HCO +Ba2++2OH-=BaCO3↓+CO +Ba2++2OH-=BaCO3↓+CO +2H2O +2H2O |
您最近一年使用:0次
2023-06-18更新
|
1745次组卷
|
8卷引用:江西省赣州地区2023-2024学年十大教学能手选拔赛高中化学试题
江西省赣州地区2023-2024学年十大教学能手选拔赛高中化学试题河南省郑州外国语学校2023届高三下学期全真模拟五理综化学试题(已下线)第九章单元测试卷(已下线)考点1 电离平衡(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)电离平衡2024届湖南省长沙市雅礼中学高三下学期4月综合测试化学试题湖南省雅礼中学2024届高三下学期综合自主压轴测试 (一)化学题2024届广东省梅州市兴宁市第一中学高三下学期二模化学试题
名校
解题方法
4 . 已知Mn2O 与S2-在酸性溶液中能发生反应: Mn2O
与S2-在酸性溶液中能发生反应: Mn2O +3S2-+14H+=2Mn3++3S↓+7H2O,则Mn2O
+3S2-+14H+=2Mn3++3S↓+7H2O,则Mn2O 中锰元素的化合价是
中锰元素的化合价是
 与S2-在酸性溶液中能发生反应: Mn2O
与S2-在酸性溶液中能发生反应: Mn2O +3S2-+14H+=2Mn3++3S↓+7H2O,则Mn2O
+3S2-+14H+=2Mn3++3S↓+7H2O,则Mn2O 中锰元素的化合价是
中锰元素的化合价是| A.+2 | B.+4 | C.+3 | D.+6 |
您最近一年使用:0次
2022-02-28更新
|
853次组卷
|
36卷引用:云南省玉溪市江川区第二中学2020-2021学年高一下学期竞赛化学试题
云南省玉溪市江川区第二中学2020-2021学年高一下学期竞赛化学试题河南省安阳市第三十六中学2017-2018学年高一上学期期中考试化学试题安徽省阜阳市第三中学2018-2019学年高一下学期开学考试化学试题夯基提能2020届高三化学选择题对题专练——氧化还原反应的实际应用广东省2020年普通高中学业水平考试化学合格性考试模拟试题(七)陕西省汉中市龙岗学校2019-2020学年高一上学期期末考试化学试题(已下线)【南昌新东方】江西省九江一中2013-2014学年高一上学期期中考试化学试题广东省珠海市第二中学2019-2020学年高一上学期期中考试化学试题广东省中山纪念中学2019-2020学年高一上学期第二次段考化学试题山东省济宁市邹城兖矿一中2020-2021学年度高一9月月考化学试题吉林公主岭范家屯一中2020-2021学年高一上学期期中考试化学试题(已下线)【浙江新东方】30湖南省岳阳市楚雄中学2020-2021学年高一上学期期中考试化学试题广东省湛江市第四中学2020-2021学年高一上学期期中考试化学试题北京市铁路第二中学2020-2021学年高一上学期期中考试化学试题(已下线)【南昌新东方】9. 2020 高一上 铁路一中 刘惠文 钟欣(已下线)【浙江新东方】双师 (55)宁夏青铜峡市高级中学2020-2021学年高一12月月考化学试题河北衡水市第十四中学2020-2021学年高一上学期三调考试化学试题天津市滨海新区2020-2021学年高一上学期期末考试化学试题河北省衡水市武邑武罗学校2020-2021学年高一上学期期中考试化学试题新疆巴音郭楞蒙古自治州第二中学2021届高三上学期第一次摸底考试化学试题河北省衡水市武强中学2020-2021学年高一上学期第一次月考化学试题黑龙江省鸡西市第一中学2020-2021学年高一上学期第一次月考化学试题四川省成都市第七中学2021-2022学年高一上学期期中考试化学试题四川省攀枝花市第十五中学校2021-2022学年高一上学期期中考试化学试题安徽省安庆市第十中学2021-2022学年高一上学期10月月考化学试题江苏省宿迁市泗阳县实验高级中学2021-2022学年高一上学期第二次调研测试化学试题广东省梅州市兴宁市叶塘中学2021-2022学年高一上学期摸底考试化学试题浙江省绿谷联盟2022-2023学年高一上学期10月份考试化学试题 黑龙江省鹤岗市第一中学2022-2023学年高一上学期10月月考化学试题山西省晋城市第一中学校2022-2023学年高一上学期第二次调研考试化学试题四川省仁寿县铧强中学2021-2022学年高一上学期半期考试化学试题云南省昆明市第八中学2020-2021学年高一上学期期中考试化学试题(已下线)专题七 氧化还原反应天津市宁河区2023-2024学年高一上学期期末考试化学试题
名校
解题方法
5 . 金属铁与一定浓度HNO3反应的离子方程式可表示为:aFe+ bNO + cH+ = dFe3++fFe2+ + gNO2↑+ hNO↑+ kH2O。下列关系一定成立的是
+ cH+ = dFe3++fFe2+ + gNO2↑+ hNO↑+ kH2O。下列关系一定成立的是
 + cH+ = dFe3++fFe2+ + gNO2↑+ hNO↑+ kH2O。下列关系一定成立的是
+ cH+ = dFe3++fFe2+ + gNO2↑+ hNO↑+ kH2O。下列关系一定成立的是| A.c+3d+2f= b | B.2b=g+k |
| C.2b=g-k | D.若a=b,则f=g |
您最近一年使用:0次
2021-08-01更新
|
165次组卷
|
2卷引用:2018年广东和广西高中学生化学竞赛试题
名校
6 . +5价V在不同pH下微粒的化学式不同,其微粒与pH关系如表所示。
另外,V价态不同在溶液中颜色不同,如V2+(紫色)、V3+(绿色)、VO2+(蓝色)、VO (黄色)、VO
(黄色)、VO (无色)、V5O
(无色)、V5O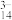 (红棕色)等。下列说法正确的是
(红棕色)等。下列说法正确的是
| 含钒元素的不同微粒 | VO | VO | V2O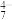 | VO |
| pH | 4~6 | 6~8 | 8~10 | 10~12 |
 (黄色)、VO
(黄色)、VO (无色)、V5O
(无色)、V5O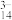 (红棕色)等。下列说法正确的是
(红棕色)等。下列说法正确的是A.VO 转化为V2O 转化为V2O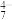 的离子反应为2VO 的离子反应为2VO +H2O=V2O +H2O=V2O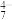 +2H+ +2H+ |
B.含VO 的溶液中滴加氨水有NH4VO3沉淀产生,该过程V元素被还原 的溶液中滴加氨水有NH4VO3沉淀产生,该过程V元素被还原 |
C.酸性VO 滴加烧碱溶液,溶液显红棕色时离子反应为5VO 滴加烧碱溶液,溶液显红棕色时离子反应为5VO +8OH-=V5O +8OH-=V5O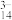 +4H2O +4H2O |
| D.紫色VSO4溶液中滴加酸性高锰酸钾溶液,溶液颜色出现绿色→蓝色→黄色,两个过程均失去1mol电子 |
您最近一年使用:0次
2021-04-14更新
|
966次组卷
|
12卷引用:第34届(2021年)高中化学奥林匹克竞赛浙江省预赛试题
第34届(2021年)高中化学奥林匹克竞赛浙江省预赛试题河南省洛阳市宜阳县第一高级中学2023-2024学年高一下学期竞赛选拔赛化学试题湖北师大附中2021届高三下学期教学质量测评化学试题(已下线)2021年高考化学押题预测卷(山东卷)02(含考试版、答题卡、参考答案、全解全析)湖北省华大新高考联盟2021-2022学年高三下学期开学考试化学试题浙江省绍兴市2022届高三选考科目适应性考试(二模)化学试题陕西省西安市长安区第一中学2021-2022学年高一下学期期末考试化学(理科)试题陕西省西安市长安区第一中学2021-2022学年高一下学期期末考试化学(理科)试题黑龙江省富锦市第一中学2022-2023学年高二下学期期末考试化学试题湖北省武汉市第六中学2023-2024学年高三上学期第一次月考化学试题河南省济源市第四中学2023-2024学年高一上学期11月月考化学试题河南省周口恒大中学2023-2024学年高三下学期4月期中考试化学试题
名校
解题方法
7 . 某反应的氧化剂与还原剂及部分产物如下所示:2Mn2+ + 5IO4— + …… → 2MnO4— + ……已知该反应体系还包括H+、H2O与另一种含碘微粒。对于该氧化还原反应说法正确的是
| A.Mn2+是氧化剂,IO4—是还原剂 |
| B.体系中另一种含碘微粒为I— |
| C.随着反应进行,溶液pH不断上升 |
| D.每有1 mol IO4—参加反应,转移2 mol电子 |
您最近一年使用:0次
2019-12-24更新
|
200次组卷
|
3卷引用:2019年上海市高中生化学竞赛初赛试题(“华理一化工杯”)初赛试题
8 . 已知Co2O3在酸性溶液中易被还原成Co2+,且Co2O3、Cl2、FeCl3、I2的氧化性依次减弱。下列叙述中,正确的是( )
| A.FeCl3溶液能使淀粉-KI试纸变蓝 |
| B.Cl2通入FeI2溶液中,可存在反应3Cl2+6FeI2═2FeCl3+4FeI3 |
| C.每1 mol Co2O3在酸性溶液中被氧化生成Co2+时转移2 mol e-电子 |
| D.I2是ⅦA族元素单质,具有较强的氧化性,可以将Co2+氧化成Co2O3 |
您最近一年使用:0次
2019-12-16更新
|
99次组卷
|
9卷引用:第25届(2011年)高中生化学竞赛(河北赛区)初赛试题
第25届(2011年)高中生化学竞赛(河北赛区)初赛试题(已下线)2011届山东省济南市高三教学质量调研(一模)化学试卷2016-2017学年浙江省余姚中学高一上期中化学试卷【全国百强校】福建省三明市第一中学2019届高三上学期第一次月考化学试题福建省长汀、连城一中等六校2020届高三上学期期中考联考化学试题宁夏回族自治区吴忠市青铜峡市高级中学2020届高三上学期第二次月考化学试题广西桂林市龙胜中学2020届高三上学期期中考试化学试题(已下线)【新东方】【2019】【高一上】【期中考】【JYZ】【化学】陕西省榆林市第十二中学2021届高三上学期第二次月考化学试题
名校
9 . 某离子反应中涉及H2O、ClO-、NH4+、H+、N2、Cl-六种粒子。其中N2、ClO-的物质的量随时间变化的曲线如图所示。下列判断不正确的是
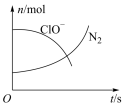

| A.该反应的氧化剂是ClO- |
| B.消耗1mol还原剂,转移3mol电子 |
| C.氧化剂与还原剂的物质的量之比为2:3 |
| D.该离子方程式为3ClO-+2NH4+=2H++N2↑+3Cl-+3H2O |
您最近一年使用:0次
2019-03-12更新
|
999次组卷
|
6卷引用:江西省横峰中学等五校2019-2020学年新高一竞赛班联考化学试题
名校
解题方法
10 . 铀(U)常见化合价有+4 和+6,硝酸铀酰[UO2(NO3)2]加热可发生如下分解,UO2(NO3)2----UxOy+ NO2↑+ O2↑,在600K 时,将气体产物收集于试管中并倒扣于水中,气体全部被吸收,水充满试管。则生成的铀的氧化物化学式
| A.UO2 | B.2UO2·UO3 | C.UO2·2UO3 | D.UO3 |
您最近一年使用:0次
2018-08-31更新
|
302次组卷
|
11卷引用:第22届(2008年)全国高中学生化学竞赛(河南省赛区)预赛试题
第22届(2008年)全国高中学生化学竞赛(河南省赛区)预赛试题湖南省2007年高中学生化学竞赛试题2015届江苏省连云港市赣榆县海头高中高三上学期期中化学试卷2015届上海理工大学附中高三上学期月考化学试卷2016届上海市崇明县高三上学期第一次模拟化学试卷辽宁省大连育明高级中学、本溪市高级中学2018届高三10月月考化学(理)试题(已下线)学科网2019年高考化学一轮复习讲练测2.4 氧化还原反应的规律及应用 练(已下线)专题04 氧化还原反应-备战2021届高考化学二轮复习题型专练安徽省黄山市屯溪第一中学2022届高三10月月考化学试题湖南省邵阳市第二中学2022-2023学年高三上学期第三次月考化学试题内蒙古赤峰二中2022-2023高一上学期期末考试化学试题



