解题方法
1 . 舍勒发现氯气是在1774年,当他使软锰矿与浓盐酸混合并加热时,产生了一种黄绿色的气体,发生的反应为MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,这种气体有强烈的刺激性气味。舍勒制备出氯气以后,把它溶解在水里,发现这种水溶液对纸张、蔬菜和花都具有永久性的漂白作用;他还发现氯气能与金属、非金属、碱等发生化学反应。实验室常用高锰酸钾代替二氧化锰制取氯气,反应的化学方程式为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,下列对于该反应的说法正确的是
MnCl2+Cl2↑+2H2O,这种气体有强烈的刺激性气味。舍勒制备出氯气以后,把它溶解在水里,发现这种水溶液对纸张、蔬菜和花都具有永久性的漂白作用;他还发现氯气能与金属、非金属、碱等发生化学反应。实验室常用高锰酸钾代替二氧化锰制取氯气,反应的化学方程式为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,下列对于该反应的说法正确的是
 MnCl2+Cl2↑+2H2O,这种气体有强烈的刺激性气味。舍勒制备出氯气以后,把它溶解在水里,发现这种水溶液对纸张、蔬菜和花都具有永久性的漂白作用;他还发现氯气能与金属、非金属、碱等发生化学反应。实验室常用高锰酸钾代替二氧化锰制取氯气,反应的化学方程式为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,下列对于该反应的说法正确的是
MnCl2+Cl2↑+2H2O,这种气体有强烈的刺激性气味。舍勒制备出氯气以后,把它溶解在水里,发现这种水溶液对纸张、蔬菜和花都具有永久性的漂白作用;他还发现氯气能与金属、非金属、碱等发生化学反应。实验室常用高锰酸钾代替二氧化锰制取氯气,反应的化学方程式为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,下列对于该反应的说法正确的是| A.KMnO4是还原剂 | B.MnCl2是氧化产物 |
| C.HCl在反应中得电子 | D.HCl体现还原性和酸性 |
您最近半年使用:0次
解题方法
2 . 下列方案设计、现象和结论都正确的是
| 实验目的 | 方案设计 | 现象和结论 | |
| A | 探究浓硫酸的特性 | 将浓硫酸滴到蔗糖表面,固体变黑膨胀,有刺激性气体产生 | 浓硫酸有脱水性和强氧化性 |
| B | 检验 和浓盐酸反应后是否有酸剩余 和浓盐酸反应后是否有酸剩余 | 取少量反应后的溶液于试管中,依次加入稀硝酸、 溶液,观察 溶液,观察 | 若产生大量白色沉淀,则说明盐酸有剩余 |
| C | 证明 有氧化性 有氧化性 | 将足量的 溶液滴入酸性高锰酸钾溶液中 溶液滴入酸性高锰酸钾溶液中 | 若溶液中的紫红色褪去,则证明 有氧化性 有氧化性 |
| D | 鉴别两种红棕色气体 和 和 | 向盛有 淀粉溶液的试管中通入气体 淀粉溶液的试管中通入气体 | 溶液变成蓝色,说明该气体是 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
3 . 双碱法脱硫过程如图所示。下列说法不正确的是

A.过程Ⅰ中, 表现出酸性氧化物的性质 表现出酸性氧化物的性质 |
B.过程Ⅱ中, 可氧化 可氧化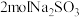 |
| C.过程Ⅰ和过程Ⅱ中都发生了氧化还原反应 |
D.总反应为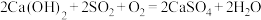 |
您最近半年使用:0次
名校
4 . 工厂烟气(主要污染物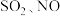 )直接排放会造成空气污染,需处理后才能排放。
)直接排放会造成空气污染,需处理后才能排放。
(1)“纳米零价铁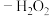 ”体系可将烟气中难溶的NO氧化为可溶的
”体系可将烟气中难溶的NO氧化为可溶的 。在一定温度下,将
。在一定温度下,将 溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。
溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。
① 催化
催化 分解产生HO·,HO·将NO氧化为
分解产生HO·,HO·将NO氧化为 的机理如下图所示,Y的化学式为
的机理如下图所示,Y的化学式为___________ 。 反应生成HNO3的化学方程式为
反应生成HNO3的化学方程式为___________ 。
③纳米零价铁的作用是___________ 。
④NO脱除率随温度的变化如下图所示。温度高于120℃时,NO脱除率随温度升高呈现下降趋势的主要原因是___________ 。 、
、 ,下列措施能提高尾气中NO和
,下列措施能提高尾气中NO和 去除率的有
去除率的有___________ (填字母)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
(3) 脱硝技术已成为使用广泛和成熟的烟气净化技术,脱硝效率高达
脱硝技术已成为使用广泛和成熟的烟气净化技术,脱硝效率高达 %以上。反应机理如下图所示,写出该反应发生的化学方程式
%以上。反应机理如下图所示,写出该反应发生的化学方程式___________ 。 溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为
溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为 的转化率随
的转化率随 溶液初始pH(用稀盐酸调节)的变化如图所示:
溶液初始pH(用稀盐酸调节)的变化如图所示: 溶液中,
溶液中, 氧化NO生成Cl-和
氧化NO生成Cl-和 ,其离子方程式为
,其离子方程式为___________ 。
②NaClO溶液的初始pH越小,NO转化率越高。其原因是___________ 。
(5)目前, 溶液广泛地应用于脱硫脱硝。某课外小组同学设计了如图喷淋吸收塔装置
溶液广泛地应用于脱硫脱硝。某课外小组同学设计了如图喷淋吸收塔装置 如图
如图 。设计该装置的优点是
。设计该装置的优点是___________ 。脱硝反应中,每吸收标准状况下448mL的NO,转移的电子数为___________ mol。
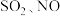 )直接排放会造成空气污染,需处理后才能排放。
)直接排放会造成空气污染,需处理后才能排放。(1)“纳米零价铁
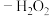 ”体系可将烟气中难溶的NO氧化为可溶的
”体系可将烟气中难溶的NO氧化为可溶的 。在一定温度下,将
。在一定温度下,将 溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。
溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。①
 催化
催化 分解产生HO·,HO·将NO氧化为
分解产生HO·,HO·将NO氧化为 的机理如下图所示,Y的化学式为
的机理如下图所示,Y的化学式为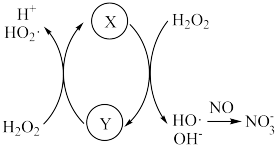
 反应生成HNO3的化学方程式为
反应生成HNO3的化学方程式为③纳米零价铁的作用是
④NO脱除率随温度的变化如下图所示。温度高于120℃时,NO脱除率随温度升高呈现下降趋势的主要原因是

 、
、 ,下列措施能提高尾气中NO和
,下列措施能提高尾气中NO和 去除率的有
去除率的有A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
(3)
 脱硝技术已成为使用广泛和成熟的烟气净化技术,脱硝效率高达
脱硝技术已成为使用广泛和成熟的烟气净化技术,脱硝效率高达 %以上。反应机理如下图所示,写出该反应发生的化学方程式
%以上。反应机理如下图所示,写出该反应发生的化学方程式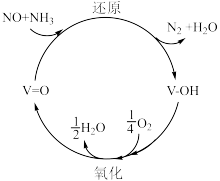
 溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为
溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为 的转化率随
的转化率随 溶液初始pH(用稀盐酸调节)的变化如图所示:
溶液初始pH(用稀盐酸调节)的变化如图所示: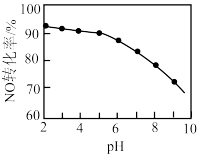
 溶液中,
溶液中, 氧化NO生成Cl-和
氧化NO生成Cl-和 ,其离子方程式为
,其离子方程式为②NaClO溶液的初始pH越小,NO转化率越高。其原因是
(5)目前,
 溶液广泛地应用于脱硫脱硝。某课外小组同学设计了如图喷淋吸收塔装置
溶液广泛地应用于脱硫脱硝。某课外小组同学设计了如图喷淋吸收塔装置 如图
如图 。设计该装置的优点是
。设计该装置的优点是
您最近半年使用:0次
解题方法
5 . 既有氧化性,又有还原性的微粒是
| A.Fe | B.Fe2+ | C.Fe3+ | D.Cl- |
您最近半年使用:0次
名校
解题方法
6 . 已知还原性: ,则将
,则将 通入到
通入到 、
、 、
、 的混合溶液中,
的混合溶液中, 、
、 、
、 生成的先后顺序为
生成的先后顺序为
 ,则将
,则将 通入到
通入到 、
、 、
、 的混合溶液中,
的混合溶液中, 、
、 、
、 生成的先后顺序为
生成的先后顺序为A. , , , , | B. , , , , | C. , , , , | D. , , , , |
您最近半年使用:0次
7 . 氯化亚铜(CuCl)是一种易水解的白色固体。以低品位铜矿砂(主要成分CuS)为原料制备CuCl的工艺流程如图所示。
(1)“酸溶1”时,CuS作_______ (填“氧化剂”或“还原剂”)。
(2)“除锰”时,Cu2+转化为Cu(NH3)4CO3,Mn2+转化为MnCO3沉淀。沉锰的反应化学方程式为_______ 。将生成的MnCO3分离出来的实验操作为_______ 。
(3)“酸溶2”投料后,以一定的速率搅拌反应,可提高铜浸出率的措施有_______ (只答一种方法)。
(4)合成步骤加入Na2SO3的速率不宜过快,否则会产生_______ 气体。
(5)“洗涤”应先用稀盐酸洗涤,其目的是_______ 。

(1)“酸溶1”时,CuS作
(2)“除锰”时,Cu2+转化为Cu(NH3)4CO3,Mn2+转化为MnCO3沉淀。沉锰的反应化学方程式为
(3)“酸溶2”投料后,以一定的速率搅拌反应,可提高铜浸出率的措施有
(4)合成步骤加入Na2SO3的速率不宜过快,否则会产生
(5)“洗涤”应先用稀盐酸洗涤,其目的是
您最近半年使用:0次
解题方法
8 . 下列离子方程式正确的是
A.向 溶液中加入少量 溶液中加入少量 溶液: 溶液: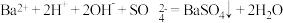 |
B.将SO2通入NaCIO溶液中:SO2+H2O+ClO-=HClO+HSO |
| C.FeBr2与等物质的量氯气在溶液中反应:Cl2+2Br-=Br2+2Cl- |
D.向苯酚钠溶液中通入少量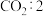 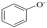 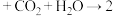 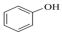  |
您最近半年使用:0次
名校
9 .  是一种压电材料。实验室以纯净
是一种压电材料。实验室以纯净 为原料,采用下列路线模拟工业制备
为原料,采用下列路线模拟工业制备 ,“焙烧”所得产物的物质的量之比为1:4.下列说法错误的是
,“焙烧”所得产物的物质的量之比为1:4.下列说法错误的是
 是一种压电材料。实验室以纯净
是一种压电材料。实验室以纯净 为原料,采用下列路线模拟工业制备
为原料,采用下列路线模拟工业制备 ,“焙烧”所得产物的物质的量之比为1:4.下列说法错误的是
,“焙烧”所得产物的物质的量之比为1:4.下列说法错误的是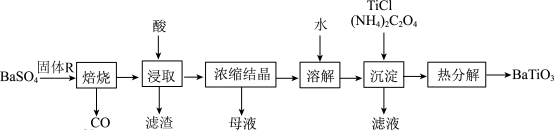
| A.“焙烧”步骤中固体R为炭粉,作还原剂 |
| B.“浸取”步骤应选用的酸是稀硫酸 |
| C.“浸取”过程中会产生有毒气体,需要在通风橱中进行 |
D.“沉淀”产品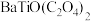 的热分解方程式为 的热分解方程式为 |
您最近半年使用:0次
名校
解题方法
10 . 下列方程式与所给事实相符的是
| A.“84”消毒液不能和洁厕灵混用是因为ClO-+Cl-+2H+=Cl2 ↑+H2O |
| B.Fe和稀硝酸反应:Fe+2H+=Fe2++H2 ↑ |
C.向NaClO溶液中通如少量SO2:2ClO-+SO2+H2O=2HClO+ |
| D.向CuSO4溶液中通入H2S气体:Cu2++S2-=CuS↓ |
您最近半年使用:0次



