解题方法
1 . 在下列溶液中能大量共存的是
A.在0.1 mol·L-1 NaHCO3溶液中:Al3+、Mg2+、 、Cl- 、Cl- |
B.在0.1 mol·L-1 H2S溶液中:Fe3+、 、Cl-、 、Cl-、 |
C.在0.1 mol·L-1 Ba(OH)2溶液中:Na+、K+、 、Br- 、Br- |
D.在0.1 mol·L-1 NH3·H2O溶液中:Cu2+、 、 、 、 、 |
您最近半年使用:0次
解题方法
2 . N-羧基丙氨酸酸酐广泛用于生物领域,用碳酸二甲酯 和丙氨酸
和丙氨酸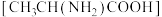 为原料可以制备N-羧基丙氨酸酸酐,其反应机理如图所示。下列说法错误的是
为原料可以制备N-羧基丙氨酸酸酐,其反应机理如图所示。下列说法错误的是
 和丙氨酸
和丙氨酸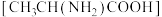 为原料可以制备N-羧基丙氨酸酸酐,其反应机理如图所示。下列说法错误的是
为原料可以制备N-羧基丙氨酸酸酐,其反应机理如图所示。下列说法错误的是
| A.在强酸性环境不利于反应进行 |
B.该过程中 元素的化合价发生改变 元素的化合价发生改变 |
C.反应过程中有 的断裂和形成 的断裂和形成 |
D.用甘氨酸 代替丙氨酸,可制得 代替丙氨酸,可制得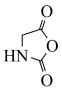 |
您最近半年使用:0次
3 . 鲜榨苹果汁是人们喜爱的饮料。由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由淡绿色的Fe2+ 变为棕黄色Fe3+ 。若在榨汁的时候加入适量的维生素C,可有效防止这种现象的发生。 这说明维生素C具有
| A.氧化性 | B.还原性 | C.酸性 | D.碱性 |
您最近半年使用:0次
2024·浙江·模拟预测
4 . 关于反应2Cu2S+14HNO3=2CuSO4+2Cu(NO3)2+5NO2↑+5NO↑+7H2O,下列说法不正确 的是
| A.HNO3在反应中体现氧化性和酸性 |
| B.Cu2S和Cu(NO3)2都是氧化产物 |
| C.0.2mol Cu2S参加反应,转移电子2mol |
| D.随着产物中NO和NO2比例的改变,CuSO4和Cu(NO3)2的比例也发生相应的改变 |
您最近半年使用:0次
5 . 某同学研究浓硝酸的氧化性,做了如下实验:
资料:
i. 中
中 、
、 、
、 元素的化合价依次为:
元素的化合价依次为: 价、
价、 价、
价、 价。
价。
ii. 的性质类似卤素离子,能被氧化为黄色的
的性质类似卤素离子,能被氧化为黄色的 ,
, 可聚合为红色的
可聚合为红色的 。
。
(1)写出实验Ⅰ中铜和浓硝酸反应的离子方程式______ 。
(2)甲同学对实验Ⅱ中红色褪去的原因提出猜想,浓硝酸氧化了 ,其理论依据是
,其理论依据是______ 。
甲同学为证明猜想,做了如下实验Ⅲ
实验Ⅲ: 溶液,溶液立即变红是因为生成了
溶液,溶液立即变红是因为生成了______ (填化学式)。推测红棕色气体是______ (填化学式)。
(4)研究 的转化产物:
的转化产物:
实验Ⅳ:
a.将实验Ⅲ 中的气体通入
中的气体通入 和
和 的混合溶液中,有白色沉淀生成。
的混合溶液中,有白色沉淀生成。
b.过滤、洗涤白色沉淀,取少量于试管中,加入过量的稀硝酸,沉淀完全溶解,再滴加少量 溶液,不褪色。
溶液,不褪色。
c.另取少量实验Ⅲ中反应后的溶液,加入 溶液,产生大量白色沉淀。
溶液,产生大量白色沉淀。
①通过 证实了红棕色气体中不含
证实了红棕色气体中不含 ,证据是
,证据是______ 。
② 中,
中, 溶液中加入
溶液中加入 溶液以增大
溶液以增大 浓度的目的是
浓度的目的是______ 。
③由上述实验现象可知: 转化的最终产物中一定有
转化的最终产物中一定有______ 。
序号 | 实验Ⅰ | 实验Ⅱ |
操作 | 1:2 | 1:2 |
实验现象 | 铜片迅速溶解,产生大量红棕色气体,溶液变成绿色 | 滴入硝酸后,溶液变为红色,一段时间后,溶液褪为无色。 |
i.
 中
中 、
、 、
、 元素的化合价依次为:
元素的化合价依次为: 价、
价、 价、
价、 价。
价。ii.
 的性质类似卤素离子,能被氧化为黄色的
的性质类似卤素离子,能被氧化为黄色的 ,
, 可聚合为红色的
可聚合为红色的 。
。(1)写出实验Ⅰ中铜和浓硝酸反应的离子方程式
(2)甲同学对实验Ⅱ中红色褪去的原因提出猜想,浓硝酸氧化了
 ,其理论依据是
,其理论依据是甲同学为证明猜想,做了如下实验Ⅲ
实验Ⅲ:
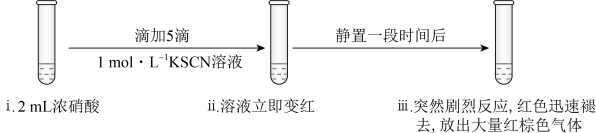
 溶液,溶液立即变红是因为生成了
溶液,溶液立即变红是因为生成了(4)研究
 的转化产物:
的转化产物:实验Ⅳ:
a.将实验Ⅲ
 中的气体通入
中的气体通入 和
和 的混合溶液中,有白色沉淀生成。
的混合溶液中,有白色沉淀生成。b.过滤、洗涤白色沉淀,取少量于试管中,加入过量的稀硝酸,沉淀完全溶解,再滴加少量
 溶液,不褪色。
溶液,不褪色。c.另取少量实验Ⅲ中反应后的溶液,加入
 溶液,产生大量白色沉淀。
溶液,产生大量白色沉淀。①通过
 证实了红棕色气体中不含
证实了红棕色气体中不含 ,证据是
,证据是②
 中,
中, 溶液中加入
溶液中加入 溶液以增大
溶液以增大 浓度的目的是
浓度的目的是③由上述实验现象可知:
 转化的最终产物中一定有
转化的最终产物中一定有
您最近半年使用:0次
2024·浙江·模拟预测
解题方法
6 . 根据物质的组成和结构可推测其性质,下列推测不合理 的是
| 物质 | 性质描述 | 推测 | |
| A | 三甲基铝Al(CH3)3 | 暴露空气中瞬间着火,与水反应剧烈 | 水反应可得到CH4和Al(OH)3 |
| B | 三氟化氯 ClF3 | 极强助燃剂,能发生自耦电离: 2ClF3  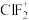 + + | BrF3比ClF3更易发生自耦电离 |
| C | 亚铁氰化钾K4[Fe(CN)6] | 食盐的抗结剂,3K4[Fe(CN)6] 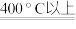 12KCN+Fe3C+5C+3N2↑ 12KCN+Fe3C+5C+3N2↑ | 在空气中灼烧,生成K2CO3、FeO、CO2和N2 |
| D | 魔酸SbF5∙HSO3F | 五氟化锑和氟磺酸的混合物,是一种酸性比普通无机酸强106~1010倍的超强酸 | SbF5∙HF是超强酸 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
7 . 下列反应的离子方程式书写正确的是
A. 溶液与醋酸溶液反应: 溶液与醋酸溶液反应: |
B. 溶液与 溶液与 溶液反应: 溶液反应: |
C.电解饱和食盐水: |
D.向 溶液中通入过量的 溶液中通入过量的 : : |
您最近半年使用:0次
2024高三·全国·专题练习
解题方法
8 . 化学需氧量(COD)是指用强氧化剂将1 L废水中的还原性物质氧化为二氧化碳和水所消耗的氧化剂的量,并换算成以O2为氧化剂时所消耗O2的质量。水体COD值常作为水体中有机污染物相对含量的综合指标之一,Fenton(Fe2+/H2O2)法能产生Fe3+和具有强氧化性的羟基自由基(·OH)引发一系列链式反应,被广泛应用于有机废水的治理。
(1)羟基自由基(·OH)的电子式为___________ 。
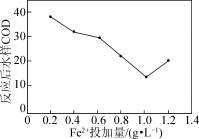
(2)分别取初始pH=4、COD=80的废水200 mL,加入200 mL H2O2,改变起始投加FeSO4·7H2O的量,反应相同时间。测得反应后水样COD随Fe2+投加量的关系如图所示。当Fe2+投加量超过1 g·L-1时,反应后水样COD不降反升的原因可能是___________ 。 )的氧化技术引起关注。研究发现,一种Mn3O4石墨烯纳米复合材料对催化活化S2O
)的氧化技术引起关注。研究发现,一种Mn3O4石墨烯纳米复合材料对催化活化S2O 产生SO
产生SO 具有很好的效果。S2O
具有很好的效果。S2O 结构如图所示。
结构如图所示。 的使用范围更广。SO
的使用范围更广。SO 在强碱性条件下反应生成·OH,写出该反应的离子方程式:
在强碱性条件下反应生成·OH,写出该反应的离子方程式:___________ 。
② 一种制取Mn3O4—石墨烯纳米复合材料的物种转化关系可表示如下(GO表示石墨烯):___________ mol。
③利用该复合材料催化活化S2O 并去除废水中有机污染物的可能反应机理如图所示。该机理可描述为
并去除废水中有机污染物的可能反应机理如图所示。该机理可描述为___________ 。
(1)羟基自由基(·OH)的电子式为
(2)分别取初始pH=4、COD=80的废水200 mL,加入200 mL H2O2,改变起始投加FeSO4·7H2O的量,反应相同时间。测得反应后水样COD随Fe2+投加量的关系如图所示。当Fe2+投加量超过1 g·L-1时,反应后水样COD不降反升的原因可能是
 )的氧化技术引起关注。研究发现,一种Mn3O4石墨烯纳米复合材料对催化活化S2O
)的氧化技术引起关注。研究发现,一种Mn3O4石墨烯纳米复合材料对催化活化S2O 产生SO
产生SO 具有很好的效果。S2O
具有很好的效果。S2O 结构如图所示。
结构如图所示。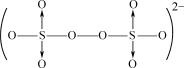
 的使用范围更广。SO
的使用范围更广。SO 在强碱性条件下反应生成·OH,写出该反应的离子方程式:
在强碱性条件下反应生成·OH,写出该反应的离子方程式:② 一种制取Mn3O4—石墨烯纳米复合材料的物种转化关系可表示如下(GO表示石墨烯):
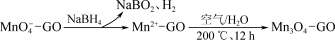
③利用该复合材料催化活化S2O
 并去除废水中有机污染物的可能反应机理如图所示。该机理可描述为
并去除废水中有机污染物的可能反应机理如图所示。该机理可描述为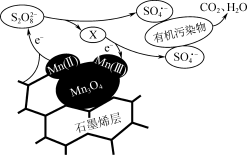
您最近半年使用:0次
9 . 物质类别和元素价态是认识物质两个重要维度。下图列为硫及其化合物的价类二维图,下列说法错误的是
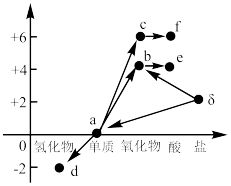
A.附着有a的试管,可用 清洗 清洗 | B.b和d反应生成a时,d发生还原反应 |
| C.b、c两种氧化物的VSEPR模型相同 | D.g的钠盐可与f的稀溶液反应生成a和b |
您最近半年使用:0次
名校
解题方法
10 . 氢化铵 与氯化铵的结构相似,又知
与氯化铵的结构相似,又知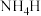 与水反应有氢气生成,下列叙述不正确的是
与水反应有氢气生成,下列叙述不正确的是
 与氯化铵的结构相似,又知
与氯化铵的结构相似,又知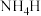 与水反应有氢气生成,下列叙述不正确的是
与水反应有氢气生成,下列叙述不正确的是A.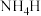 是离子化合物 是离子化合物 |
B.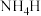 溶于水,形成的溶液显酸性 溶于水,形成的溶液显酸性 |
C.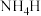 固体投入少量水中,有两种气体产生 固体投入少量水中,有两种气体产生 |
D.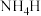 与水反应时, 与水反应时,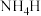 是氧化剂 是氧化剂 |
您最近半年使用:0次



