名校
1 . 红树林沉积物中微生物驱动的硫循环过程原理如图所示,下列叙述错误的是
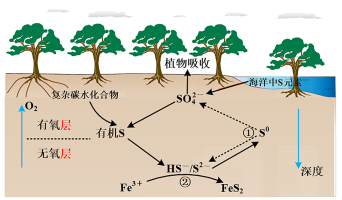
A.海洋中疏元素主要以 形式存在 形式存在 |
B.依据价态及图示分析,在无氧层, 是重要的氧化剂 是重要的氧化剂 |
| C.硫循环与金属元素的耦合可以有效固定沉积物中的重金属元素 |
| D.反应①与反应②过程中硫元素均被氧化 |
您最近半年使用:0次
2 . 常温下,往烧杯中加入10mL1mol/LFeCl3溶液和10mL2mol/LKI溶液,c(I-)随时间变化如图所示,不考虑溶液混合时体积的改变。下列说法正确的是
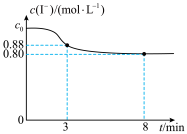
| A.c0=2 |
| B.3~8min内,Fe3+的平均反应速率为0.08mol/(L·min) |
| C.8min时,往烧杯中滴加KSCN溶液,溶液不变红 |
D.烧杯中发生反应的离子方程式为2Fe3++2I- 2Fe2++I2 2Fe2++I2 |
您最近半年使用:0次
名校
解题方法
3 . 下列变化中,气体被还原的是
| A.NH3制硝酸 | B.CO2使Na2O2固体变为白色 |
| C.HCl使Na2SiO3溶液产生胶状沉淀 | D.Cl2使FeBr2溶液变为黄色 |
您最近半年使用:0次
名校
4 . 门捷列夫在研究周期表时预言了“类硅”元素锗和“类铝”元素镓等11种元素。锗及其化合物应用于航空航天测控、光纤通讯等领域。一种提纯二氧化锗粗品(主要含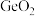 、
、 )的工艺如下:
)的工艺如下: 与碱反应生成
与碱反应生成 ;
; 与碱反应生成
与碱反应生成 。
。
ii. 极易水解生成
极易水解生成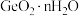 ;
; 沸点
沸点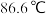 。
。
(1) 位于同主族
位于同主族 的下一周期,
的下一周期, 在周期表中的位置是
在周期表中的位置是___________ 。
(2)从原子结构角度解释金属性 比
比 强的原因
强的原因___________ 。
(3)“氧化”过程是将 氧化为
氧化为 ,其离子方程式为
,其离子方程式为___________ 。
(4)加盐酸蒸馏生成 ,生成
,生成 的化学方程式为
的化学方程式为___________ 。
(5)高纯二氧化锗的含量常采用碘酸钾 滴定法进行测定。碘酸钾
滴定法进行测定。碘酸钾 与碘化钾(KI)在酸性情况下会生成使淀粉变蓝的碘单质。配平离子方程式
与碘化钾(KI)在酸性情况下会生成使淀粉变蓝的碘单质。配平离子方程式___________ 。

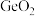 、
、 )的工艺如下:
)的工艺如下: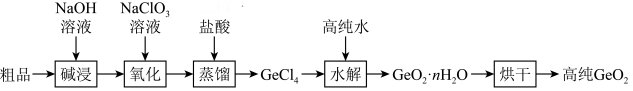
 与碱反应生成
与碱反应生成 ;
; 与碱反应生成
与碱反应生成 。
。ii.
 极易水解生成
极易水解生成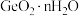 ;
; 沸点
沸点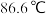 。
。(1)
 位于同主族
位于同主族 的下一周期,
的下一周期, 在周期表中的位置是
在周期表中的位置是(2)从原子结构角度解释金属性
 比
比 强的原因
强的原因(3)“氧化”过程是将
 氧化为
氧化为 ,其离子方程式为
,其离子方程式为(4)加盐酸蒸馏生成
 ,生成
,生成 的化学方程式为
的化学方程式为(5)高纯二氧化锗的含量常采用碘酸钾
 滴定法进行测定。碘酸钾
滴定法进行测定。碘酸钾 与碘化钾(KI)在酸性情况下会生成使淀粉变蓝的碘单质。配平离子方程式
与碘化钾(KI)在酸性情况下会生成使淀粉变蓝的碘单质。配平离子方程式
您最近半年使用:0次
名校
解题方法
5 . 以下是一系列非金属元素间的置换反应,其中不能说明反应前的非金属单质的氧化性强于产物中非金属单质的氧化性的是
A. | B.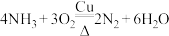 |
C. | D. |
您最近半年使用:0次
6 . 铬铁渣是火法炼铬所产生的废渣,其中铬以低价态的 存在,主要杂质为铁、铝、硅的氧化物,从铬铁渣中提取铬的一种流程如图所示
存在,主要杂质为铁、铝、硅的氧化物,从铬铁渣中提取铬的一种流程如图所示 存在,在碱性介质中以
存在,在碱性介质中以 存在。下列说法错误的是
存在。下列说法错误的是
 存在,主要杂质为铁、铝、硅的氧化物,从铬铁渣中提取铬的一种流程如图所示
存在,主要杂质为铁、铝、硅的氧化物,从铬铁渣中提取铬的一种流程如图所示
 存在,在碱性介质中以
存在,在碱性介质中以 存在。下列说法错误的是
存在。下列说法错误的是A.焙烧后,含铬化合物主要以 存在 存在 |
| B.加水浸取过滤,滤渣1的主要成分应含有铁元素 |
| C.除铝步骤,为使杂质沉淀彻底,应加入足量稀硫酸 |
D.还原步骤发生的离子反应是: |
您最近半年使用:0次
7 . 细菌可以促使铁、氮两种元素进行氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如下图所示。_______ (填字母序号)。
a.N2转化为氨态氮 b.硝化过程 c.反硝化过程
(2)氮肥是水体中氨态氮的主要来源之一,氨气是生产氮肥的主要原料,工业合成氨的化学方程式为_______ 。
(3)硝化过程中,含氮物质发生_______ (填“氧化”或“还原”)反应。
(4)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02 mol 氮气时,转移的电子的物质的量为_______ mol。
(5)NO是大气污染气体,测定某气体样品中NO含量操作如下:将2L气样通入适量酸化的H2O2溶液中,使NO完全被氧化为 。向上述反应后溶液中加入30 mL0.1 mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与3.5 mL、0.1 mol·L−1K2Cr2O7恰好反应。NO被H2O2氧化为
。向上述反应后溶液中加入30 mL0.1 mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与3.5 mL、0.1 mol·L−1K2Cr2O7恰好反应。NO被H2O2氧化为 的离子方程式是
的离子方程式是______ 。上述过程中发生下列反应:3Fe2++ +4H+=NO↑+3Fe3++2H2O;
+4H+=NO↑+3Fe3++2H2O; + 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O。则气样中NO的含量为
+ 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O。则气样中NO的含量为_______ mg /L。(保留计算过程)
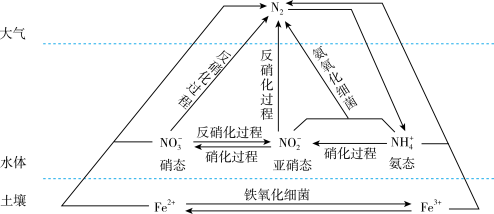
a.N2转化为氨态氮 b.硝化过程 c.反硝化过程
(2)氮肥是水体中氨态氮的主要来源之一,氨气是生产氮肥的主要原料,工业合成氨的化学方程式为
(3)硝化过程中,含氮物质发生
(4)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02 mol 氮气时,转移的电子的物质的量为
(5)NO是大气污染气体,测定某气体样品中NO含量操作如下:将2L气样通入适量酸化的H2O2溶液中,使NO完全被氧化为
 。向上述反应后溶液中加入30 mL0.1 mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与3.5 mL、0.1 mol·L−1K2Cr2O7恰好反应。NO被H2O2氧化为
。向上述反应后溶液中加入30 mL0.1 mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与3.5 mL、0.1 mol·L−1K2Cr2O7恰好反应。NO被H2O2氧化为 的离子方程式是
的离子方程式是 +4H+=NO↑+3Fe3++2H2O;
+4H+=NO↑+3Fe3++2H2O; + 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O。则气样中NO的含量为
+ 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O。则气样中NO的含量为
您最近半年使用:0次
名校
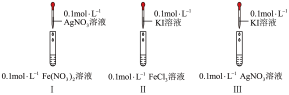
8 . 通过如下实验,比较 、
、 、
、 的氧化性。
的氧化性。
(1)实验室 溶液通常盛放在
溶液通常盛放在___________ 试剂瓶中。
(2)Ⅱ中反应的离子方程式为___________ 。
(3)I、Ⅱ中的现象说明___________。
(4)实验后,I试管壁上的黑色沉淀可用___________洗去。
(5)写出检验I中是否含有 的方法。
的方法。___________ 。
(6)检验Ⅱ中是否含有 不可选用:___________。(不定项)
不可选用:___________。(不定项)
(7)推测Ⅲ中未发生 氧化
氧化 的原因
的原因___________ 。
 、
、 、
、 的氧化性。
的氧化性。
| 实验现象 |
I中产生黑色沉淀,滴加 溶液,变红 溶液,变红 | |
| Ⅱ中溶液呈棕黄色,滴加淀粉溶液,变蓝 | |
| Ⅲ中产生黄色沉淀,滴加淀粉溶液,未变蓝 |
(1)实验室
 溶液通常盛放在
溶液通常盛放在(2)Ⅱ中反应的离子方程式为
(3)I、Ⅱ中的现象说明___________。
A.氧化性顺序: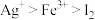 | B.氧化性顺序: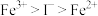 |
C.还原性顺序: | D.还原性顺序: |
(4)实验后,I试管壁上的黑色沉淀可用___________洗去。
| A.酒精 | B.二硫化碳 | C.浓硝酸 | D.热盐酸 |
(5)写出检验I中是否含有
 的方法。
的方法。(6)检验Ⅱ中是否含有
 不可选用:___________。(不定项)
不可选用:___________。(不定项)| A.氢氧化钠溶液 | B.酸性高辒酸钾溶液 | C.硫氰化钾溶液 | D.稀氨水 |
(7)推测Ⅲ中未发生
 氧化
氧化 的原因
的原因
您最近半年使用:0次
名校
解题方法
9 . 如图是硫元素的“价—类”二维图:___________ 。
(2) 的浓溶液与铝单质在加热条件下可以发生化学反应生成
的浓溶液与铝单质在加热条件下可以发生化学反应生成 ,该反应的化学方程式为
,该反应的化学方程式为___________ ,可用___________ 法收集 。
。
A.向上排空气 B.向下排空气 C.排饱和食盐水 D.排饱和 溶液
溶液
(3) 和
和 均能使品红溶液褪色,但两种气体按一定比例同时通入品红溶液中无明显现象。用离子方程式解释原因
均能使品红溶液褪色,但两种气体按一定比例同时通入品红溶液中无明显现象。用离子方程式解释原因___________ 。
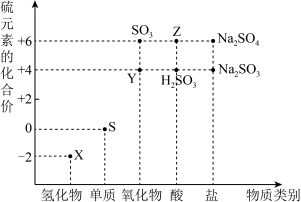
(2)
 的浓溶液与铝单质在加热条件下可以发生化学反应生成
的浓溶液与铝单质在加热条件下可以发生化学反应生成 ,该反应的化学方程式为
,该反应的化学方程式为 。
。A.向上排空气 B.向下排空气 C.排饱和食盐水 D.排饱和
 溶液
溶液(3)
 和
和 均能使品红溶液褪色,但两种气体按一定比例同时通入品红溶液中无明显现象。用离子方程式解释原因
均能使品红溶液褪色,但两种气体按一定比例同时通入品红溶液中无明显现象。用离子方程式解释原因
您最近半年使用:0次
10 . 研究和采取措施去除氮氧化物尾气和水中硝酸盐造成的氮污染备受关注。
Ⅰ氧化吸收法 酸性条件下,NaClO溶液氧化 、NO和
、NO和 等生成
等生成 和
和 。
。
(1)其他条件一定, 转化为
转化为 的转化率随水体溶液初始pH的变化如图1所示。
的转化率随水体溶液初始pH的变化如图1所示。 、NO和
、NO和 三种气体中,相同条件下最易被NaClO氧化的是
三种气体中,相同条件下最易被NaClO氧化的是________ 。
②在酸性水体中,加入NaClO溶液吸收 的离子方程式为
的离子方程式为________ 。
③水体溶液初始pH越小, 转化率越高。其原因是
转化率越高。其原因是________ 。
(2)NaClO吸收液还可以同时脱除烟气中NO和 。研究发现NaClO吸收液在不同初始pH条件下,对流动烟气的脱硫效率都接近100%,而对NO的脱除率如图2所示:
。研究发现NaClO吸收液在不同初始pH条件下,对流动烟气的脱硫效率都接近100%,而对NO的脱除率如图2所示:
①酸性条件下, 的脱除率高于NO,其原因除
的脱除率高于NO,其原因除 的还原性比NO强外,还可能是
的还原性比NO强外,还可能是________ 。
②若用盐酸调节NaClO吸收液pH,不仅不利于NO的吸收,还会在反应过程中生成一种有毒气体,其化学式为________ 。
Ⅱ催化还原法
(3)在 的催化条件下,使用
的催化条件下,使用 作为还原剂,可将水中的
作为还原剂,可将水中的 转化为
转化为 。该反应机理分为三步,如题17图3所示:第一步:
。该反应机理分为三步,如题17图3所示:第一步:________ (补充完整该步反应机理);第二步: 从Cu表面迁移至W的表面;第三步:
从Cu表面迁移至W的表面;第三步: 在W表面吸附并解离为活性氢原子(W-H),W-H将
在W表面吸附并解离为活性氢原子(W-H),W-H将 还原为
还原为 ,同时W-H将CuO还原为Cu,自身转化为W,实现Cu和W的催化循环。
,同时W-H将CuO还原为Cu,自身转化为W,实现Cu和W的催化循环。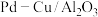 作为还原硝酸盐过程的催化剂,其催化机理与
作为还原硝酸盐过程的催化剂,其催化机理与 相似。但还原过程中检测到三种含氮化合物微粒,其浓度变化如图4所示,在1.5小时以后,
相似。但还原过程中检测到三种含氮化合物微粒,其浓度变化如图4所示,在1.5小时以后, 的百分含量不断减少,
的百分含量不断减少, 的百分含量不断增多的可能原因是
的百分含量不断增多的可能原因是________ 。
Ⅰ氧化吸收法 酸性条件下,NaClO溶液氧化
 、NO和
、NO和 等生成
等生成 和
和 。
。(1)其他条件一定,
 转化为
转化为 的转化率随水体溶液初始pH的变化如图1所示。
的转化率随水体溶液初始pH的变化如图1所示。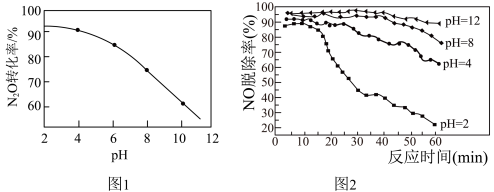
 、NO和
、NO和 三种气体中,相同条件下最易被NaClO氧化的是
三种气体中,相同条件下最易被NaClO氧化的是②在酸性水体中,加入NaClO溶液吸收
 的离子方程式为
的离子方程式为③水体溶液初始pH越小,
 转化率越高。其原因是
转化率越高。其原因是(2)NaClO吸收液还可以同时脱除烟气中NO和
 。研究发现NaClO吸收液在不同初始pH条件下,对流动烟气的脱硫效率都接近100%,而对NO的脱除率如图2所示:
。研究发现NaClO吸收液在不同初始pH条件下,对流动烟气的脱硫效率都接近100%,而对NO的脱除率如图2所示:①酸性条件下,
 的脱除率高于NO,其原因除
的脱除率高于NO,其原因除 的还原性比NO强外,还可能是
的还原性比NO强外,还可能是②若用盐酸调节NaClO吸收液pH,不仅不利于NO的吸收,还会在反应过程中生成一种有毒气体,其化学式为
Ⅱ催化还原法
(3)在
 的催化条件下,使用
的催化条件下,使用 作为还原剂,可将水中的
作为还原剂,可将水中的 转化为
转化为 。该反应机理分为三步,如题17图3所示:第一步:
。该反应机理分为三步,如题17图3所示:第一步: 从Cu表面迁移至W的表面;第三步:
从Cu表面迁移至W的表面;第三步: 在W表面吸附并解离为活性氢原子(W-H),W-H将
在W表面吸附并解离为活性氢原子(W-H),W-H将 还原为
还原为 ,同时W-H将CuO还原为Cu,自身转化为W,实现Cu和W的催化循环。
,同时W-H将CuO还原为Cu,自身转化为W,实现Cu和W的催化循环。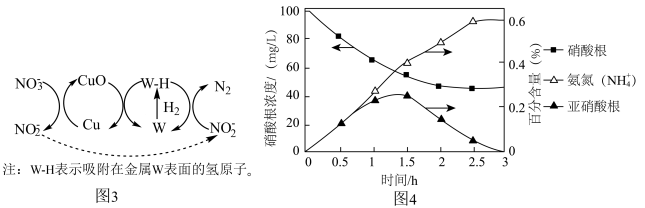
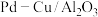 作为还原硝酸盐过程的催化剂,其催化机理与
作为还原硝酸盐过程的催化剂,其催化机理与 相似。但还原过程中检测到三种含氮化合物微粒,其浓度变化如图4所示,在1.5小时以后,
相似。但还原过程中检测到三种含氮化合物微粒,其浓度变化如图4所示,在1.5小时以后, 的百分含量不断减少,
的百分含量不断减少, 的百分含量不断增多的可能原因是
的百分含量不断增多的可能原因是
您最近半年使用:0次