1 . K2FeO4是常见的水处理剂,其原理如图所示。请回答下列问题:
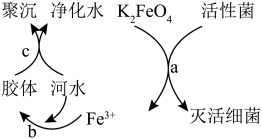
(1)高铁酸钾(K2FeO4)中铁元素的化合价为________ .
(2)过程a中K2FeO4体现________ (填“氧化”或“还原”)性,氧化产物是________ 。
(3)过程b反应的离子方程式为________ ,过程c属于________ (填“物理”或“化学”)变化。
(4)碱性条件下用Fe(OH)3和KClO反应制备K2FeO4。配平其反应的化学方程式:________ 。
Fe(OH)3+_______KOH+_______KClO=_______ K2FeO4+_______KCl+_______H2O
(5)根据以上K2FeO4净水原理,相比于Cl2,其优点是________ 。

(1)高铁酸钾(K2FeO4)中铁元素的化合价为
(2)过程a中K2FeO4体现
(3)过程b反应的离子方程式为
(4)碱性条件下用Fe(OH)3和KClO反应制备K2FeO4。配平其反应的化学方程式:
Fe(OH)3+_______KOH+_______KClO=_______ K2FeO4+_______KCl+_______H2O
(5)根据以上K2FeO4净水原理,相比于Cl2,其优点是
您最近一年使用:0次
2 . 用还原法可以将硝酸厂烟气中的大量氮氧化物(NOx)转化为无害物质。常温下,将NO与H2的混合气体通入Ce(SO4)2与Ce2(SO4)2的混合溶液中,其物质的转化过程如图所示。
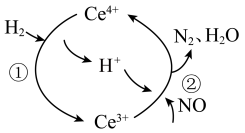
下列说法正确的是

下列说法正确的是
| A.反应①②中含Ce的物质均作氧化剂 |
| B.反应①中氧化剂与还原剂的个数之比为1:2 |
C.总反应的化学方程式为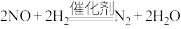 |
| D.转化反应前后混合溶液内Ce3+和Ce4+的总数保持不变 |
您最近一年使用:0次
3 . 国产航母001A等舰艇的船底都涂有含 的防污涂料,制备
的防污涂料,制备 的一种方法为
的一种方法为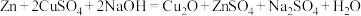 。该反应的下列说法正确的是
。该反应的下列说法正确的是
 的防污涂料,制备
的防污涂料,制备 的一种方法为
的一种方法为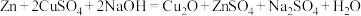 。该反应的下列说法正确的是
。该反应的下列说法正确的是A. 得到电子 得到电子 | B. 被还原 被还原 |
C. 是还原剂 是还原剂 | D.消耗 ,转移 ,转移 电子 电子 |
您最近一年使用:0次
4 .  是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得
是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得 :
: 。下列说法不正确的是
。下列说法不正确的是
 是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得
是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得 :
: 。下列说法不正确的是
。下列说法不正确的是A. 在反应中得到电子 在反应中得到电子 | B.反应前后Cl元素化合价降低 |
C. 发生氧化反应 发生氧化反应 | D.1个 参加反应有2个电子转移 参加反应有2个电子转移 |
您最近一年使用:0次
5 . 近年来,我国储氧纳米碳管研究获重大进展,电弧法合成的碳纳米管常伴有大量物质一碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯。其反应的化学方程式为:
(1)此反应的氧化剂是_____ ,氧化产物是_____ ,比较两者氧化性的强弱______ 。
(2)在上述反应中 表现出来的性质是_______(填选项编号)。
表现出来的性质是_______(填选项编号)。
(3)上述反应中若产生气体物质11g,则消耗的还原剂_______ g。

(1)此反应的氧化剂是
(2)在上述反应中
 表现出来的性质是_______(填选项编号)。
表现出来的性质是_______(填选项编号)。| A.酸性 | B.氧化性 | C.吸水性 | D.脱水性 |
您最近一年使用:0次
6 . 实验室,以 为原料制备
为原料制备 、KOH的工艺流程如下图所示:
、KOH的工艺流程如下图所示:
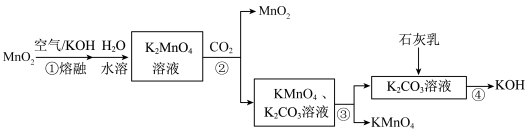
下列说法正确的是
 为原料制备
为原料制备 、KOH的工艺流程如下图所示:
、KOH的工艺流程如下图所示:
下列说法正确的是
| A.步骤①用烧杯作反应器 | B.步骤②中 只体现还原性 只体现还原性 |
| C.步骤③用到的玻璃仪器有漏斗、烧杯、玻璃棒等 | D.步骤④过程中有电子转移 |
您最近一年使用:0次
解题方法
7 . 现有下列三个氧化还原反应:
① ;
;
②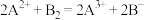 ;
;
③ ;
;
根据上述反应,判断下列结论中正确的是
①
 ;
;②
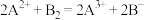 ;
;③
 ;
;根据上述反应,判断下列结论中正确的是
A.在溶液中不可能发生反应: |
B. 是 是 的氧化产物, 的氧化产物, 是 是 的还原产物 的还原产物 |
C.还原性强弱顺序为: |
D.只除去含有 、 、 和 和 混合溶液中的 混合溶液中的 ,应加入 ,应加入 |
您最近一年使用:0次
解题方法
8 . 氯气是一种重要的化工原料,它的发现和研究经过了化学家们的不懈努力。
(1)舍勒发现氯气的方法是实验室制取氯气(如图)的主要方法之一。
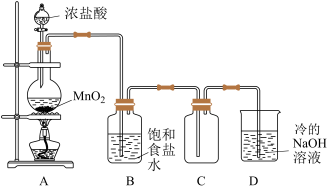
①盛装浓盐酸的仪器名称为_____ ;装置A中发生反应的化学方程式为___________ 。
②装置B中饱和食盐水的作用是___________ 。
③装置D中发生反应的离子方程式为___________ 。
(2)含氧化合物亚氯酸钠( )是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
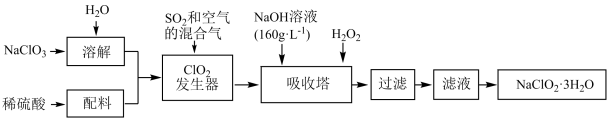
已知:纯 易分解爆炸,一般用稀有气体或空气稀释到10%以下较安全。
易分解爆炸,一般用稀有气体或空气稀释到10%以下较安全。
① 发生器中发生反应的离子方程式为
发生器中发生反应的离子方程式为_____ ,在发生器中鼓入空气的作用可能是_____ 。
②吸收塔中为防止 被还原成NaCl,可用还原性适中的
被还原成NaCl,可用还原性适中的 作还原剂,写出吸收塔中发生反应的化学方程式:
作还原剂,写出吸收塔中发生反应的化学方程式:_____ ;除 外还可以选择的还原剂是
外还可以选择的还原剂是_____ (填字母)。
A. B.
B. C.
C.
(1)舍勒发现氯气的方法是实验室制取氯气(如图)的主要方法之一。

①盛装浓盐酸的仪器名称为
②装置B中饱和食盐水的作用是
③装置D中发生反应的离子方程式为
(2)含氧化合物亚氯酸钠(
 )是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
已知:纯
 易分解爆炸,一般用稀有气体或空气稀释到10%以下较安全。
易分解爆炸,一般用稀有气体或空气稀释到10%以下较安全。①
 发生器中发生反应的离子方程式为
发生器中发生反应的离子方程式为②吸收塔中为防止
 被还原成NaCl,可用还原性适中的
被还原成NaCl,可用还原性适中的 作还原剂,写出吸收塔中发生反应的化学方程式:
作还原剂,写出吸收塔中发生反应的化学方程式: 外还可以选择的还原剂是
外还可以选择的还原剂是A.
 B.
B. C.
C.
您最近一年使用:0次
解题方法
9 . 下列说法中正确的是
| A.中和反应的离子方程式均可用H++OH-=H2O来表示 |
| B.有单质参与的化学反应不一定是氧化还原反应 |
| C.物质可分为电解质和非电解质 |
| D.由同种元素组成的物质一定是纯净物 |
您最近一年使用:0次
解题方法
10 . 氧化还原反应是从元素化合价是否有变化的角度对化学反应进行分类的结果。结合你的认识完成下列题目。
(1)煤的气化是煤炭综合利用的重要途径之一,主要反应为:C+H2O CO+H2。氧化剂是
CO+H2。氧化剂是_______ (填化学式),碳元素的化合价_______ (填“升高”或“降低”)。
(2)高温下铝粉与氧化铁的反应可用来焊接钢轨。其原理是:该反应放出大量的热,置换出的铁呈熔融态。熔融的铁流入钢轨的裂缝里,冷却后就将钢轨牢牢地焊接在一起。该反应的化学方程式为_______ ,被还原的物质是_______ (填化学式,下同),被氧化的元素是_______ 。
(3)已知下列反应:Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O。被还原的HNO3与参加反应的HNO3的个数之比为_______ 。
(4)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有_______ (填“氧化性”或“还原性”)。
(5)下列各种微粒中,只具有氧化性的是_______ (填序号,下同),只具有还原性的是_______ 。
①Mg ②Cu ③Cu2+ ④H2O2 ⑤Cl- ⑥Cl2
(6)某危险品仓库中存放的化工原料氰化钠(NaCN,N元素化合价-3)有剧毒,一旦进入城市排水系统,后果不堪设想。当仓库发生火灾爆炸事故时,工作人员一方面封堵氰化钠泄漏渠道,另一方面对已经泄漏的少量氰化钠做无害化处理。下列物质中,可用于处理泄漏的氰化钠的是_______ (填序号)。
①铁粉 ②双氧水 ③臭氧(O3) ④氯化钠
(1)煤的气化是煤炭综合利用的重要途径之一,主要反应为:C+H2O
 CO+H2。氧化剂是
CO+H2。氧化剂是(2)高温下铝粉与氧化铁的反应可用来焊接钢轨。其原理是:该反应放出大量的热,置换出的铁呈熔融态。熔融的铁流入钢轨的裂缝里,冷却后就将钢轨牢牢地焊接在一起。该反应的化学方程式为
(3)已知下列反应:Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O。被还原的HNO3与参加反应的HNO3的个数之比为
(4)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有
(5)下列各种微粒中,只具有氧化性的是
①Mg ②Cu ③Cu2+ ④H2O2 ⑤Cl- ⑥Cl2
(6)某危险品仓库中存放的化工原料氰化钠(NaCN,N元素化合价-3)有剧毒,一旦进入城市排水系统,后果不堪设想。当仓库发生火灾爆炸事故时,工作人员一方面封堵氰化钠泄漏渠道,另一方面对已经泄漏的少量氰化钠做无害化处理。下列物质中,可用于处理泄漏的氰化钠的是
①铁粉 ②双氧水 ③臭氧(O3) ④氯化钠
您最近一年使用:0次



