1 . 能正确表示下列反应的离子方程式为
A.向 溶液中通入过量 溶液中通入过量 : : |
B.食醋去除水垢中的 : :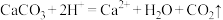 |
C.向碳酸钠溶液中通入少量 : : |
D.次磷酸(一元弱酸)与足量NaOH溶液反应: |
您最近一年使用:0次
2024-04-03更新
|
63次组卷
|
2卷引用:海南省华东师范大学第二附属中学乐东黄流中学2023-2024学年高一上学期11月期中化学试题
名校
解题方法
2 . 利用空气催化氧化法除掉电石渣浆[含Ca(OH)2]上清液中的S2-,制取石膏(CaSO4·2H2O)的过程如图:
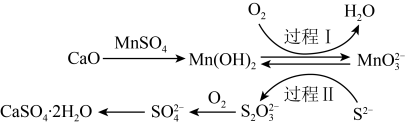
下列说法正确的是
| A.CaSO4∙2H2O属于混合物 |
| B.过程Ⅱ中,S2-为还原剂 |
| C.上述流程中,有两种元素的化合价发生变化 |
D.过程I中,反应的离子方程式为 |
您最近一年使用:0次
名校
解题方法
3 . 回答下列问题。
(1)依据物质的性质分析:CaO、Na2O、Fe2O3、CuO均属于______ (填“酸性氧化物”、“碱性氧化物”或“两性氧化物”),下列物质均能与它们发生反应的是______ (填字母)。
a.水 b.盐酸 c.氢氧化钠溶液
(2)木炭与浓硫酸发生反应: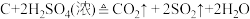 。作还原剂的物质是
。作还原剂的物质是______ ,硫元素的化合价______ (填“升高”或“降低”)。
(3)某反应中反应物与生成物的Fe3+、Mn2+、H+、 、H2O和一种未知离子X
、H2O和一种未知离子X
①已知 在反应中得到电子,则X是
在反应中得到电子,则X是______ 。
②该反应的离子方程式是______ 。
(1)依据物质的性质分析:CaO、Na2O、Fe2O3、CuO均属于
a.水 b.盐酸 c.氢氧化钠溶液
(2)木炭与浓硫酸发生反应:
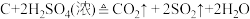 。作还原剂的物质是
。作还原剂的物质是(3)某反应中反应物与生成物的Fe3+、Mn2+、H+、
 、H2O和一种未知离子X
、H2O和一种未知离子X①已知
 在反应中得到电子,则X是
在反应中得到电子,则X是②该反应的离子方程式是
您最近一年使用:0次
解题方法
4 . 现有下列几个离子反应:① +14H++6Cl-=2Cr3++3Cl2↑+7H2O;②2Fe2++Br2=2Fe3++2Br-;③2Fe3++SO2+2H2O=2Fe2++
+14H++6Cl-=2Cr3++3Cl2↑+7H2O;②2Fe2++Br2=2Fe3++2Br-;③2Fe3++SO2+2H2O=2Fe2++ +4H+;④Cl2+2Br-=2Cl-+Br2,下列判断正确的是
+4H+;④Cl2+2Br-=2Cl-+Br2,下列判断正确的是
 +14H++6Cl-=2Cr3++3Cl2↑+7H2O;②2Fe2++Br2=2Fe3++2Br-;③2Fe3++SO2+2H2O=2Fe2++
+14H++6Cl-=2Cr3++3Cl2↑+7H2O;②2Fe2++Br2=2Fe3++2Br-;③2Fe3++SO2+2H2O=2Fe2++ +4H+;④Cl2+2Br-=2Cl-+Br2,下列判断正确的是
+4H+;④Cl2+2Br-=2Cl-+Br2,下列判断正确的是A.氧化性: >Cl2>Fe3+ >Cl2>Fe3+ |
| B.若在FeBr2溶液中通入少量Cl2,则优先发生反应④ |
| C.还原性:SO2<Fe2+<Br- |
D. 不能将Fe2+氧化为Fe3+ 不能将Fe2+氧化为Fe3+ |
您最近一年使用:0次
5 . 下列变化需要加入氧化剂才能实现的转化是
| A.浓H2SO4→SO2 | B.Br-→Br2 | C.Fe2O3→Fe | D.HCO →CO2 →CO2 |
您最近一年使用:0次
解题方法
6 . 常温下,下列各组离子在指定溶液中能大量共存的是
A.pH=13的溶液中: 、 、 、 、 、 、 |
B.在中性溶液中: 、 、 、 、 、 、 |
C.水电离出来的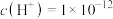 的溶液中: 的溶液中: 、 、 、 、 、 、 |
D.弱碱性溶液中可能大量存在 、 、 、 、 、 、 |
您最近一年使用:0次
7 . 下列选项中有关描述与对应图像不相符的是
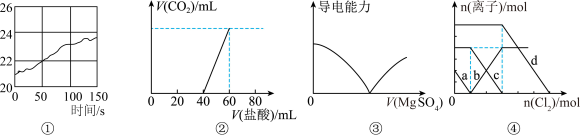

A.图①为新制氯水在阳光直射时,广口瓶内 的体积分数的变化曲线 的体积分数的变化曲线 |
B.图②为 、 、 混合液中滴加盐酸产生 混合液中滴加盐酸产生 的图像 的图像 |
C.图③为氨水溶液中滴加 溶液的导电性变化图像 溶液的导电性变化图像 |
D.图④为 、 、 混合液,各离子物质的量随 混合液,各离子物质的量随 通入的变化图像,b代表的是 通入的变化图像,b代表的是 |
您最近一年使用:0次
8 . 分析以下A-D四个涉及H2O2的反应(未配平),填空:
A.
B.
C.
D.
(1)H2O2仅体现氧化性的是_______ ;H2O2仅体现还原性的是_______ ;H2O2既体现氧化性又体现还原性的是_______ ;H2O2既不能体现氧化性又不能体现还原性的是_______ (填代号)。
(2)D反应中1分子还原剂完全反应转移电子为_______ 个。
(3)ClO2是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备: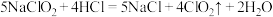 。该反应中氧化剂是
。该反应中氧化剂是_______ ,请用双线桥标明电子转移的方向和数目_______ 。
(4)海水制得的粗盐中常常含有泥沙、Ca2+、Mg2+、 等杂,粗盐提纯的步骤有:①加入过量的BaCl2溶液 ②加入过量的Na2CO3溶液 ③加入过量的NaOH溶液 ④用适量的盐酸调节溶液至中性 ⑤溶解 ⑥过滤 ⑦蒸发,正确的操作顺序是
等杂,粗盐提纯的步骤有:①加入过量的BaCl2溶液 ②加入过量的Na2CO3溶液 ③加入过量的NaOH溶液 ④用适量的盐酸调节溶液至中性 ⑤溶解 ⑥过滤 ⑦蒸发,正确的操作顺序是_______ (填选项字母)
A.⑤⑥①②③④⑥⑦ B.⑤⑥①③②⑥④⑦ C.⑤⑥②③①⑥④⑦ D.⑤⑥③①②⑥④⑦ E.⑤⑥③②①⑥④⑦
A.

B.

C.

D.

(1)H2O2仅体现氧化性的是
(2)D反应中1分子还原剂完全反应转移电子为
(3)ClO2是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备:
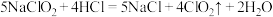 。该反应中氧化剂是
。该反应中氧化剂是(4)海水制得的粗盐中常常含有泥沙、Ca2+、Mg2+、
 等杂,粗盐提纯的步骤有:①加入过量的BaCl2溶液 ②加入过量的Na2CO3溶液 ③加入过量的NaOH溶液 ④用适量的盐酸调节溶液至中性 ⑤溶解 ⑥过滤 ⑦蒸发,正确的操作顺序是
等杂,粗盐提纯的步骤有:①加入过量的BaCl2溶液 ②加入过量的Na2CO3溶液 ③加入过量的NaOH溶液 ④用适量的盐酸调节溶液至中性 ⑤溶解 ⑥过滤 ⑦蒸发,正确的操作顺序是A.⑤⑥①②③④⑥⑦ B.⑤⑥①③②⑥④⑦ C.⑤⑥②③①⑥④⑦ D.⑤⑥③①②⑥④⑦ E.⑤⑥③②①⑥④⑦
您最近一年使用:0次
解题方法
9 . 下列转化过程需加入氧化剂的是
A.MnO →Mn2+ →Mn2+ | B.Fe3+→Fe2+ | C.Cl-→AgCl | D.SO2→SO |
您最近一年使用:0次
10 . K2FeO4是常见的水处理剂,其原理如图所示。请回答下列问题:
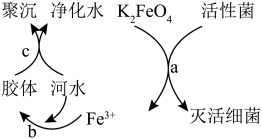
(1)高铁酸钾(K2FeO4)中铁元素的化合价为________ .
(2)过程a中K2FeO4体现________ (填“氧化”或“还原”)性,氧化产物是________ 。
(3)过程b反应的离子方程式为________ ,过程c属于________ (填“物理”或“化学”)变化。
(4)碱性条件下用Fe(OH)3和KClO反应制备K2FeO4。配平其反应的化学方程式:________ 。
Fe(OH)3+_______KOH+_______KClO=_______ K2FeO4+_______KCl+_______H2O
(5)根据以上K2FeO4净水原理,相比于Cl2,其优点是________ 。

(1)高铁酸钾(K2FeO4)中铁元素的化合价为
(2)过程a中K2FeO4体现
(3)过程b反应的离子方程式为
(4)碱性条件下用Fe(OH)3和KClO反应制备K2FeO4。配平其反应的化学方程式:
Fe(OH)3+_______KOH+_______KClO=_______ K2FeO4+_______KCl+_______H2O
(5)根据以上K2FeO4净水原理,相比于Cl2,其优点是
您最近一年使用:0次



