1 . 下列变化中需要加入还原剂才能实现的是
A. | B. |
C. | D. |
您最近半年使用:0次
解题方法
2 . 已知:① ,②
,② ,③
,③ ,根据上述反应,判断下列结论错误的是
,根据上述反应,判断下列结论错误的是
 ,②
,② ,③
,③ ,根据上述反应,判断下列结论错误的是
,根据上述反应,判断下列结论错误的是A.溶液中可发生反应 | B.还原性: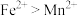 |
C.氧化性: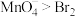 | D. 在反应①③中均为氧化剂 在反应①③中均为氧化剂 |
您最近半年使用:0次
3 . 下列类比或推理结果正确的是
A.已知 和浓硫酸可发生归中反应,则 和浓硫酸可发生归中反应,则 和硝酸也可发生归中反应 和硝酸也可发生归中反应 |
B.已知加热时Cu与 反应生成 反应生成 ,则加热时Cu与S反应生成 ,则加热时Cu与S反应生成 |
C.已知C、Si形成的氧化物晶体类型不同,可推知等物质的量的 和 和 中σ键数目不相同 中σ键数目不相同 |
D.已知氧化性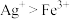 ,根据溶液中 ,根据溶液中 和 和 易发生氧化还原反应,推断溶液中 易发生氧化还原反应,推断溶液中 和 和 也易发生氧化还原反应 也易发生氧化还原反应 |
您最近半年使用:0次
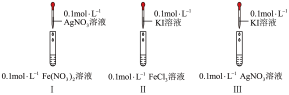
4 . 在酸性环境中,纳米Fe/Ni复合材料去除污染水体的N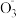 的反应过程(Ni不参与反应)如图所示,下列说法正确的是
的反应过程(Ni不参与反应)如图所示,下列说法正确的是
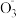 的反应过程(Ni不参与反应)如图所示,下列说法正确的是
的反应过程(Ni不参与反应)如图所示,下列说法正确的是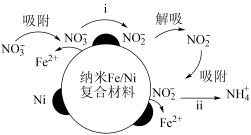
| A.反应步骤i中产生了气体 | B.反应步骤ⅱ不需要H+的参与 |
C.去除N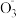 后的水体pH增大 后的水体pH增大 | D.处理过程中Fe/Ni复合材料作催化剂 |
您最近半年使用:0次
名校
5 . 一定条件下,氨气和氟气发生反应:4NH3+3F2 =NF3 +3NH4F,其中产物NF3分子结构和NH3相似。下列有关说法错误的是
| A.NF3分子含有极性共价键 | B.NF3中原子均达8电子稳定结构 |
| C.氧化剂与还原剂物质的量之比 3:4 | D.NH4F中既有离子键又有极性键 |
您最近半年使用:0次
6 . 氮是动植物生长不可缺少的元素,含氮化合物也是重要的化工原料。自然界中存在如图所示的氮元素的循环过程。下列说法正确的是

| A.过程①、③都是氮的固定 |
| B.过程①、②中氮气均被氧化 |
C.过程④反应可能是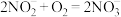 |
D.过程⑤反应可能是 |
您最近半年使用:0次
名校
7 . 某班同学用如下实验探究 、
、 的性质。(已知
的性质。(已知 遇
遇 溶液生成蓝色沉淀)回答下列问题:
溶液生成蓝色沉淀)回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 的溶液。在
的溶液。在 溶液中需加入少量铁屑,其目的是
溶液中需加入少量铁屑,其目的是___________ 。
(2)甲组同学取2mL 溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明
溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明 可将
可将 氧化。
氧化。 溶液与氯水反应的离子方程式为
溶液与氯水反应的离子方程式为___________ 。
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mL 溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是
溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是___________ 。
(4)丙组同学取10mL 0.1 KI溶液,加入6mL 0.1
KI溶液,加入6mL 0.1
 溶液混合。分别取2mL此溶液于3支试管中进行如下实验:
溶液混合。分别取2mL此溶液于3支试管中进行如下实验:
①第一支试管中加入1mL 充分振荡、静置,
充分振荡、静置, 层显紫色;
层显紫色;
②第二支试管中加入1滴 溶液,生成蓝色沉淀;
溶液,生成蓝色沉淀;
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是___________ (填离子符号);实验①和③说明:在 过量的情况下,溶液中仍含有
过量的情况下,溶液中仍含有___________ (填离子符号),由此可以证明该氧化还原反应为___________ 。
(5)丁组同学向盛有 溶液的试管中加入几滴酸化的
溶液的试管中加入几滴酸化的 溶液,溶液变成棕黄色,发生反应的离子方程式为
溶液,溶液变成棕黄色,发生反应的离子方程式为___________ 。
(6)利用如图装置探究 的稳定性。
的稳定性。___________ (填字母)。
A. 、
、 、
、
B. 、
、 、
、 、
、
C.FeO、 、
、 、
、 、
、
②III中溴水是用来检验是否有 气体生成,若有
气体生成,若有 生成,溴水将褪色。实验中,观察到溴水褪色,据此推测
生成,溴水将褪色。实验中,观察到溴水褪色,据此推测 分解最有可能被氧化的元素是
分解最有可能被氧化的元素是___________ 。
③NaOH的作用是吸收 气体,请写出用过量NaOH溶液吸收
气体,请写出用过量NaOH溶液吸收 气体的化学方程式:
气体的化学方程式:___________ 。
 、
、 的性质。(已知
的性质。(已知 遇
遇 溶液生成蓝色沉淀)回答下列问题:
溶液生成蓝色沉淀)回答下列问题:(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1
 的溶液。在
的溶液。在 溶液中需加入少量铁屑,其目的是
溶液中需加入少量铁屑,其目的是(2)甲组同学取2mL
 溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明
溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明 可将
可将 氧化。
氧化。 溶液与氯水反应的离子方程式为
溶液与氯水反应的离子方程式为(3)乙组同学认为甲组的实验不够严谨,该组同学在2mL
 溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是
溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是(4)丙组同学取10mL 0.1
 KI溶液,加入6mL 0.1
KI溶液,加入6mL 0.1
 溶液混合。分别取2mL此溶液于3支试管中进行如下实验:
溶液混合。分别取2mL此溶液于3支试管中进行如下实验:①第一支试管中加入1mL
 充分振荡、静置,
充分振荡、静置, 层显紫色;
层显紫色;②第二支试管中加入1滴
 溶液,生成蓝色沉淀;
溶液,生成蓝色沉淀;③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是
 过量的情况下,溶液中仍含有
过量的情况下,溶液中仍含有(5)丁组同学向盛有
 溶液的试管中加入几滴酸化的
溶液的试管中加入几滴酸化的 溶液,溶液变成棕黄色,发生反应的离子方程式为
溶液,溶液变成棕黄色,发生反应的离子方程式为(6)利用如图装置探究
 的稳定性。
的稳定性。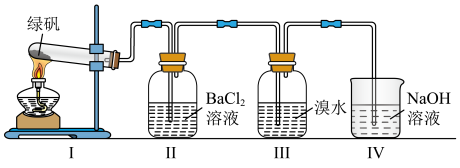
A.
 、
、 、
、
B.
 、
、 、
、 、
、
C.FeO、
 、
、 、
、 、
、
②III中溴水是用来检验是否有
 气体生成,若有
气体生成,若有 生成,溴水将褪色。实验中,观察到溴水褪色,据此推测
生成,溴水将褪色。实验中,观察到溴水褪色,据此推测 分解最有可能被氧化的元素是
分解最有可能被氧化的元素是③NaOH的作用是吸收
 气体,请写出用过量NaOH溶液吸收
气体,请写出用过量NaOH溶液吸收 气体的化学方程式:
气体的化学方程式:
您最近半年使用:0次
名校
8 . 通过如下实验,比较 、
、 、
、 的氧化性。
的氧化性。
(1)实验室 溶液通常盛放在
溶液通常盛放在___________ 试剂瓶中。
(2)Ⅱ中反应的离子方程式为___________ 。
(3)I、Ⅱ中的现象说明___________。
(4)实验后,I试管壁上的黑色沉淀可用___________洗去。
(5)写出检验I中是否含有 的方法。
的方法。___________ 。
(6)检验Ⅱ中是否含有 不可选用:___________。(不定项)
不可选用:___________。(不定项)
(7)推测Ⅲ中未发生 氧化
氧化 的原因
的原因___________ 。
 、
、 、
、 的氧化性。
的氧化性。
| 实验现象 |
I中产生黑色沉淀,滴加 溶液,变红 溶液,变红 | |
| Ⅱ中溶液呈棕黄色,滴加淀粉溶液,变蓝 | |
| Ⅲ中产生黄色沉淀,滴加淀粉溶液,未变蓝 |
(1)实验室
 溶液通常盛放在
溶液通常盛放在(2)Ⅱ中反应的离子方程式为
(3)I、Ⅱ中的现象说明___________。
A.氧化性顺序: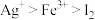 | B.氧化性顺序: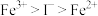 |
C.还原性顺序: | D.还原性顺序: |
(4)实验后,I试管壁上的黑色沉淀可用___________洗去。
| A.酒精 | B.二硫化碳 | C.浓硝酸 | D.热盐酸 |
(5)写出检验I中是否含有
 的方法。
的方法。(6)检验Ⅱ中是否含有
 不可选用:___________。(不定项)
不可选用:___________。(不定项)| A.氢氧化钠溶液 | B.酸性高辒酸钾溶液 | C.硫氰化钾溶液 | D.稀氨水 |
(7)推测Ⅲ中未发生
 氧化
氧化 的原因
的原因
您最近半年使用:0次
9 . 已知Ⅰ: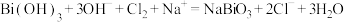 ;
;
Ⅱ.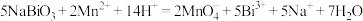 。下列推断不正确的是
。下列推断不正确的是
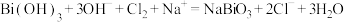 ;
;Ⅱ.
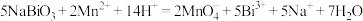 。下列推断不正确的是
。下列推断不正确的是A. 可与盐酸发生反应: 可与盐酸发生反应: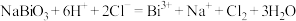 |
B.任何条件下,都存在氧化性: |
C.反应Ⅱ中,当有10.45g 生成时转移电子数为 生成时转移电子数为 |
D.已知 可由 可由 与王水(浓硝酸和浓盐酸的混合物)反应制取,说明 与王水(浓硝酸和浓盐酸的混合物)反应制取,说明 不能被硝酸氧化 不能被硝酸氧化 |
您最近半年使用:0次
名校
解题方法
10 . 如图是硫元素的“价—类”二维图:___________ 。
(2) 的浓溶液与铝单质在加热条件下可以发生化学反应生成
的浓溶液与铝单质在加热条件下可以发生化学反应生成 ,该反应的化学方程式为
,该反应的化学方程式为___________ ,可用___________ 法收集 。
。
A.向上排空气 B.向下排空气 C.排饱和食盐水 D.排饱和 溶液
溶液
(3) 和
和 均能使品红溶液褪色,但两种气体按一定比例同时通入品红溶液中无明显现象。用离子方程式解释原因
均能使品红溶液褪色,但两种气体按一定比例同时通入品红溶液中无明显现象。用离子方程式解释原因___________ 。
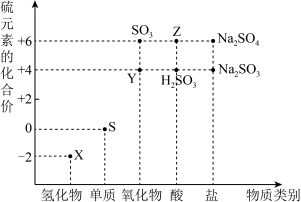
(2)
 的浓溶液与铝单质在加热条件下可以发生化学反应生成
的浓溶液与铝单质在加热条件下可以发生化学反应生成 ,该反应的化学方程式为
,该反应的化学方程式为 。
。A.向上排空气 B.向下排空气 C.排饱和食盐水 D.排饱和
 溶液
溶液(3)
 和
和 均能使品红溶液褪色,但两种气体按一定比例同时通入品红溶液中无明显现象。用离子方程式解释原因
均能使品红溶液褪色,但两种气体按一定比例同时通入品红溶液中无明显现象。用离子方程式解释原因
您最近半年使用:0次