1 . 下列粒子组在水溶液中能否共存的结论及解释完全正确的是
| 选项 | 粒子组 | 是否共存 | 解释 |
| A | 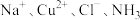 | 否 | 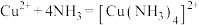 |
| B | 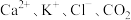 | 否 |  |
| C | 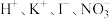 | 能 | 离子间不反应 |
| D |
| 否 |
|
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
2 . 下列反应的离子方程式书写正确的是
A.向 溶液中滴加稀 溶液中滴加稀 : :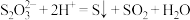 |
B.将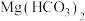 溶液长时间煮沸时形成水垢: 溶液长时间煮沸时形成水垢: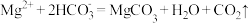 |
C.铅酸蓄电池充电时的阴极反应: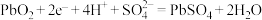 |
D.向含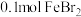 的溶液中通入 的溶液中通入 |
您最近半年使用:0次
解题方法
3 . 下列离子方程式书写正确的是
A.NaHS溶液中 的水解: 的水解: |
B.用醋酸处理水垢中的碳酸钙: |
C.向 溶液中通入等物质的量的 溶液中通入等物质的量的 : : |
D.明矾溶液与过量氨水混合: |
您最近半年使用:0次
解题方法
4 . 以碲铜废料(主要含 )为原料回收碲单质的一种工艺流程如下:
)为原料回收碲单质的一种工艺流程如下: 和二元弱酸
和二元弱酸
②
下列说法错误的是
 )为原料回收碲单质的一种工艺流程如下:
)为原料回收碲单质的一种工艺流程如下: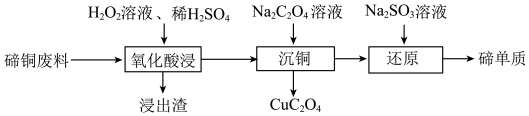
 和二元弱酸
和二元弱酸
②

下列说法错误的是
A.“氧化酸浸”时, 作氧化剂 作氧化剂 |
B.“沉铜”时,需加过量 |
C.螯合物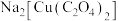 中Cu(Ⅱ)的配位数为4 中Cu(Ⅱ)的配位数为4 |
D.“还原”时,发生的主要反应为 |
您最近半年使用:0次
5 . 根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向KBrO3溶液中通入少量Cl2,然后再加入少量苯,有机相呈橙红色 | 氧化性:KBrO3>Cl2 |
| B | 用铂丝蘸取某溶液进行焰色试验,火焰呈黄色 | 溶液中一定不含有K+ |
| C | 将铁锈溶于稀盐酸,向其中滴入酸性KMnO4溶液,紫色褪去 | 铁锈中含有二价铁 |
| D | 常温下,用pH计测量0.1mol/LNaClO溶液的pH | 若pH>7,说明HClO是弱酸 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
6 . 下列各组粒子在溶液中能大量共存,且在加入试剂X后,发生反应的离子方程式正确的是
| 选项 | 粒子 | 试剂X | 发生的离子反应 |
| A |  | 少量醋酸 |  |
| B |  | 少量硫化钠 |  |
| C |  | 少量纯碱 |  |
| D | 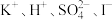 | 少量氧化铁 |  |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
7 . 某研究小组在进行完银镜反应后清洗试管时误将 溶液当浓硝酸倒入试管中,发现银镜会消失。
溶液当浓硝酸倒入试管中,发现银镜会消失。
Ⅰ.提出猜想 猜想一: 氧化了Ag
氧化了Ag
猜想二:酸性条件下 氧化了Ag
氧化了Ag
猜想三:酸性条件下 与
与 同时氧化了Ag
同时氧化了Ag
验证猜想
(1)向反应后的试管中滴加___________ 溶液(填化学式)溶液未出现蓝色沉淀,说明猜想一、三不成立。
提出疑问
(2)验证猜想的实验证据不充分,原因是:___________ 。
Ⅱ.重新设计实验探究:
(3)配制 溶液,下列配制过程说法错误的有:___________。
溶液,下列配制过程说法错误的有:___________。
(4)取一支沾有少量Ag的试管,加入 溶液(过量),充分振荡,发现银镜消失较慢,溶液黄色明显变浅,产生较多白色沉淀。
溶液(过量),充分振荡,发现银镜消失较慢,溶液黄色明显变浅,产生较多白色沉淀。
①选用 溶液的目的是
溶液的目的是___________ 。
②根据实验现象写出实验中的离子方程式___________ 。
结论 具有氧化性,能够溶解单质Ag。
具有氧化性,能够溶解单质Ag。
(5)在(4)实验方案基础上进一步设计了如下列实验方案:
本实验目的为___________ ,根据实验目的可以判断出步骤c中的试剂A为___________ (注明离子浓度及pH值)。
(6)查阅资料发现, 、
、 的氧化性差异不大,推测在一定条件下Ag与
的氧化性差异不大,推测在一定条件下Ag与 反应可能是可逆反应,改用如下图所示装置进行探究,连接装置(盐桥中的物质不参与反应),进行下表中实验操作并记录电流表读数。
反应可能是可逆反应,改用如下图所示装置进行探究,连接装置(盐桥中的物质不参与反应),进行下表中实验操作并记录电流表读数。
根据步骤C中电流表读数x___________ 0(填“大于”、“小于”、“等于”),确定Ag与 反应是可逆反应。综合上述实验写出
反应是可逆反应。综合上述实验写出 和
和 反应的离子方程式
反应的离子方程式___________ 。
 溶液当浓硝酸倒入试管中,发现银镜会消失。
溶液当浓硝酸倒入试管中,发现银镜会消失。Ⅰ.提出猜想 猜想一:
 氧化了Ag
氧化了Ag猜想二:酸性条件下
 氧化了Ag
氧化了Ag猜想三:酸性条件下
 与
与 同时氧化了Ag
同时氧化了Ag验证猜想
(1)向反应后的试管中滴加
提出疑问
(2)验证猜想的实验证据不充分,原因是:
Ⅱ.重新设计实验探究:
(3)配制
 溶液,下列配制过程说法错误的有:___________。
溶液,下列配制过程说法错误的有:___________。A.计算 需要4.0g,将固体置于滤纸上称量后转移到烧杯中溶解 需要4.0g,将固体置于滤纸上称量后转移到烧杯中溶解 |
| B.将溶解后冷却至室温的溶液转移到容量瓶中 |
| C.加水到离刻度线1~2cm时改用胶头滴管滴加至刻度线 |
| D.盖好瓶塞并旋紧,左右摇动瓶身混均后,贴上标签待用 |
 溶液(过量),充分振荡,发现银镜消失较慢,溶液黄色明显变浅,产生较多白色沉淀。
溶液(过量),充分振荡,发现银镜消失较慢,溶液黄色明显变浅,产生较多白色沉淀。①选用
 溶液的目的是
溶液的目的是②根据实验现象写出实验中的离子方程式
结论
 具有氧化性,能够溶解单质Ag。
具有氧化性,能够溶解单质Ag。(5)在(4)实验方案基础上进一步设计了如下列实验方案:
| 序号 | 实验步骤 | 实验现象 |
| a | 用pH计测定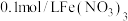 的pH 的pH | pH=2.00 |
| b | 取一支沾有少量Ag的试管,加入 溶液(过量),充分振荡 溶液(过量),充分振荡 | 银镜消失较快;溶液黄色略变浅 |
| c | 取一支沾有少量Ag的试管,加入试剂A,充分振荡 | 银镜消失较快 |
(6)查阅资料发现,
 、
、 的氧化性差异不大,推测在一定条件下Ag与
的氧化性差异不大,推测在一定条件下Ag与 反应可能是可逆反应,改用如下图所示装置进行探究,连接装置(盐桥中的物质不参与反应),进行下表中实验操作并记录电流表读数。
反应可能是可逆反应,改用如下图所示装置进行探究,连接装置(盐桥中的物质不参与反应),进行下表中实验操作并记录电流表读数。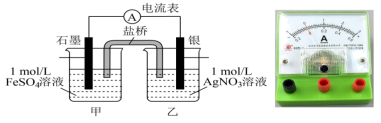
| 序号 | 实验步骤 | 电流表读数(A) |
| A | 按上图连接装置并加入药品,电流表指针偏转,发现银电极质量有增加,读出电流表读数a | a(a>0) |
| B | 充分反应一段时间后,读出电流表读数b | b=0 |
| C | 再继续向烧杯甲中缓缓加入 固体,读出电流表读数x 固体,读出电流表读数x | x |
 反应是可逆反应。综合上述实验写出
反应是可逆反应。综合上述实验写出 和
和 反应的离子方程式
反应的离子方程式
您最近半年使用:0次
解题方法
8 . 利用CoP/CdS复合光催化剂可实现温和条件下废弃聚乳酸塑料(PLA)高选择性地转化为丙氨酸小分子,其转化历程如下:

| A.该过程光能转化为化学能 |
| B.每生成1mol丙氨酸,催化剂吸收2.41eV的能量 |
| C.乳酸铵转化为丙酮酸主要发生氧化反应 |
D.PLA转化为乳酰胺的化学方程式为: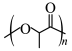 +nNH3 +nNH3 H2O H2O n n +nH2O +nH2O |
您最近半年使用:0次
名校
9 . 利用废电池材料 (含炭黑及少量
(含炭黑及少量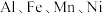 等元素)回收金属资源的工艺流程如下:
等元素)回收金属资源的工艺流程如下: 如下表:
如下表:
②电极电位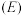 表示溶液中某微粒获得电子被还原的趋势(即氧化性);如电极反应
表示溶液中某微粒获得电子被还原的趋势(即氧化性);如电极反应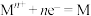 的
的 越大,表示
越大,表示 的氧化性越强。
的氧化性越强。
酸性条件: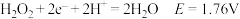 ;
;
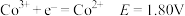
碱性条件: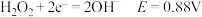 ;
;
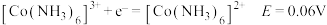
③丁二酮肟是不溶于水的固体,溶于乙醇后可与 反应生成丁二酮肟镍。
反应生成丁二酮肟镍。 转化后的钴离子价电子排布式为
转化后的钴离子价电子排布式为______ ,滤渣1为______ 。
(2)“氧化调 "中,
"中, 转化为
转化为 ,滤渣2中还有
,滤渣2中还有______ ,调节 范围为
范围为______ 。
(3)“转化”时,加入浓氨水将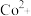 转化为
转化为 的原因是
的原因是______ ,加 目的是
目的是______ 。
(4)“沉镍”后,从滤渣3中回收丁二酮肟固体的操作是______ 。
(5)由 溶液制备催化剂
溶液制备催化剂 的步骤为:第一步加入尿素
的步骤为:第一步加入尿素 生成
生成 沉淀(有
沉淀(有 气体产生),第二步焙烧得到
气体产生),第二步焙烧得到 。写出第一步的离子方程式
。写出第一步的离子方程式______ 。
(6)由 制备得一种锂离子电池材料
制备得一种锂离子电池材料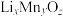 ,其晶胞分别由4个
,其晶胞分别由4个 个
个 立方单元构成。则
立方单元构成。则
______ 。
 (含炭黑及少量
(含炭黑及少量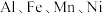 等元素)回收金属资源的工艺流程如下:
等元素)回收金属资源的工艺流程如下:
 如下表:
如下表:氢氧化物 |
|
|
|
|
完全沉淀 | 9.2 | 1.3 | 4.7 | 3.1 |
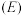 表示溶液中某微粒获得电子被还原的趋势(即氧化性);如电极反应
表示溶液中某微粒获得电子被还原的趋势(即氧化性);如电极反应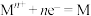 的
的 越大,表示
越大,表示 的氧化性越强。
的氧化性越强。酸性条件:
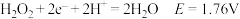 ;
;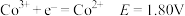
碱性条件:
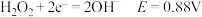 ;
;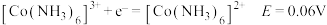
③丁二酮肟是不溶于水的固体,溶于乙醇后可与
 反应生成丁二酮肟镍。
反应生成丁二酮肟镍。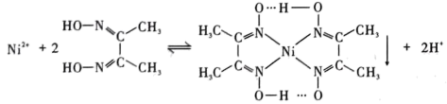
 转化后的钴离子价电子排布式为
转化后的钴离子价电子排布式为(2)“氧化调
 "中,
"中, 转化为
转化为 ,滤渣2中还有
,滤渣2中还有 范围为
范围为(3)“转化”时,加入浓氨水将
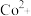 转化为
转化为 的原因是
的原因是 目的是
目的是(4)“沉镍”后,从滤渣3中回收丁二酮肟固体的操作是
(5)由
 溶液制备催化剂
溶液制备催化剂 的步骤为:第一步加入尿素
的步骤为:第一步加入尿素 生成
生成 沉淀(有
沉淀(有 气体产生),第二步焙烧得到
气体产生),第二步焙烧得到 。写出第一步的离子方程式
。写出第一步的离子方程式(6)由
 制备得一种锂离子电池材料
制备得一种锂离子电池材料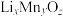 ,其晶胞分别由4个
,其晶胞分别由4个 个
个 立方单元构成。则
立方单元构成。则

您最近半年使用:0次
10 . 锂电池的研发、使用及废电池的回收具有重要意义。
(1)比能量是指电池单位质量(或体积)输出的电能。锂金属电池放电时总反应为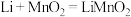 。下列关于锂金属电池说法正确的是
。下列关于锂金属电池说法正确的是___________ (填序号)。
A放电时Li作负极 B.比能量高于锌锰干电池 C.可用稀 作电解质
作电解质
(2)钴酸锂( )、磷酸铁锂(
)、磷酸铁锂( )等锂离子二次电池应用普遍。
)等锂离子二次电池应用普遍。
①钴酸锂电池放电时示意图如图1所示。放电时, 由
由 中脱嵌。写出放电至完全时
中脱嵌。写出放电至完全时 电极的电极反应式:
电极的电极反应式:___________ 。 脱嵌形成
脱嵌形成 。
。 晶胞中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构(如图2所示)。x=
晶胞中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构(如图2所示)。x=___________ 。 和NaCl溶液中使电池充分放电是电池回收工艺的首要步骤。电池在不同溶液中放电的残余电压随时间的变化如图3所示。对浸泡液中沉淀物热处理后,得到XRD示意图谱如图4所示。
和NaCl溶液中使电池充分放电是电池回收工艺的首要步骤。电池在不同溶液中放电的残余电压随时间的变化如图3所示。对浸泡液中沉淀物热处理后,得到XRD示意图谱如图4所示。___________ 。
②与 溶液相比,NaCl溶液的质量分数由5%增大至10%时,电池残余电压降低速率更快。依据图4XRD图谱,分析其主要原因:
溶液相比,NaCl溶液的质量分数由5%增大至10%时,电池残余电压降低速率更快。依据图4XRD图谱,分析其主要原因:___________ 。
(4)将放电完全的钴酸锂电池正极材料粉碎后进行酸浸处理。实验测得,在相同条件下,使用盐酸作浸取剂可使钴转化为 ,转化率达到99%,但工业生产使用
,转化率达到99%,但工业生产使用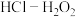 混合物作浸取剂。
混合物作浸取剂。
①写出盐酸作浸取剂发生酸浸反应的化学反应方程式:___________ 。
②工业生产时在盐酸中加入 ,
, 的作用是
的作用是___________ 。
(1)比能量是指电池单位质量(或体积)输出的电能。锂金属电池放电时总反应为
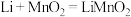 。下列关于锂金属电池说法正确的是
。下列关于锂金属电池说法正确的是A放电时Li作负极 B.比能量高于锌锰干电池 C.可用稀
 作电解质
作电解质(2)钴酸锂(
 )、磷酸铁锂(
)、磷酸铁锂( )等锂离子二次电池应用普遍。
)等锂离子二次电池应用普遍。①钴酸锂电池放电时示意图如图1所示。放电时,
 由
由 中脱嵌。写出放电至完全时
中脱嵌。写出放电至完全时 电极的电极反应式:
电极的电极反应式: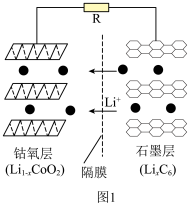
 脱嵌形成
脱嵌形成 。
。 晶胞中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构(如图2所示)。x=
晶胞中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构(如图2所示)。x=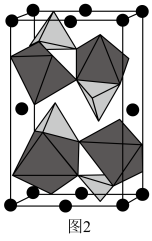
 和NaCl溶液中使电池充分放电是电池回收工艺的首要步骤。电池在不同溶液中放电的残余电压随时间的变化如图3所示。对浸泡液中沉淀物热处理后,得到XRD示意图谱如图4所示。
和NaCl溶液中使电池充分放电是电池回收工艺的首要步骤。电池在不同溶液中放电的残余电压随时间的变化如图3所示。对浸泡液中沉淀物热处理后,得到XRD示意图谱如图4所示。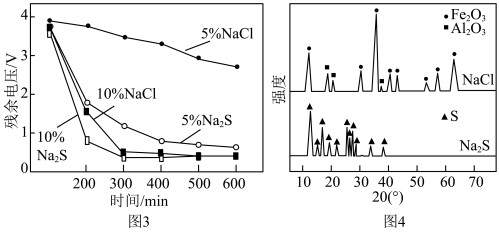
②与
 溶液相比,NaCl溶液的质量分数由5%增大至10%时,电池残余电压降低速率更快。依据图4XRD图谱,分析其主要原因:
溶液相比,NaCl溶液的质量分数由5%增大至10%时,电池残余电压降低速率更快。依据图4XRD图谱,分析其主要原因:(4)将放电完全的钴酸锂电池正极材料粉碎后进行酸浸处理。实验测得,在相同条件下,使用盐酸作浸取剂可使钴转化为
 ,转化率达到99%,但工业生产使用
,转化率达到99%,但工业生产使用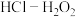 混合物作浸取剂。
混合物作浸取剂。①写出盐酸作浸取剂发生酸浸反应的化学反应方程式:
②工业生产时在盐酸中加入
 ,
, 的作用是
的作用是
您最近半年使用:0次

 、
、 、
、 、
、
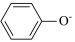 +
+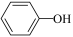 +
+






