名校
1 . 实验室制备顺式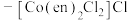 配合物流程如图所示。已知:反式
配合物流程如图所示。已知:反式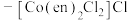 为绿色晶体,顺式
为绿色晶体,顺式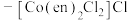 为紫黑色晶体,均易溶于热水,微溶于冷水,难溶于乙醇;
为紫黑色晶体,均易溶于热水,微溶于冷水,难溶于乙醇;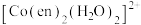 、
、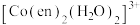 均呈深红色;乙二胺(H2NCH2CH2NH2)用en表示,配离子参与的反应为可逆反应。
均呈深红色;乙二胺(H2NCH2CH2NH2)用en表示,配离子参与的反应为可逆反应。
 值越大,电对中氧化型物质的氧化能力越强
值越大,电对中氧化型物质的氧化能力越强
下列说法错误的是
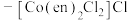 配合物流程如图所示。已知:反式
配合物流程如图所示。已知:反式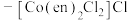 为绿色晶体,顺式
为绿色晶体,顺式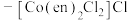 为紫黑色晶体,均易溶于热水,微溶于冷水,难溶于乙醇;
为紫黑色晶体,均易溶于热水,微溶于冷水,难溶于乙醇;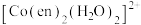 、
、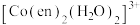 均呈深红色;乙二胺(H2NCH2CH2NH2)用en表示,配离子参与的反应为可逆反应。
均呈深红色;乙二胺(H2NCH2CH2NH2)用en表示,配离子参与的反应为可逆反应。
| 电极反应 | 电极电位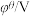 |
 | 1.84 |
 | 0.10 |
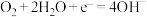 | 0.41 |
 | 0.88 |
 值越大,电对中氧化型物质的氧化能力越强
值越大,电对中氧化型物质的氧化能力越强下列说法错误的是
| A.方案一中加“试剂X”与“空气中搅拌20 min”两个步骤可调换顺序 |
| B.试剂Y可选用双氧水 |
| C.可以使用NaCl代替盐酸 |
D.顺式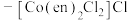 热稳定性强于反式 热稳定性强于反式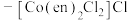 |
您最近一年使用:0次
2024-05-29更新
|
120次组卷
|
2卷引用:2024届山东省日照市五莲县第一中学高三下学期模拟预测化学试题
名校
2 . 物质类别和元素价态是学习元素及其化合物性质的重要认识视角。部分含N及Cl物质的分类与相应化合价关系如图所示,下列推断合理的是
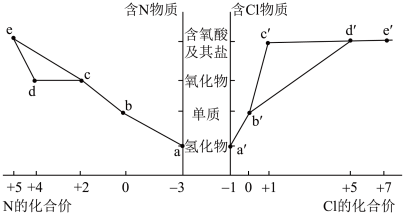
| A.a和e反应一定能得到b |
B.工业上通过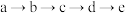 来制备 来制备 |
C.e中 的杂化方式与e′中 的杂化方式与e′中 的杂化方式相同 的杂化方式相同 |
| D.浓a′溶液和浓c′溶液反应可以得到b′ |
您最近一年使用:0次
3 . 在溶液中能大量共存的离子组是
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、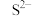 | D. 、 、 、 、 、 、 |
您最近一年使用:0次
4 . 纯净物状态下的标准电极电势可用来比较对应氧化剂的氧化性强弱。现有六组标准电极电势数据如表所示:
下列分析正确的是
氧化还原电对(氧化型/还原型) | 电极反应式 | 标准电极电势 |
|
| 0.77 |
|
| 0.54 |
|
| 1.50 |
|
| 1.07 |
|
| 1.36 |
|
| 0.15 |
A.氧化性: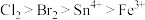 |
B.往含有 的 的 溶液中滴加少量氯水,溶液变红 溶液中滴加少量氯水,溶液变红 |
C.往淀粉- 溶液中加入过量 溶液中加入过量 溶液,溶液变蓝 溶液,溶液变蓝 |
D. 溶液与足量酸性 溶液与足量酸性 溶液反应的离子方程式: 溶液反应的离子方程式: |
您最近一年使用:0次
2024-05-20更新
|
316次组卷
|
2卷引用:湖南省新高考教学教研联盟2023-2024学年高三下学期第二次联考化学试题
5 . 由辉铜矿(含 ,少量
,少量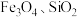 )合成
)合成 的流程如下。
的流程如下。 时,
时, ,
,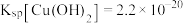 ,离子浓度
,离子浓度 时可认为离子完全沉淀。下列说法正确的是
时可认为离子完全沉淀。下列说法正确的是
 ,少量
,少量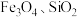 )合成
)合成 的流程如下。
的流程如下。
 时,
时, ,
,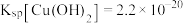 ,离子浓度
,离子浓度 时可认为离子完全沉淀。下列说法正确的是
时可认为离子完全沉淀。下列说法正确的是A.煅烧时只有 两种元素被氧化 两种元素被氧化 |
B.酸浸后,滤液的主要成分为 和 和 |
C.调 为 为 时,可实现铜、铁的分离 时,可实现铜、铁的分离 |
D. 乙醇的作用为增大 乙醇的作用为增大 的溶解度 的溶解度 |
您最近一年使用:0次
6 . 在含 (过二硫酸根)和
(过二硫酸根)和 的溶液中,发生反应:
的溶液中,发生反应: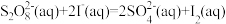 ,其分解机理及反应过程中的能量变化如图所示:
,其分解机理及反应过程中的能量变化如图所示:
 (过二硫酸根)和
(过二硫酸根)和 的溶液中,发生反应:
的溶液中,发生反应: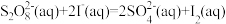 ,其分解机理及反应过程中的能量变化如图所示:
,其分解机理及反应过程中的能量变化如图所示:
| A.步骤②决定总反应的速率 |
| B.步骤①是吸热过程,步骤②是放热过程 |
C.由反应机理可以看出, 是中间产物 是中间产物 |
| D.反应中S元素不参与电子转移 |
您最近一年使用:0次
7 . 下列粒子组在水溶液中能否共存的结论及解释完全正确的是
| 选项 | 粒子组 | 是否共存 | 解释 |
| A | 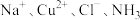 | 否 | 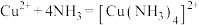 |
| B | 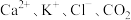 | 否 |  |
| C | 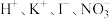 | 能 | 离子间不反应 |
| D |
| 否 |
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . NH4NO3受撞击时会发生爆炸: 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A. 溶液中含 溶液中含 数目为 数目为 |
B.1molN2中含 键数目为 键数目为 |
C.标准状况下,22.4LH2O中含电子数为 |
D.每生成0.2molNO2,该反应中转移电子数为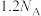 |
您最近一年使用:0次
名校
9 . 标准电极电位指离子有效浓度为1mol/L时相对标准氢电极的电极电位差值,电对的标准电极电势 越高,其电对中氧化剂的氧化性越强。酸性介质中,以下电对的标准电极电势为:①
越高,其电对中氧化剂的氧化性越强。酸性介质中,以下电对的标准电极电势为:①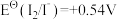 ;②
;②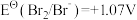 ;③
;③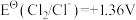 ;④
;④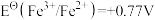 ;⑤
;⑤ ;⑥
;⑥ 。下列有关说法正确的是
。下列有关说法正确的是
 越高,其电对中氧化剂的氧化性越强。酸性介质中,以下电对的标准电极电势为:①
越高,其电对中氧化剂的氧化性越强。酸性介质中,以下电对的标准电极电势为:①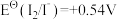 ;②
;②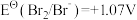 ;③
;③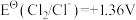 ;④
;④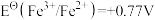 ;⑤
;⑤ ;⑥
;⑥ 。下列有关说法正确的是
。下列有关说法正确的是A.向1mol/L的HBr溶液中滴加 溶液,无明显现象发生 溶液,无明显现象发生 |
B.2mol/L的 与2mol/L的稀盐酸等体积混合有大量 与2mol/L的稀盐酸等体积混合有大量 产生 产生 |
C.在含 、 、 、 、 的混合溶液中若仅氧化 的混合溶液中若仅氧化 ,最佳的氧化剂是 ,最佳的氧化剂是 |
D.浓度相等时,还原性: |
您最近一年使用:0次
名校
解题方法
10 . 我国的钴(Co)资源非常贫乏,一种利用湿法炼锌净化渣回收钴的工艺如下图所示。已知净化渣含有较高的锌、铜、铅、钴元素以及一定量的铁和锰元素,它们大多以金属单质和氧化物的形式存在。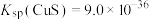 ,
, ,
, 。
。
② 在酸性溶液中有强氧化性
在酸性溶液中有强氧化性
(1)“常压浸出”需加热至70℃左右,宜采用___________ (填序号;①盐酸②硫酸③硝酸)进行酸浸,浸出渣主要成分为___________ 。
(2)大多数金属硫化物都难溶于水,能选择 除铜的原因是
除铜的原因是___________ ,若加入 后溶液中
后溶液中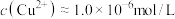 ,
,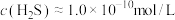 ,则溶液的pH约为
,则溶液的pH约为___________ 。
(3)过二硫酸钠( )氧化Mn2+生成MnO2沉淀,同时生成
)氧化Mn2+生成MnO2沉淀,同时生成 ,请写出该反应的离子方程式:
,请写出该反应的离子方程式:___________ 。
(4)根据流程可知:在“沉淀分离”步骤中,还原性Co2+___________ Mn2+(填“强于”或“弱于”);氧化沉淀所得产物为Co(OH)3,最终钴产品是Co(OH)3脱水后的产物,脱水前后质量比为55:46,则钴产品的化学式为___________ 。

 ,
, ,
, 。
。②
 在酸性溶液中有强氧化性
在酸性溶液中有强氧化性(1)“常压浸出”需加热至70℃左右,宜采用
(2)大多数金属硫化物都难溶于水,能选择
 除铜的原因是
除铜的原因是 后溶液中
后溶液中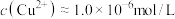 ,
,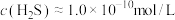 ,则溶液的pH约为
,则溶液的pH约为(3)过二硫酸钠(
 )氧化Mn2+生成MnO2沉淀,同时生成
)氧化Mn2+生成MnO2沉淀,同时生成 ,请写出该反应的离子方程式:
,请写出该反应的离子方程式:(4)根据流程可知:在“沉淀分离”步骤中,还原性Co2+
您最近一年使用:0次

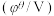

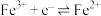


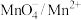
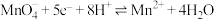
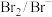
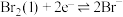
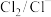
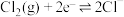
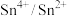

 、
、 、
、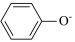 +
+ +
+


