名校
1 . 下列指定反应的离子方程式正确的是
| A.Ca(NO3)2溶液中通入少量CO2:Ca2++CO2+H2O=CaCO3↓+2H+ |
| B.KI溶液中加入少量已酸化的双氧水:2H++2I-+H2O2=I2+O2↑+2H2O |
| C.向AgNO3溶液滴入氨水至沉淀刚好消失:Ag++2NH3·H2O=[Ag(NH3)2]++OH- |
D.Ba(OH)2溶液中加少量NaHCO3溶液:Ba2++OH-+HCO =BaCO3↓+H2O =BaCO3↓+H2O |
您最近一年使用:0次
2 . 在浓盐酸中H3AsO3与SnCl2反应的离子方程式为:3SnCl2 + 12Cl-+ 2H3AsO3 + 6H+=2As + 3SnCl + 6M。关于该反应的说法中正确的组合是
+ 6M。关于该反应的说法中正确的组合是
①氧化剂是H3AsO3 ②每生成1molAs,反应中转移电子的物质的量为3 mol
③还原性:Cl-> As ④M为OH- ⑤SnCl 是氧化产物
是氧化产物
 + 6M。关于该反应的说法中正确的组合是
+ 6M。关于该反应的说法中正确的组合是 ①氧化剂是H3AsO3 ②每生成1molAs,反应中转移电子的物质的量为3 mol
③还原性:Cl-> As ④M为OH- ⑤SnCl
 是氧化产物
是氧化产物| A.①②⑤ | B.①③④⑤ | C.①②③④ | D.只有①② |
您最近一年使用:0次
3 . 已知以下四个反应:
①4HCl(浓)+MnO2 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
②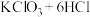 (浓)
(浓)
③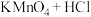 (浓)
(浓)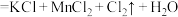 (未配平)
(未配平)
④
根据以上四个反应,回答下列有关问题:
(1)反应①中,氧化产物与还原产物的质量比为___________ 。(写最简整数比)
(2)反应②中氧化剂与还原剂的个数之比为___________ 。(写最简整数比)
(3)若要制得相同质量的氯气,①②反应中电子转移的数目之比为_______ 。(写最简整数比)
(4)请将反应③配平:
 (浓)=
(浓)=



________
(5)请用单线桥表示反应④的电子转移情况:
__________
(6)将 ,
, ,
, 按由强到弱的氧化性顺序排序
按由强到弱的氧化性顺序排序___________ 。(例A>B>C)
①4HCl(浓)+MnO2
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O②
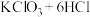 (浓)
(浓)
③
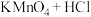 (浓)
(浓)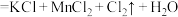 (未配平)
(未配平)④

根据以上四个反应,回答下列有关问题:
(1)反应①中,氧化产物与还原产物的质量比为
(2)反应②中氧化剂与还原剂的个数之比为
(3)若要制得相同质量的氯气,①②反应中电子转移的数目之比为
(4)请将反应③配平:

 (浓)=
(浓)=



(5)请用单线桥表示反应④的电子转移情况:

(6)将
 ,
, ,
, 按由强到弱的氧化性顺序排序
按由强到弱的氧化性顺序排序
您最近一年使用:0次
4 . 回答下列问题:
(1)请配平以下的氧化还原方程式:。
①□ □
□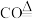 □
□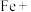 □
□
______
②□ □
□ □
□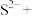 □
□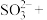 □
□
______
③□ □
□ □_______=□
□_______=□ □
□ □
□ (缺了一种反应物)
(缺了一种反应物)________
(2)已知还原性强弱顺序是 ,向含有
,向含有 、
、 、
、 的溶液中通入氯气,先被氧化的离子是
的溶液中通入氯气,先被氧化的离子是___________ 。
(3)高铁酸钠(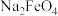 )被公认为绿色净水剂,比
)被公认为绿色净水剂,比 、
、 ,
, 氧化性更强,无二次污染:
氧化性更强,无二次污染:
①干法制备高铁酸钠的主要反应为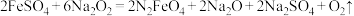 ,该反应中的氧化剂为
,该反应中的氧化剂为___________ ,氧化产物为___________ 。
②除了干法制备高铁酸钠,还可用湿法制备高铁酸钠,其反应物和生成物共有七种微粒: 、
、 、
、 、
、 、
、 、
、 、
、 ,写出该反应的离子方程式:
,写出该反应的离子方程式:___________ 。
(1)请配平以下的氧化还原方程式:。
①□
 □
□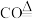 □
□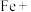 □
□
②□
 □
□ □
□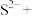 □
□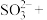 □
□
③□
 □
□ □_______=□
□_______=□ □
□ □
□ (缺了一种反应物)
(缺了一种反应物)(2)已知还原性强弱顺序是
 ,向含有
,向含有 、
、 、
、 的溶液中通入氯气,先被氧化的离子是
的溶液中通入氯气,先被氧化的离子是(3)高铁酸钠(
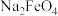 )被公认为绿色净水剂,比
)被公认为绿色净水剂,比 、
、 ,
, 氧化性更强,无二次污染:
氧化性更强,无二次污染:①干法制备高铁酸钠的主要反应为
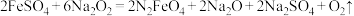 ,该反应中的氧化剂为
,该反应中的氧化剂为②除了干法制备高铁酸钠,还可用湿法制备高铁酸钠,其反应物和生成物共有七种微粒:
 、
、 、
、 、
、 、
、 、
、 、
、 ,写出该反应的离子方程式:
,写出该反应的离子方程式:
您最近一年使用:0次
2021-10-24更新
|
1543次组卷
|
2卷引用:重庆西南大学附属中学校2021-2022学年高一上学期第二次测试化学试题
名校
解题方法
5 . 我国四大发明之一的黑火药是由硫磺粉、 和木炭粉按一定比例混合而成的,爆炸时的反应为:
和木炭粉按一定比例混合而成的,爆炸时的反应为: 。下列说法正确的是
。下列说法正确的是
 和木炭粉按一定比例混合而成的,爆炸时的反应为:
和木炭粉按一定比例混合而成的,爆炸时的反应为: 。下列说法正确的是
。下列说法正确的是A.生成物中只有 是还原产物 是还原产物 |
| B.用双线桥表示该反应中的电子转移总数目为10e- |
| C.该反应为离子反应 |
| D.该反应中只有C作还原剂 |
您最近一年使用:0次
2021-10-24更新
|
166次组卷
|
2卷引用:重庆西南大学附属中学校2021-2022学年高一上学期第二次测试化学试题
名校
解题方法
6 . 下列变化需要加入氧化剂才能实现的是
A. | B.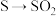 | C. | D. |
您最近一年使用:0次
2021-10-24更新
|
142次组卷
|
2卷引用:重庆西南大学附属中学校2021-2022学年高一上学期第二次测试化学试题
名校
解题方法
7 . 下列关于氧化还原反应的叙述中,正确的是
| A.还原剂在反应过程中化合价升高 |
| B.氧化还原反应的本质是元素化合价发生了变化 |
| C.一种元素被氧化,必定有另一种元素被还原 |
| D.氧化还原反应中,生成物不是氧化产物就是还原产物 |
您最近一年使用:0次
名校
解题方法
8 . 下列应用不涉及氧化还原反应的是
| A.小苏打用作食品膨松剂 |
| B.工业合成氨实现人工固氮 |
| C.烟气脱硫(SO2)生产硫酸 |
| D.利用铝热反应焊接钢轨 |
您最近一年使用:0次
2021-03-18更新
|
964次组卷
|
9卷引用:重庆市西南大学附中2020-2021学年高三下学期第四次月考化学试题
重庆市西南大学附中2020-2021学年高三下学期第四次月考化学试题广东省广州市2021届高三3月第一次模拟考试化学试题广东省广州市2021届高三下学期毕业班综合测试(一)化学试题广东省中山市卓雅外国语学校2020-2021学年高二下学期第一次段考化学试题广东省广州市番禺区洛溪新城中学2020-2021学年高一下学4月月考化学试题(已下线)押山东卷第02题 氧化还原反应在生产生活中的应用-备战2021年高考化学临考题号押题(山东卷)(已下线)第9周 周测卷-备战2022年高考化学周测与晚练(新高考专用)广东省深圳市第七高级中学2022届高三上学期9月月考化学试题广东省深圳市第七高级中学2022届高三第二次月考化学试题
9 . 如图表示Fe与不同的浓度硝酸反应时,各种还原产物的相对含量与硝酸溶液浓度的关系。

下列说法正确的是

下列说法正确的是
| A.硝酸浓度越大,还原产物总类越多 |
| B.根据还原产物的化合价可推知硝酸浓度越低氧化性越强 |
C.若c(HNO3)=9.75mol/L,生成还原产物总量为1mol时,转移电子的物质的量为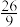 mol mol |
D.当HNO3浓度为12.2mol/L时,Fe与足量的HNO3反应的离子方程式为:2Fe+6H++2NO =2Fe2+++NO2↑+NO↑+3H2O =2Fe2+++NO2↑+NO↑+3H2O |
您最近一年使用:0次
2020-12-23更新
|
481次组卷
|
5卷引用:重庆市西南大学附属中学校高2021届高三第二次月考化学试题
重庆市西南大学附属中学校高2021届高三第二次月考化学试题山东省滨州市2021届高三上学期期末考试化学试题山东省威海乳山市银滩高级中学2022-2023学年高三9月月考化学试题(已下线)T12-化学反应及限度(已下线)选择题6-10
名校
10 . 已知X2、Y2、Z2、W2四种物质的氧化能力为:W2>Z2>X2>Y2,下列氧化还原反应能发生的是
| A.2W- + Z2 = 2Z- +W2 | B.2X- + Y2 = 2Y- + X2 |
| C.2Y- + W2 = 2W- + Y2 | D.2Z- + X2 = 2X- + Z2 |
您最近一年使用:0次
2020-07-09更新
|
126次组卷
|
11卷引用:重庆西南大学附属中学校2021-2022学年高一上学期第二次测试化学试题
重庆西南大学附属中学校2021-2022学年高一上学期第二次测试化学试题2015-2016学年山西大学附属中学高一上期中化学试卷2015-2016学年湖南常德石门第一中学高一上期中化学试卷山西省晋中市平遥县第二中学2018-2019学年高一上学期12月月考化学试题安徽省六安市霍邱县第二中学2019-2020学年高一上学期段考化学试题山西省晋中市平遥县第二中学2019-2020学年高一12月月考化学试题云南省昆明市昆明第八中学2019-2020学年高一上学期期中考试化学试题甘肃省静宁县第一中学2019-2020学年高一上学期期末考试化学试题新疆生产建设兵团第十师北屯高级中学2020-2021学年高一上学期阶段性检测化学试题宁夏回族自治区银川市六盘山市高级中学2020-2021学年高一上学期第二次月考化学试题(已下线)【新东方】化学出门测1234



