名校
解题方法
1 . 汽车尾气系统中均安装了催化转化器。在催化转化器中,汽车尾气中的CO和NO在催化剂高温条件下发生反应,生成两种无毒气体。下列说法错误的是
A.上述反应的化学方程式为 |
| B.氧化产物与还原产物的分子数之比为2∶1 |
| C.催化转化过程中NO中的N元素被氧化 |
| D.将CO和NO转化为无毒物质,从而减少了汽车尾气排放所造成的空气污染 |
您最近半年使用:0次
2023-07-05更新
|
346次组卷
|
5卷引用:重庆市西南大学附属中学2022-2023学年高一上学期期中考试化学试题
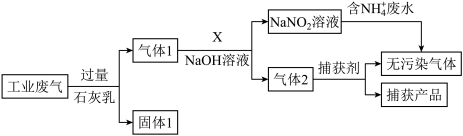
2 . 为落实“五水共治”,某工厂拟综合处理含 废水和工业废气(主要含
废水和工业废气(主要含 、
、 、
、 、
、 、
、 ,不考虑其他成分),设计了如下流程,下列说法错误的是
,不考虑其他成分),设计了如下流程,下列说法错误的是
 废水和工业废气(主要含
废水和工业废气(主要含 、
、 、
、 、
、 、
、 ,不考虑其他成分),设计了如下流程,下列说法错误的是
,不考虑其他成分),设计了如下流程,下列说法错误的是
A.固体1中主要含有 、 、 、 、 |
| B.捕获剂捕获的气体主要是CO,防止污染空气 |
C.X可以是空气,当它过量时会导致废水中 的去除率下降 的去除率下降 |
D.通过处理含 的废水,可生成标况下 的废水,可生成标况下 无污染气体 无污染气体 |
您最近半年使用:0次
名校
3 . 为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”,其中包括8位中国青年化学家。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。回答下列问题:
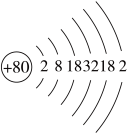
(1)上图为汞的原子结构示意图,汞在第___________ 周期。
(2)①叠氮化钠 可用于汽车安全气囊的产气药,
可用于汽车安全气囊的产气药, 在撞击时能发生分解反应生成两种单质。计算理论上
在撞击时能发生分解反应生成两种单质。计算理论上 完全分解,释放出标准状况下的气体体积
完全分解,释放出标准状况下的气体体积___________ L。
②氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,工业将氧化铝、氮气和碳在一定条件下反应制得AlN和CO,请将下列的化学反应方程式配平,并用单线桥表示电子转移情况___________ 。
_________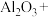 _____
_____ _____
_____ 
 ________AlN+________CO
________AlN+________CO
(3)利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的“价—类”二维图:

①从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有___________ (填化学式)。
②Z的浓溶液与铝单质在加热条件下可以发生化学反应生成Y,该反应的化学方程式为___________ ,可用___________ 法收集Y(填序号)
A.向上排空气 B.向下排空气 C.排饱和食盐水 D.排饱和 溶液
溶液
③Y和 均能使品红溶液褪色,但两种气体按一定比例同时通入品红溶液中无明显现象。请用离子方程式解释原因
均能使品红溶液褪色,但两种气体按一定比例同时通入品红溶液中无明显现象。请用离子方程式解释原因___________ 。

(1)上图为汞的原子结构示意图,汞在第
(2)①叠氮化钠
 可用于汽车安全气囊的产气药,
可用于汽车安全气囊的产气药, 在撞击时能发生分解反应生成两种单质。计算理论上
在撞击时能发生分解反应生成两种单质。计算理论上 完全分解,释放出标准状况下的气体体积
完全分解,释放出标准状况下的气体体积②氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,工业将氧化铝、氮气和碳在一定条件下反应制得AlN和CO,请将下列的化学反应方程式配平,并用单线桥表示电子转移情况
_________
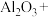 _____
_____ _____
_____ 
 ________AlN+________CO
________AlN+________CO(3)利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的“价—类”二维图:

①从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有
②Z的浓溶液与铝单质在加热条件下可以发生化学反应生成Y,该反应的化学方程式为
A.向上排空气 B.向下排空气 C.排饱和食盐水 D.排饱和
 溶液
溶液③Y和
 均能使品红溶液褪色,但两种气体按一定比例同时通入品红溶液中无明显现象。请用离子方程式解释原因
均能使品红溶液褪色,但两种气体按一定比例同时通入品红溶液中无明显现象。请用离子方程式解释原因
您最近半年使用:0次
2023-03-22更新
|
209次组卷
|
2卷引用:重庆西南大学附属中学2022-2023学年高一下学期第一次月考化学试题
名校
解题方法
4 . 纳米级 可用于以太阳能为热源分解水制
可用于以太阳能为热源分解水制 ,过程如图所示。下列说法不正确的是
,过程如图所示。下列说法不正确的是
 可用于以太阳能为热源分解水制
可用于以太阳能为热源分解水制 ,过程如图所示。下列说法不正确的是
,过程如图所示。下列说法不正确的是
A. 中Fe元素的化合价为+2、+3 中Fe元素的化合价为+2、+3 |
B.过程I中每消耗 转移2mol电子 转移2mol电子 |
C.过程Ⅱ的化学方程式为 |
D.铁氧化合物循环制 具有节约能源、产物易分离等优点 具有节约能源、产物易分离等优点 |
您最近半年使用:0次
2023-02-16更新
|
448次组卷
|
6卷引用:重庆市西南大学附属中学校2022-2023学年高一上学期期末考试化学试题
重庆市西南大学附属中学校2022-2023学年高一上学期期末考试化学试题(已下线)第13讲 铁和铁的氧化物-【暑假自学课】2023年新高一化学暑假精品课(人教版2019必修第一册)湖南省株洲市炎陵县2022-2023学年高一下学期3月月考化学试题辽宁省六校协作体2023-2024学年高一上学期第三次考试化学试题广西柳州铁一中学2023-2024学年高一上学期期末考试化学试卷 河南省南阳市第一中学校2023-2024学年高一上学期第四次月考化学试题
名校
5 . 下列指定反应的离子方程式正确的是
| A.Ca(NO3)2溶液中通入少量CO2:Ca2++CO2+H2O=CaCO3↓+2H+ |
| B.KI溶液中加入少量已酸化的双氧水:2H++2I-+H2O2=I2+O2↑+2H2O |
| C.向AgNO3溶液滴入氨水至沉淀刚好消失:Ag++2NH3·H2O=[Ag(NH3)2]++OH- |
D.Ba(OH)2溶液中加少量NaHCO3溶液:Ba2++OH-+HCO =BaCO3↓+H2O =BaCO3↓+H2O |
您最近半年使用:0次
6 . 烯烃不对称环氧化在药物合成中应用广泛,如图为手性酮催化的烯烃不对称环氧化反应的机理图(部分产物未写出):
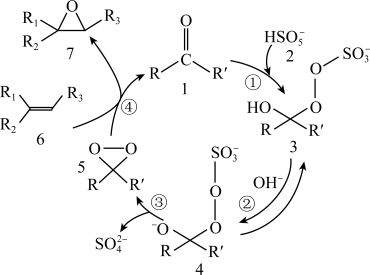
下列说法不正确的是

下列说法不正确的是
A.总反应方程式为OH-+HSO + +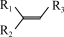  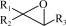 +SO +SO +H2O +H2O |
| B.1是催化剂,反应过程中pH应该控制在合理范围内 |
| C.2、3、4、5均具有较强氧化性 |
| D.4到5的转化过程中有极性键和非极性键的断裂与形成 |
您最近半年使用:0次
2022-04-01更新
|
726次组卷
|
4卷引用:重庆市西南大学附属中学校2022届高三模拟考试(一)化学试题
重庆市西南大学附属中学校2022届高三模拟考试(一)化学试题(已下线)【奋进985】05-备战2022年高考化学名校进阶模拟卷(通用版)湖北省华中师范大学第一附属中学2022届高三学业水平等级考试模拟演练(一)化学试题湖北省普通高中2022届高三学业水平选择性考试5月适应性考试化学试题
7 . 在浓盐酸中H3AsO3与SnCl2反应的离子方程式为:3SnCl2 + 12Cl-+ 2H3AsO3 + 6H+=2As + 3SnCl + 6M。关于该反应的说法中正确的组合是
+ 6M。关于该反应的说法中正确的组合是
①氧化剂是H3AsO3 ②每生成1molAs,反应中转移电子的物质的量为3 mol
③还原性:Cl-> As ④M为OH- ⑤SnCl 是氧化产物
是氧化产物
 + 6M。关于该反应的说法中正确的组合是
+ 6M。关于该反应的说法中正确的组合是 ①氧化剂是H3AsO3 ②每生成1molAs,反应中转移电子的物质的量为3 mol
③还原性:Cl-> As ④M为OH- ⑤SnCl
 是氧化产物
是氧化产物| A.①②⑤ | B.①③④⑤ | C.①②③④ | D.只有①② |
您最近半年使用:0次
8 . 已知以下四个反应:
①4HCl(浓)+MnO2 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
②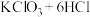 (浓)
(浓)
③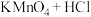 (浓)
(浓)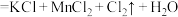 (未配平)
(未配平)
④
根据以上四个反应,回答下列有关问题:
(1)反应①中,氧化产物与还原产物的质量比为___________ 。(写最简整数比)
(2)反应②中氧化剂与还原剂的个数之比为___________ 。(写最简整数比)
(3)若要制得相同质量的氯气,①②反应中电子转移的数目之比为_______ 。(写最简整数比)
(4)请将反应③配平:
 (浓)=
(浓)=



________
(5)请用单线桥表示反应④的电子转移情况:
__________
(6)将 ,
, ,
, 按由强到弱的氧化性顺序排序
按由强到弱的氧化性顺序排序___________ 。(例A>B>C)
①4HCl(浓)+MnO2
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O②
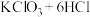 (浓)
(浓)
③
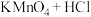 (浓)
(浓)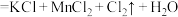 (未配平)
(未配平)④

根据以上四个反应,回答下列有关问题:
(1)反应①中,氧化产物与还原产物的质量比为
(2)反应②中氧化剂与还原剂的个数之比为
(3)若要制得相同质量的氯气,①②反应中电子转移的数目之比为
(4)请将反应③配平:

 (浓)=
(浓)=



(5)请用单线桥表示反应④的电子转移情况:

(6)将
 ,
, ,
, 按由强到弱的氧化性顺序排序
按由强到弱的氧化性顺序排序
您最近半年使用:0次
9 . 回答下列问题:
(1)请配平以下的氧化还原方程式:。
①□ □
□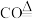 □
□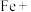 □
□
______
②□ □
□ □
□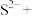 □
□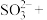 □
□
______
③□ □
□ □_______=□
□_______=□ □
□ □
□ (缺了一种反应物)
(缺了一种反应物)________
(2)已知还原性强弱顺序是 ,向含有
,向含有 、
、 、
、 的溶液中通入氯气,先被氧化的离子是
的溶液中通入氯气,先被氧化的离子是___________ 。
(3)高铁酸钠(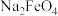 )被公认为绿色净水剂,比
)被公认为绿色净水剂,比 、
、 ,
, 氧化性更强,无二次污染:
氧化性更强,无二次污染:
①干法制备高铁酸钠的主要反应为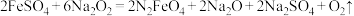 ,该反应中的氧化剂为
,该反应中的氧化剂为___________ ,氧化产物为___________ 。
②除了干法制备高铁酸钠,还可用湿法制备高铁酸钠,其反应物和生成物共有七种微粒: 、
、 、
、 、
、 、
、 、
、 、
、 ,写出该反应的离子方程式:
,写出该反应的离子方程式:___________ 。
(1)请配平以下的氧化还原方程式:。
①□
 □
□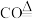 □
□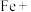 □
□
②□
 □
□ □
□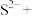 □
□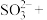 □
□
③□
 □
□ □_______=□
□_______=□ □
□ □
□ (缺了一种反应物)
(缺了一种反应物)(2)已知还原性强弱顺序是
 ,向含有
,向含有 、
、 、
、 的溶液中通入氯气,先被氧化的离子是
的溶液中通入氯气,先被氧化的离子是(3)高铁酸钠(
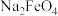 )被公认为绿色净水剂,比
)被公认为绿色净水剂,比 、
、 ,
, 氧化性更强,无二次污染:
氧化性更强,无二次污染:①干法制备高铁酸钠的主要反应为
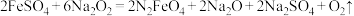 ,该反应中的氧化剂为
,该反应中的氧化剂为②除了干法制备高铁酸钠,还可用湿法制备高铁酸钠,其反应物和生成物共有七种微粒:
 、
、 、
、 、
、 、
、 、
、 、
、 ,写出该反应的离子方程式:
,写出该反应的离子方程式:
您最近半年使用:0次
2021-10-24更新
|
1535次组卷
|
2卷引用:重庆西南大学附属中学校2021-2022学年高一上学期第二次测试化学试题
名校
解题方法
10 . 我国四大发明之一的黑火药是由硫磺粉、 和木炭粉按一定比例混合而成的,爆炸时的反应为:
和木炭粉按一定比例混合而成的,爆炸时的反应为: 。下列说法正确的是
。下列说法正确的是
 和木炭粉按一定比例混合而成的,爆炸时的反应为:
和木炭粉按一定比例混合而成的,爆炸时的反应为: 。下列说法正确的是
。下列说法正确的是A.生成物中只有 是还原产物 是还原产物 |
| B.用双线桥表示该反应中的电子转移总数目为10e- |
| C.该反应为离子反应 |
| D.该反应中只有C作还原剂 |
您最近半年使用:0次
2021-10-24更新
|
165次组卷
|
2卷引用:重庆西南大学附属中学校2021-2022学年高一上学期第二次测试化学试题



